Maladie à virus Ebola
La maladie à virus Ebola[2], également appelée fièvre hémorragique Ebola ou fièvre d’Ebola[3] (en anglais : Ebola virus disease ou EVD), est la maladie provoquée par le virus Ebola, qui touche les primates et d'autres animaux tels que le porc. Il s'agit d'une fièvre hémorragique virale aiguë accompagnée d'une atteinte sévère de l'hémostase et du système immunitaire conduisant à une grave immunodépression[4],[5]. Présentant un tableau clinique identique à celui des affections à virus Marburg, la maladie à virus Ebola est réputée plus grave et le plus souvent mortelle chez l'homme, avec un taux de létalité atteignant parfois 90 % lors des flambées épidémiques. Ces dernières surviennent principalement dans les villages isolés d'Afrique centrale et d'Afrique de l'Ouest, à proximité des forêts de feuillus humides tropicales et subtropicales[4]. Aucun facteur de prédisposition à l'infection n'a été identifié ; toutefois, les personnes de 20 à 30 ans semblent particulièrement sensibles au virus.
| Causes | Virus Ebola transmis par contact direct |
|---|---|
| Transmission | Transmission par contact (d) et transmission de l'agent pathogène par contact hématologique (d) |
| Incubation min | 2 j |
| Incubation max | 21 j |
| Début habituel | Après 2 jours à 3 semaines d'incubation |
| Symptômes | fièvre soudaine, asthénie, myalgie, arthralgie, céphalée, diarrhée, vomissements, douleurs abdominales soudaines, conjonctivite, exanthème, état de choc, œdème cérébral, coagulopathie, infection bactérienne secondaire, pharyngite, ulcérations, hémorragies multiples |
| Complications | Hypovolémie |
| Diagnostic | ARN viral ou anticorps sanguins |
|---|---|
| Différentiel | Paludisme, choléra, fièvre typhoïde, méningite, autre fièvre hémorragique (fièvre de Lassa...) |
| Prévention | Coordination et sécurité sanitaire, acceptation du risque de la viande de brousse, anthropologie et représentation de l'infection et des informations fournies. |
| Traitement | Symptomatique |
| Pronostic | 25-90% de mortalité |
| Spécialité | Infectiologie |
| CISP-2 | A77 |
|---|---|
| CIM-10 | A98.4 |
| CIM-9 | 065.8 |
| DiseasesDB | 18043 |
| MedlinePlus | 001339 |
| eMedicine | 216288 |
| MeSH | D019142 |
Il n'existe pas encore de vaccin ni de traitement spécifique homologué[6],[7], bien que plusieurs d'entre eux soient localement en cours d'essais cliniques sous le contrôle de l'OMS contre l'épidémie apparue en Afrique de l'Ouest en 2014, tels que le cAd3-ZEBOV, le VSV-EBOV, le favipiravir (Avigan), ou encore le brincidofovir. La prise en charge des personnes atteintes repose avant tout sur des soins palliatifs intensifs. Le virus se transmet à l'homme à partir d'animaux sauvages et circule ensuite au sein des populations humaines par contact avec les fluides corporels de personnes présentant les symptômes de la maladie (à l'issue de la période d'incubation), voire par voie entérale[8], mais pas par aérosols (voie aérienne)[9]. Des chercheurs pensent que des chauves-souris frugivores de la famille des ptéropodidés constituent le réservoir naturel du virus Ebola[7],[10], bien que les porcs aient été également impliqués dans la transmission d'un virus de même type[11].
L'épidémie qui a sévi en Afrique de l'Ouest en 2014 et 2015 a été provoquée par un virus très semblable à celui identifié lors de précédentes épidémies en République démocratique du Congo, en République du Congo et au Gabon[12],[13], une première étude ayant d'abord fait penser à une mutation de ce virus, à 97 % identique à celui que l'on retrouve en République démocratique du Congo[14]. Elle avait provoqué au , selon les données recueillies par l'OMS à partir des informations communiquées par les autorités des dix[15] pays concernés, la mort de 11 323 personnes sur 28 646 cas recensés[16], soit une létalité globale de 39,5 % ; si la remontée d'informations s'est par la suite progressivement fiabilisée, l'OMS avait cependant averti le 14 août 2014 que « les équipes opérant sur les sites de l'épidémie constatent des signes évidents que les données rapportées sur le nombre de cas et de morts sous-évaluent largement l'ampleur de l'épidémie »[17].
Une nouvelle épidémie frappe la République démocratique du Congo en 2019, faisant plus de 2 000 morts[18],[19].
En 2021, plusieurs cas sont à nouveau détectés dans la région de Nzérékoré, au Sud-Est de la Guinée[20].
Agent infectieux
modifierComme le virus Marburg, le virus Ebola appartient à la famille des Filoviridae (filovirus), de l'ordre des Mononegavirales (mononégavirus). Il a été décrit pour la première fois en 1976 par David Finkes[23]. Les Filoviridae sont des virus à ARN de forme filamenteuse, d'où leur nom. Le génome du virus Ebola contient sept gènes qui codent neuf protéines différentes[24].
Le genre Ebolavirus regroupe cinq espèces différentes[25],[26] :
- ebolavirus Zaïre, identifiée au Zaïre en 1976 (la souche découverte en 2014 appartient à cette espèce[27]) ;
- ebolavirus Soudan, identifiée au Soudan en 1976 ;
- ebolavirus Reston, identifiée dans le secteur de Reston aux États-Unis en 1989[28] ;
- ebolavirus Forêt de Taï (anciennement appelée Ebola-Côte d'Ivoire), identifiée dans le parc national de Taï en Côte d'Ivoire en 1994 ;
- ebolavirus Bundibugyo, identifiée à Bundibugyo, en Ouganda en 2008.
Les deux premières (Zaïre et Soudan) sont responsables de la quasi-totalité des cas humains[24]. Le virus philippino-américano-africain (Reston) semble être transmissible aux humains (par contact de fluides, comme les autres souches, et aéroporté) mais sans donner de signes cliniques[29].
Le virus Ebola peut être linéaire ou ramifié, long de 0,8 à 1 μm mais pouvant atteindre 14 μm[30] par concatémérisation (formation d'une particule longue par concaténation de particules plus courtes), avec un diamètre constant de 80 nm. Il possède une capside nucléaire hélicoïdale de 20 à 30 nm de diamètre constituée de nucléoprotéines NP et VP30, elle-même enveloppée d'une matrice hélicoïdale de 40 à 50 nm de diamètre constituée de protéines VP24 et VP40 et comprenant des stries transversales de 5 nm[4].
Action pathogène
modifierComme les autres filovirus, le virus Ebola attaque l'ensemble de l'organisme en y provoquant une coagulation intravasculaire disséminée (CIVD) croissante qui dégrade rapidement l'hémostase et le fonctionnement des organes vitaux[31]. L'infection vise en priorité les cellules endothéliales, les phagocytes mononucléaires — monocytes, macrophages, cellules dendritiques, mastocytes — et les hépatocytes. Elle s'accompagne par ailleurs de la rapide neutralisation de certaines populations de lymphocytes T par un effet superantigène[32].
L'entrée du virus dans les cellules repose sur la protéine NPC1[33],[34], codée par un gène en 18q11 dont la mutation provoque la maladie de Niemann-Pick type C, une maladie lysosomale caractérisée par l'accumulation de cholestérol non estérifié et de glycolipides dans les lysosomes. Dans les cellules normales, la protéine NPC1 agit avec la protéine NPC2 pour transporter les grosses molécules hydrophobes à travers le système endosome-lysosome ; il a été observé que, lorsque cette protéine n'est pas fonctionnelle, ni le virus Ebola ni le virus Marburg ne peuvent entrer dans la cellule, cette dernière demeurant donc indemne malgré la présence des virus dans son environnement. Une étude complémentaire a montré que le deuxième domaine lysosomal de la protéine NPC1 se lie directement à la glycoprotéine de l'enveloppe virale de ces virus[35].
Une fois le virus dans la cellule, il sécrète la glycoprotéine soluble sGP et la glycoprotéine structurelle GP. La réplication du virus sature la biosynthèse des protéines dans les cellules infectées et notamment celles du système immunitaire de l'hôte. La glycoprotéine GP forme un complexe trimérique liant le virus aux cellules endothéliales qui tapissent l'intérieur des vaisseaux sanguins, tandis que la glycoprotéine sécrétée sGP forme un dimère qui interfère avec les granulocytes neutrophiles, un type de leucocytes, permettant au virus d'échapper au système immunitaire de l'hôte par inactivation précoce des neutrophiles. Ces leucocytes inactivés servent alors de transporteurs du virus à travers l'ensemble de l'organisme pour notamment contaminer les ganglions lymphatiques, le foie, les poumons et la rate[36]. La présence des particules virales et les dommages causées aux cellules par leur éclosion provoquent la libération de cytokines — TNFα, IL-6, IL-8, etc. — qui sont les molécules de signalisation cellulaire provoquant fièvre et inflammation. L'atteinte des cellules épithéliales par effet cytopathique conduit à la perte de l'intégrité vasculaire, aggravée d'une part par la glycoprotéine virale qui réduit l'efficacité des intégrines responsables de l'adhérence des cellules au sein des structures intercellulaires, et d'autre part par les atteintes hépatiques, responsables de la coagulopathie[37].
Symptômes et évolution
modifierLes premiers signes de la maladie apparaissent au bout d'une incubation de deux jours à trois semaines, le plus souvent entre 4 et 9 jours[39]. Il s'agit de symptômes non spécifiques rappelant ceux de la grippe : fièvre soudaine, asthénie, myalgie, arthralgie, céphalée, diarrhée, vomissements et douleurs abdominales soudaines[40]. D'autres symptômes initiaux peuvent parfois accompagner ce tableau : conjonctivite, irritation de la gorge, exanthème, insuffisance rénale et insuffisance hépatocellulaire, avec éventuellement, dès le début de l'affection, état de choc, œdème cérébral, coagulopathie et infection bactérienne secondaire[41]. À ce stade, des hémorragies internes et externes peuvent déjà être observées chez certains patients.
Les symptômes hémorragiques apparaissent généralement quatre à cinq jours après l'infection, comprenant pharyngite, ulcérations buccales et labiales, saignement des gencives et des yeux (conjonctivite hémorragique), et rejets de sang par la bouche (hématémèse), le nez (épistaxis), l'anus (méléna), l'urine (hématurie) ainsi que par saignements vaginaux[42]. On peut également observer des lésions hépatiques, une augmentation du taux sérique de transaminases, une insuffisance médullaire — baisse de la numération leucocytaire (leucopénie) et plaquettaire (thrombopénie) — et une protéinurie.[réf. nécessaire]
En phase terminale de la maladie, on observe habituellement normothermie (absence de fièvre), obnubilation, anurie, état de choc, tachypnée, arthralgie et atteinte oculaire. La coagulopathie est souvent accompagnée d'insuffisance rénale, de lésions hépatiques, d'une atteinte du système nerveux central et d'un choc terminal avec défaillance polyviscérale entraînant la mort.[réf. nécessaire]
Le virus peut également se manifester sous forme d'une virose aiguë accompagnée de malaise et d'une éruption maculopapuleuse (en). Les femmes enceintes perdent généralement leur fœtus avec des saignements abondants. Le taux de létalité varie de 25 à 90 % selon le type de virus et les conditions de prise en charge[43], la plupart des morts résultant dans ce cas de la déshydratation consécutive aux atteintes gastriques[39].
Les sujets touchés par le virus demeurent contagieux tant que le virion est présent dans leur sang, leurs sécrétions, leurs organes et leur sperme ; le virus Ebola a été observé dans le liquide séminal 61 jours après l'apparition des symptômes de la maladie. Une transmission par le sperme sept semaines après le rétablissement clinique du patient a été constatée et une autre cinq mois après le rétablissement[44].
Le mode d'exposition au virus semble influer sur la sévérité et la rapidité d'évolution de la maladie. Ainsi, lors de l'épidémie de 1976 au Zaïre, déclenchée au Yambuku Mission Hospital (YMH) par la réutilisation d'aiguilles de seringues contaminées par un patient à qui l'on avait injecté de la chloroquine pour traiter ce qu'on pensait être une crise de paludisme[45], la durée moyenne d'incubation était de 6,3 jours en cas de contamination par injection contre 9,5 jours en cas de contamination par contact, lorsque le mode de contamination avait pu être déterminé. De plus, le taux de létalité s'établissait respectivement à 100 % (85 morts sur 85 patients) et 80 % (119 morts sur 149 patients)[24].
Enfin, il convient de noter que certains individus infectés par le virus Ebola demeurent asymptomatiques[46] ; la cause de cette absence de manifestation pathologique chez ces personnes n'est pas connue.
Diagnostic
modifierLe diagnostic différentiel d'une maladie à virus Ebola doit être évalué par rapport au paludisme, la fièvre typhoïde, la shigellose, le choléra, la leptospirose, la peste bubonique, la rickettsiose, la fièvre récurrente, la méningite, une hépatite et d'autres fièvres hémorragiques virales[2] (fièvre de Lassa, fièvre hémorragique à syndrome rénal (FHSR), fièvre Congo-Crimée, Virus Marburg, etc.).[réf. nécessaire]
Le diagnostic d'une maladie à virus Ebola peut être établi notamment par titrage immunoenzymatique (ELISA) afin de détecter les anticorps anti-Ebola ou les antigènes viraux[42], par amplification génique précédée d'une transcription inverse (RT-PCR) afin de détecter l'ADN dérivé de l'ARN viral, par microscopie immunoélectronique afin d'observer les particules virales dans les tissus et les cellules, et par immunofluorescence indirecte afin de détecter les anticorps antiviraux[42],[47]. Il existe des kits diagnostiques pouvant dépister l'ARN viral au lit du patient. Ces tests peuvent néanmoins être négatifs au tout début de la maladie[48].
Les échantillons prélevés sur de tels patients représentent un risque biologique extrême et ne doivent être analysés que dans le cadre d'un confinement adapté en conséquence.[réf. nécessaire]
Prise en charge et prévention
modifierIl n'existe pas de traitement homologué contre la maladie à virus Ebola[6],[7]. La prise en charge des cas graves consiste en des soins palliatifs intensifs destinés à maintenir la fonction rénale et l'équilibre électrolytique tout en limitant les hémorragies et l'état de choc[8]. La nature particulièrement infectieuse et contagieuse de l'agent pathogène implique de prendre d'emblée les mesures prophylactiques appropriées, d'abord par l'instauration d'une zone de quarantaine autour des régions sujettes à des flambées épidémiques, puis au sein des centres de soin afin de limiter les contaminations nosocomiales et la transmission aux personnels soignants. La manipulation du virus est réglementée et ne doit être entreprise qu'au sein de laboratoires P4, ou BSL-4, conçus pour prévenir les risques de contamination.[réf. nécessaire]
Survie du virus hors d'un hôte
modifierLe virus Ebola peut survivre hors d'un hôte et demeurer infectieux pendant plusieurs jours à température ambiante ou à 4 °C[6], aussi bien dans un liquide que sur une matière sèche (par exemple sur une couverture, des vêtements). Il peut demeurer infectieux sur une période indéterminée à −70 °C ainsi que par lyophilisation. [réf. nécessaire]
Il peut être inactivé par chauffage à 60 °C pendant 30 à 60 minutes, par ébullition pendant 5 minutes ou par exposition aux rayons γ[49] ou ultraviolets[4],[50]. Il est sensible à certains agents chimiques tels que les détergents comme le laurylsulfate de sodium, le paraformaldéhyde, le formaldéhyde, l'acide acétique à 3 % (pH 2,5), l'acide peracétique, la β-propiolactone, le Triton X-100 à 0,25 %, le glutaraldéhyde 2 %, le désoxycholate de sodium, l'éther diéthylique, le méthanol, les désinfectants phénoliques, les solvants lipidiques et l'hypochlorite de sodium (eau de Javel)[47],[50],[51],[52].
Prévention en milieu hospitalier
modifierLes symptômes initiaux d'une maladie à virus Ebola n'étant pas spécifiques, il n'est pas toujours possible d'identifier rapidement les patients qui en sont atteints. C'est la raison pour laquelle les personnels soignants doivent appliquer en permanence les précautions d'usage à tous les patients, et ce indépendamment du diagnostic[2] :
- hygiène des mains ;
- hygiène respiratoire ;
- port d'un équipement de protection individuel, en cas de risque d'éclaboussures ou d'autres contacts avec des matières infectées ;
- sécurité des injections et des rites funéraires.
En présence d'une infection à virus Ebola suspectée ou confirmée, les personnels soignants doivent de surcroît éviter tout contact avec le sang ou les fluides biologiques du patient et toute exposition directe à l'environnement susceptible d'être contaminé. Les contacts rapprochés — à moins d'un mètre — avec ces patients requièrent le port d'une protection faciale (masque chirurgical et lunettes de protection), d'une blouse à manches longues et de gants[réf. nécessaire].
Le Conseil Supérieur de la Santé belge a publié en 2014 un document[53] dans lequel il définit, pour les hôpitaux belges, la prise en charge des patients chez qui une infection par le virus Ebola ou le virus Marburg est envisagée, suspectée ou confirmée.
Déclenchement des épidémies
modifierLe déclenchement des épidémies n'est pas entièrement compris. Si les chauves-souris frugivores de la famille des ptéropodidés constituent vraisemblablement le réservoir naturel du virus Ebola[7],[10], on a retrouvé des éléments génétiques de filovirus dans le génome de certains petits rongeurs, de chauves-souris insectivores, de musaraignes, de tenrecidés voire de marsupiaux[54], ce qui tendrait à prouver une interaction de plusieurs dizaines de millions d'années entre ces animaux et les filovirus. La contamination des primates à partir de ces animaux pourrait survenir par contact ou par consommation d'aliments souillés, et la contamination de l'homme pourrait elle-même résulter de contacts avec des primates contaminés ou par des animaux porteurs du virus[8].
Transmission interhumaine
modifierAu cours d'une épidémie à virus Ebola, la maladie se transmet entre humains avant tout par contact direct avec les fluides biologiques et les tissus organiques issus de patients présentant les symptômes de la maladie à un stade avancé ou par contacts directs avec les dépouilles[8],[55],[56]. Le rôle de la transmission par voie aérienne (aérosols) dans la diffusion interhumaine du virus a été étudié intensivement depuis des décennies[57], notamment pour évaluer les risques liés au bioterrorisme dans la mesure où une à dix particules virales aérosolisées suffiraient à contaminer un humain[47]. Ce mode de transmission n'a cependant jamais pu être mis en évidence au cours d'une épidémie[9], bien que des expériences en laboratoire sur des primates non humains indiquent que ce mode de contamination existe[58] dans les conditions expérimentales très particulières de ces études.
Ainsi, seule la transmission par contact direct avec la matière organique provenant d'un animal contaminé ou d'une personne présentant les symptômes de la maladie a été observée dans le milieu naturel. [réf. nécessaire]
Traitements expérimentaux
modifierL'élaboration d'un traitement contre cette maladie fait l'objet de recherches actives, motivées notamment par les risques d'une utilisation du virus Ebola à des fins de bioterrorisme. Les pistes sont variées et souvent prometteuses sur les modèles animaux, mais demeurent encore au stade expérimental et peu d'entre elles ont atteint le stade d'essai clinique sur des patients humains. La difficulté majeure, outre le fait de concevoir des traitements et des protections qui soient efficaces sans effets indésirables rédhibitoires, réside dans la nécessité de développer des molécules qui soient transportables et stockables sur les zones d'épidémies, essentiellement en Afrique équatoriale ; cette problématique concerne notamment les traitements envisagés à base d'acides nucléiques, tels que les petits ARN interférents, qui sont des molécules fragiles. [réf. nécessaire]
Essais cliniques en Afrique de l'Ouest
modifierPlusieurs traitements expérimentaux ont été ou sont prévus d'être testés contre l'épidémie sévissant encore en Afrique de l'Ouest en 2015 :
- Favipiravir (Avigan) — Deux études publiées au printemps 2014[59],[60] avaient indiqué qu'un antiviral, le favipiravir, un inhibiteur de l'ARN polymérase ARN-dépendante développé contre divers virus à ARN et notamment celui de la grippe, s'est montré efficace sur des souris, et ce même lorsqu'il était administré six jours après l'exposition de ces rongeurs au virus Ebola. Développé par la société japonaise Toyama Chemical, filiale de Fujifilm basée à Tokyo, il fait partie des traitements envisageables pour agir contre l'épidémie d'Afrique de l'Ouest[61]. Les premiers résultats chez l'être humain s'avèrent décevant[62].
- Brincidofovir (CMX001) — Développé par la société Chimerix, basée à Durham en Caroline du Nord, cet antiviral expérimental s'est montré efficace sur des modèles animaux contre les cytomégalovirus, les adénovirus, le virus BK, le virus de la variole et le virus de l'herpès[63]. Son action contre le virus Ebola était inattendue dans la mesure où il était connu pour agir contre les virus à ADN bicaténaire mais pas contre les virus à ARN monocaténaire. Il est administré depuis janvier 2015 à des patients volontaires à Monrovia, au Liberia[64].
Traitements envisagés pour des essais cliniques
modifierD'autres médicaments sont également sur les rangs pour une éventuelle utilisation sur le terrain en Afrique de l'Ouest compte tenu de l'ampleur des besoins :
- TKM-Ebola — Une étude avait montré en 2010 l'intérêt de petits ARN interférents pour limiter l'expression de l'ARN polymérase ARN-dépendante du virus Ebola[65] en administrant des ARN interférents ciblant cette enzyme ainsi que la protéine VP24 associée à l'enveloppe virale et la protéine VP35, cofacteur de l'ARN polymérase, à quatre macaques rhésus pendant sept jours consécutifs suivant leur exposition au virus : ces singes ont tous les quatre été protégés de l'évolution létale de la maladie. Baptisé TKM-Ebola, ce traitement expérimental, développé par la société canadienne Tekmira Pharmaceuticals[66] basée à Vancouver, était le seul à avoir été testé sur des humains au commencement de l'épidémie de 2014 et a fait l'objet, de la part de la FDA américaine, d'une levée partielle de la suspension des essais cliniques le 7 août[67], permettant son utilisation éventuelle comme traitement dans le cadre de l'épidémie sévissant en Afrique de l'Ouest[68]. Les résultats chez l'être humain n'ont, cependant, pas démontré d'intérêt de ce type de traitement[69].
- BCX4430 (immucilline A) — Développé par la société BioCryst Pharmaceuticals, basée à Durham en Caroline du Nord tout comme la société Chimerix qui a développé le brincidofovir, il serait actif contre le virus Ebola et le virus Marburg[70],[71], et son développement pour une utilisation chez l'homme a été accéléré afin de combler l'absence de traitements disponibles pour lutter contre l'épidémie de maladie à virus Ebola en Afrique de l'Ouest[72].
L'administration de plasma de malades guéris s'avère également décevant[73].
Autres axes de recherche
modifierUne combinaison d'anticorps monoclonaux, le REGN-EB3, ainsi que l'anticorps monoclonal MAb114, sont les seuls, en 2020 à avoir démontré une baisse de la mortalité[74].
Jusque là l'absence de traitement existant conte la maladie à virus Ebola a poussé à tester un grand nombre d'autres antiviraux par rapport à leur action éventuelle contre le virus Ebola[75],[76], y compris des composés naturels tels que la scytovirine (en) et la griffithsine[77],[78] ainsi que des composés synthétiques tels que la 3-déazaneplanocine A (DZNep)[79], le FGI-103, le FGI-104, le FGI-106, le dUY11 et le LJ-001[80]. Diverses autres substances actives ont également été testées, parfois en dehors de tout protocole, comme ce fut le cas pour la lamivudine, ou 3TC, un antiviral normalement utilisé contre le VIH, administré contre le virus Ebola par un praticien libérien, avec certains résultats[81]. Le virus Ebola utilisant un canal calcique endosomique pour pénétrer dans la cellule hôte après macropinocytose, des recherches préliminaires sur des souris, publiées en [82], ont montré que la tétrandrine, un inhibiteur calcique présent dans une herbe médicinale de la médecine traditionnelle chinoise, pourrait présenter un potentiel thérapeutique contre la maladie à virus Ebola. L'association artésunate-amodiaquine semble également diminuer la mortalité de la maladie à virus Ebola[83]. Ont également été testées les molécules JK-05 et Triazavirin (en).
Par ailleurs, les recherches, commencées dès la fin du XXe siècle, avaient notamment exploré les axes suivants :
- une étude publiée en 2013[84] a souligné l'intérêt d'un vaccin protégeant à la fois contre la rage et contre la maladie à virus Ebola développé conjointement par le NIAID et l'université Thomas Jefferson à Philadelphie, dans la mesure où cette approche est susceptible de traiter à la fois les victimes humaines et le réservoir animal du virus Ebola[85] ;
- un mélange de trois anticorps monoclonaux anti-Ebola chimériques de souris et d'homme (anticorps c13C6, h-13F6 et c6D8) produits dans des cellules CHO (cellules d'ovaires de hamsters de Chine) et de Nicotiana benthamiana (une espèce de tabac) a été testé en 2012 avec de bons résultats sur des macaques rhésus[86]. Baptisé ZMapp, ce cocktail, développé par la société californienne Mapp Biopharmaceutical basée à San Diego, a été administré pour la première fois à un humain le 31 juillet 2014 au Liberia pour traiter Kent Brantly, un médecin américain travaillant pour l'organisation caritative chrétienne Samaritan's Purse qui avait développé les symptômes de la maladie depuis le 22 juillet[87] ; sa consœur Nancy Writebol, également contaminée par le virus Ebola, a quant à elle reçu deux doses de ce traitement expérimental les 3 et 4 août. Les deux Américains ont été rapatriés les jours suivants à l'Emory University Hospital d'Atlanta pour être suivis en relation avec les CDC. À la suite de la couverture médiatique internationale offerte à ce traitement, des voix se sont élevées pour en réclamer l'utilisation à plus large échelle[88], poussant les autorités américaines à en autoriser l'utilisation au Liberia le 11 août[89] alors que Barack Obama avait indiqué quatre jours plus tôt que cette option était prématurée[90] ; l'OMS a autorisé le 12 août l'utilisation de médicaments expérimentaux dans le cadre de cette épidémie sous certaines conditions[91], ouvrant la voie à une compétition entre firmes pharmaceutiques sur ce nouveau marché[92]. Les deux patients américains traités au « ZMapp » purent quitter l'hôpital guéris le 21 août[93], tandis que le prêtre espagnol Miguel Pajares, âgé de 75 ans, qui avait également reçu ce traitement expérimental, mourait le 12 août à l'hôpital Carlos III de Madrid[94], où il avait été rapatrié cinq jours plus tôt du Liberia, pays dans lequel il avait contracté la maladie en effectuant une mission pour le compte d'une ONG. Très difficile à produire et en rupture de stock depuis octobre 2014, ce traitement, utilisé ponctuellement en Occident, n'a pas joué de rôle direct pour combattre l'épidémie en Afrique de l'Ouest, en dépit de la très forte médiatisation dont il a fait l'objet à l'été 2014. En 2016, une étude ne parvient toutefois pas à démontrer la supériorité de ce traitement par rapport à une prise en charge standard[95] ;
- une étude plus ancienne avait montré en 2003 l'intérêt de la protéine de nématode anticoagulante c2 recombinante (rNAPc2) comme inhibiteur du facteur VIIa et du facteur tissulaire pour prolonger la survie de macaques rhésus infectés[96] ;
- une étude de 1999[79] indiquait déjà que des inhibiteurs de l'adénosylhomocystéinase, notamment dérivés de la 3-déazaneplanocine A, se sont montrés efficaces pour traiter des souris exposées au virus Ebola.
Vaccins
modifierPlusieurs vaccins sont à l'étude à l'occasion de l'épidémie de 2014 en Afrique de l'Ouest :
- cAd3-ZEBOV — Des études publiées en 2010[97] et en 2006[98] ont montré l'intérêt de vaccins conçus à partir d'adénovirus affectant des chimpanzés dans le matériel génétique desquels le gène de la glycoprotéine du virus Ebola a été inséré. Le groupe britannique GlaxoSmithKline, qui avait acquis cette technologie grâce au rachat en 2013 de la société helvétique Okairos basée à Bâle et spécialisée dans les vaccins ciblant les lymphocytes T, avait annoncé le 10 août[99] son intention de commercialiser un vaccin sur ce principe dès 2015[100]. Les essais cliniques de ce vaccin ont commencé en à Oxford et à Bethesda dans le Maryland[101], puis se sont poursuivis en octobre au Mali. En , il est évalué par GSK en vue de la phase III d'essai clinique[102] pour tenter de contenir l'épidémie d'Afrique de l'Ouest[103].
- VSV-EBOV — Des résultats encourageants sur des modèles animaux (cobaye, souris, macaque rhésus) avaient été obtenus en 2006 avec un vaccin expérimental constitué d'une forme recombinante atténuée du virus de la stomatite vésiculaire — un rhabdovirus — exprimant la glycoprotéine GP du virus Ebola[104] : quatre macaques sur huit avaient survécu après avoir reçu ce traitement 20 à 30 minutes après l'exposition au virus Ebola. Développé par des chercheurs du Laboratoire national de microbiologie (en) du Canada, le VSV-EBOLA stimule une réponse immunitaire dirigée contre la glycoprotéine du virus Ebola et procure donc une protection contre ce dernier. Certains indices laissent également penser que ce vaccin pourrait présenter une action curative sur des patients déjà infectés par le virus[104]. Produit par la société Merck & Co, basée à Whitehouse Station (en) dans le New Jersey, le VSV-EBOV a fait l'objet d'un essai clinique à Genève, en Suisse, au cours duquel des patients ont fait état de douleurs articulaires[102], mais devrait faire l'objet de tests complémentaires en Afrique de l'Ouest[103]. Fin l'OMS diffuse depuis Genève un communiqué de presse et la revue médicale internationale The Lancet publie éditorial et article annonçant des résultats préliminaires de l'étude, débutée le , prometteurs, avec une efficacité vaccinale de 70 à 100 %[105],[106],[107],[108].
- r-VSV Zebov - Le , l'OMS annonce que, lors d'une phase de test, 100% des personnes vaccinées et qui auraient été en contact avec des malades d'Ebola n'auraient pas développé la maladie eux-mêmes[109].
D'autres pistes de recherche de vaccin, préalables à l'épidémie, comprennent :
- un vaccin lyophilisé — donc transportable et stockable — protégeant efficacement les souris a été annoncé en 2011[110], dans lequel la glycoprotéine virale GP est fusionnée avec un anticorps monoclonal reconnaissant un épitope sur cette protéine pour conduire à la formation de complexes immuns Ebola (EIC) ; ces derniers sont administrés en même temps qu'un agoniste de récepteurs de type Toll tel que l'acide polyinosinique-polycytidylique pour en maximiser l'effet ;
- un vaccin à ADN a été proposé dès 1998[111] sous la forme de plasmides codant la nucléoprotéine virale NP ainsi que les glycoprotéines sGP et GP.
Histoire
modifierLes deux premières épidémies recensées par l'OMS ont eu lieu en 1976, au Soudan (151 morts pour 284 cas[113]) et au Zaïre (280 décès pour 318 cas). Un cas mortel est identifié au Zaïre en 1977. De nouvelles contaminations surviennent au Soudan en 1979 : 22 décès pour 34 cas. En 1989, une épidémie touche les singes d'une animalerie de Reston, États-Unis. Elle ne fait aucune victime humaine. Le même type d'épidémie est observé en 1992 en Italie, et en 1996 aux États-Unis[réf. nécessaire].
D'autres contaminations humaines massives surviennent dans les années 1990, en 1994 au Gabon (31 décès pour 52 cas) et en Côte d'Ivoire (un cas, non mortel), en 1995 au Zaïre (254 décès pour 315 cas), en 1996 au Gabon (deux épidémies successives, causant respectivement 21 décès pour 31 cas, de janvier à avril, et 45 décès pour 60 cas, de juillet à décembre). Une infirmière ayant soigné des malades atteints au Gabon meurt de fièvre hémorragique Ebola en Afrique du Sud, la même année[réf. nécessaire].
En 2000, le virus touche pour la première fois l'Ouganda (224 décès pour 425 cas) ; il y revient en 2007 dans la région du lac Albert (37 morts pour 149 cas, soit un taux de létalité inhabituellement bas de 25 %, peut-être en raison d'une souche moins virulente), 2011 (1 cas mortel, à 35 km de la capitale[114]), 2012 (dans le district de Kibale, dans l'ouest du pays : 17 morts pour 24 cas[115]) et 2013 (4 morts pour 7 cas). Une épidémie touche de nouveau le Gabon en 2001-2002 (53 décès pour 65 cas), ainsi que la République du Congo voisine (44 décès pour 59 cas en 2001-2002, 128 décès pour 143 cas de janvier à , 29 décès pour 35 cas en novembre-, 10 décès pour 12 cas en 2005). La République démocratique du Congo est également touchée en 2007 (187 morts pour 264 cas), 2008 (dans le Kasaï-Occidental, 14 décès pour 32 cas) et 2012 (dans la Province orientale, 29 décès pour 54 cas).[réf. nécessaire]
Début 2014, l'Afrique de l'Ouest est le théâtre de l'épidémie de maladie à virus Ebola la plus meurtrière depuis la découverte des premiers cas en 1976[116],[117]. D'abord localisée dans le sud de la Guinée, notamment dans les préfectures de Gueckédou[118], Macenta et Kissidougou, l'épidémie se propage rapidement au Liberia puis dans un deuxième temps à la Sierra Leone[119],[120]. Des cas de maladie à virus Ebola survenus en Sierra Leone lors d'une épidémie de fièvre de Lassa entre 2006 et 2008 et identifiés montrent que le virus était déjà présent dans la région[121]. En juillet 2014, un décès lié au virus survient au Nigéria, il s'agit d'un homme en provenance du Liberia et mort peu après son débarquement à l'aéroport de Lagos[122]. Au , on dénombrait 660 décès pour plus de 1 100 cas de fièvre hémorragique[122].
Le , l'OMS fait état de « chaînes de transmission non détectées » à la suite d'une recrudescence de nouveaux cas en Guinée après plusieurs semaines de faible activité virale[123]. Le , l'OMS diffuse un nouveau bilan de l'épidémie de fièvre hémorragique faisant état de 932 décès en Afrique de l'Ouest[124]. Le , les États-Unis annoncent le premier cas de contraction du virus sur le sol américain[125], ce malade décède des suites de la maladie le . Un membre de l'équipe de soin affectée à ce patient contracte la maladie, il s'agit du premier cas non importé sur le sol américain. Le , un premier cas confirmé est également déclaré en Espagne, qui est également le premier cas en Europe[126].
Notes et références
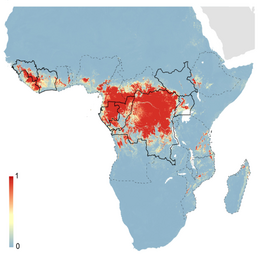
modifier- (en) David M. Pigott, Nick Golding, Adrian Mylne, Zhi Huang, Andrew J. Henry, Daniel J. Weiss, Oliver J. Brady, Moritz U. G. Kraemer, David L. Smith, Catherine L. Moyes, Samir Bhatt, Peter W. Gething, Peter W. Horby, Isaac I. Bogoch, John S. Brownstein, Sumiko R. Mekaru, Andrew J. Tatem, Kamran Khan et Simon I. Hay, « Mapping the zoonotic niche of Ebola virus disease in Africa », eLife, vol. 3, , e04395 (PMID 25201877, PMCID 4166725, DOI 10.7554/eLife.04395, lire en ligne)
- Maladie à virus Ebola sur le site de l'OMS, avril 2014.
- Dictionnaire de l’Académie de médecine.
- (en) Milanga Mwanatambwe, Nobutaka Yamada, Satoru Arai, Masumi Shimizu, Kazuhiro Shichinohe et Goro Asano, « Ebola Hemorrhagic Fever (EHF): Mechanism of Transmission and Pathogenicity », Journal of Nippon Medical School, vol. 68, no 5, , p. 370-375 (PMID 11598619, DOI 10.1272/jnms.68.370, lire en ligne).
- (en) Brian H. Harcourt, Anthony Sanchez et Margaret K. Offermann, « Ebola Virus Selectively Inhibits Responses to Interferons, but Not to Interleukin-1β, in Endothelial Cells », Journal of Virology, vol. 73, no 4, , p. 3491-3496 (PMID 10074208, PMCID 104118, lire en ligne).
- (en) Éric M. Leroy, Pierre Rouquet, Pierre Formenty, Sandrine Souquière, Annelisa Kilbourne, Jean-Marc Froment, Magdalena Bermejo, Sheilag Smit, William Karesh, Robert Swanepoel, Sherif R. Zaki et Pierre E. Rollin, « Multiple Ebola Virus Transmission Events and Rapid Decline of Central African Wildlife », Science, vol. 303, no 5656, , p. 387-390 (PMID 14726594, DOI 10.1126/science.1092528, lire en ligne)
- (en) Eric M. Leroy, Brice Kumulungui, Xavier Pourrut, Pierre Rouquet, Alexandre Hassanin, Philippe Yaba, André Délicat, Janusz T. Paweska, Jean-Paul Gonzalez et Robert Swanepoel, « Fruit bats as reservoirs of Ebola virus », Brief Communications, vol. 438, no 7068, , p. 575-576 (PMID 16319873, DOI 10.1038/438575a, Bibcode 2005Natur.438..575L, lire en ligne).
- (en) Scott F. Dowell, Rose Mukunu, Thomas G. Ksiazek, Ali S. Khan, Pierre E. Rollin et C. J. Peters, « Transmission of Ebola Hemorrhagic Fever: A Study of Risk Factors in Family Members, Kikwit, Democratic Republic of the Congo, 1995 », Journal of Infectious Diseases, vol. 179, no Supplément 1, , S87-S91 (PMID 9988169, DOI 10.1086/514284, lire en ligne).
- (en) Herwig Leirs, James N. Mills, John W. Krebs, James E. Childs, Dudu Akaibe, Neal Woollen, George Ludwig, Clarence J. Peters, Thomas G. Ksiazek et al., « Search for the Ebola Virus Reservoir in Kikwit, Democratic Republic of the Congo: Reflections on a Vertebrate Collection », Journal of Infectious Diseases, vol. 179, no Suppl. 1, , S155-S163 (PMID 9988179, DOI 10.1086/514299, lire en ligne).
- (en) Hana M. Weingart, Carissa Embury-Hyatt, Charles Nfon, Anders Leung, Greg Smith, et Gary Kobinger, « Transmission of Ebola virus from pigs to non-human primates », Scientific Reports, vol. 2, , p. 811 (PMID 23155478, PMCID 3498927, DOI 10.1038/srep00811, lire en ligne).
- (en) Gytis Dudas et Andrew Rambaut, « Phylogenetic Analysis of Guinea 2014 EBOV Ebolavirus Outbreak », PLoS Currents, vol. 6, (PMID 24860690, PMCID 4024086, DOI 10.1371/currents.outbreaks.84eefe5ce43ec9dc0bf0670f7b8b417d, lire en ligne).
- (en) Sébastien Calvignac-Spencer, Jakob M. Schulze, Franziska Zickmann et Bernhard Y. Renard, « Clock Rooting Further Demonstrates that Guinea 2014 EBOV is a Member of the Zaïre Lineage », PLoS Currents, (DOI 10.1371/currents.outbreaks.c0e035c86d721668a6ad7353f7f6fe86, lire en ligne).
- (en) Sylvain Baize, Delphine Pannetier, Lisa Oestereich, Toni Rieger, Lamine Koivogui, N'Faly Magassouba, Barrè Soropogui, Mamadou Saliou Sow, Sakoba Keïta, Hilde De Clerck, Amanda Tiffany, Gemma Dominguez, Mathieu Loua, Alexis Traoré, Moussa Kolié, Emmanuel Roland Malano, Emmanuel Heleze, Anne Bocquin, Stephane Mély, Hervé Raoul, Valérie Caro, Dániel Cadar, Martin Gabriel, Meike Pahlmann, Dennis Tappe, Jonas Schmidt-Chanasit, Benido Impouma, Abdoul Karim Diallo, Pierre Formenty, Michel Van Herp et Stephan Günther, « Emergence of Zaire Ebola Virus Disease in Guinea — Preliminary Report », The New England Journal of Medicine, (PMID 24738640, DOI 10.1056/NEJMoa1404505, lire en ligne).
- Il s'agit de la Guinée, du Liberia, de la Sierra Leone, du Nigeria, du Sénégal, de l'Espagne, des États-Unis, du Mali, du Royaume-Uni et de l'Italie.
- (en) WHO: Ebola Situation Reports publié le 30 mars 2016 sur le site de suivi de l'épidémie de l'Organisation mondiale de la santé.
-
(en) « WHO Ebola news »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), Global Alert and Response (GAR), sur OMS, (consulté le ) :
.« Staff at the outbreak sites see evidence that the numbers of reported cases and deaths vastly underestimate the magnitude of the outbreak. »
- « Ebola en RDC: le cap de mille morts franchi, l'inquiétude redouble », sur dhnet.be, .
- « Epidémie d’Ebola en RDC : le cap des 2 000 morts est franchi », Le Monde, (lire en ligne, consulté le ).
- « Guinée: quatre décès dus à Ebola, les premiers depuis 2016 », La Libre Belgique, (lire en ligne).
- (en) Microscopie électronique en transmission d'un virus Ebola sur le site des Centres pour le contrôle et la prévention des maladies aux États-Unis.
- (en) « Charting the Path of the Deadly Ebola Virus in Central Africa », PLoS Biology, vol. 3, no 11, , e403 (DOI 10.1371/journal.pbio.0030403, lire en ligne).
- (en) Pattyn S, Jacob W, van der Groen G, Piot P, Courteille G. « Isolation of Marburg-like virus from a case of haemorrhagic fever in Zaire » Lancet 1977;309 (8011): 573–4. .
- (en) Heinz Feldmann et Thomas W. Geisbert, « Ebola haemorrhagic fever », The Lancet, vol. 377, no 9768, , p. 849-862 (PMID 21084112, PMCID 3406178, DOI 10.1016/S0140-6736(10)60667-8, lire en ligne).
- (en) Jens H. Kuhn, Stephan Becker, Hideki Ebihara, Thomas W. Geisbert, Karl M. Johnson, Yoshihiro Kawaoka, W. Ian Lipkin, Ana I. Negredo, Sergey V. Netesov, Stuart T. Nichol, Gustavo Palacios, Clarence J. Peters, Antonio Tenorio, Viktor E. Volchkov et Peter B. Jahrling, « Proposal for a revised taxonomy of the family Filoviridae: classification, names of taxa and viruses, and virus abbreviations », Archives of Virology, vol. 155, no 12, , p. 2083-2103 (PMID 21046175, PMCID 3074192, DOI 10.1007/s00705-010-0814-x, lire en ligne).
- OMS, Maladie à virus Ebola
- (en) Sylvain Baize, Delphine Pannetier, Lisa Oestereich, Toni Rieger, Lamine Koivogui, N'Faly Magassouba, Barrè Soropogui, Mamadou Saliou Sow, Sakoba Keïta, Hilde De Clerck, Amanda Tiffany, Gemma Dominguez, Mathieu Loua, Alexis Traoré, Moussa Kolié, Emmanuel Roland Malano, Emmanuel Heleze, Anne Bocquin, Stephane Mély, Hervé Raoul, Valérie Caro, Dániel Cadar, Martin Gabriel, Meike Pahlmann, Dennis Tappe, Jonas Schmidt-Chanasit, Benido Impouma, Abdoul Karim Diallo, Pierre Formenty, Michel Van Herp et Stephan Günther, « Emergence of Zaire Ebola Virus Disease in Guinea - Preliminary Report », N Engl J Med, vol. [prépublication électronique], (PMID 24738640, DOI 10.1056/NEJMoa1404505, lire en ligne [html])
- (en) T. W. Geisbert et P. B. Jahrling, « Use of immunoelectron microscopy to show Ebola virus during the 1989 United States epizootic », Journal of Clinical Pathology (en), vol. 43, no 10, , p. 813-816 (DOI 10.1136/jcp.43.10.813, lire en ligne [PDF], consulté le ).
- (en) Miranda ME, Ksiazek TG, Retuya TJ. et al. « Epidemiology of Ebola (subtype Reston) virus in Philippines, 1996 » J Infect Dis. 1999;179(suppl 1):S115-S119.
- (en) T. W. Geisbert et P.B. Jahrling, « Differentiation of filoviruses by electron microscopy », Virus Research, vol. 39, nos 2-3, , p. 129-150 (PMID 8837880, DOI 10.1016/0168-1702(95)00080-1, lire en ligne).
- (en) Thomas W. Geisbert, Howard A. Young, Peter B. Jahrling, Kelly J. Davis, Elliott Kagan et Lisa E. Hensley, « Mechanisms Underlying Coagulation Abnormalities in Ebola Hemorrhagic Fever: Overexpression of Tissue Factor in Primate Monocytes/Macrophages Is a Key Event », Journal of Infectious Diseases, vol. 188, no 11, , p. 1618-1629 (PMID 14639531, DOI 10.1086/379724, lire en ligne).
- (en) Eric M. Leroy, Pierre Becquart, Nadia Wauquier et Sylvain Baize, « Evidence for Ebola Virus Superantigen Activity », Journal of Virology, vol. 85, no 8, , p. 4041-4042 (PMID 21307193, PMCID 3126126, DOI 10.1128/JVI.00181-11, lire en ligne).
- (en) Jan E. Carette, Matthijs Raaben, Anthony C. Wong, Andrew S. Herbert, Gregor Obernosterer, Nirupama Mulherkar, Ana I. Kuehne, Philip J. Kranzusch, April M. Griffin, Gordon Ruthel, Paola Dal Cin, John M. Dye, Sean P. Whelan, Kartik Chandran et Thijn R. Brummelkamp, « Ebola virus entry requires the cholesterol transporter Niemann–Pick C1 », Nature, vol. 477, no 7364, , p. 340-343 (PMID 21866103, PMCID 3175325, DOI 10.1038/nature10348, Bibcode 2011Natur.477..340C, lire en ligne).
- (en) Marceline Côté, John Misasi, Tao Ren, Anna Bruchez, Kyungae Lee, Claire Marie Filone, Lisa Hensley, Qi Li, Daniel Ory, Kartik Chandran et James Cunningham, « Small molecule inhibitors reveal Niemann–Pick C1 is essential for Ebola virus infection », Nature, vol. 477, no 7364, , p. 344-348 (PMID 21866101, PMCID 3230319, DOI 10.1038/nature10380, Bibcode 2011Natur.477..344C, lire en ligne).
- (en) Emily Happy Miller, Gregor Obernosterer, Matthijs Raaben, Andrew S. Herbert, Maika S. Deffieu, Anuja Krishnan, Esther Ndungo, Rohini G. Sandesara, Jan E. Carette, Ana I. Kuehne, Gordon Ruthel, Suzanne R. Pfeffer, John M. Dye, Sean P. Whelan, Thijn R. Brummelkamp et Kartik Chandran, « Ebola virus entry requires the host-programmed recognition of an intracellular receptor », The EMBO Journal, vol. 31, no 8, , p. 1947-1960 (PMID 22395071, PMCID 3343336, DOI 10.1038/emboj.2012.53, lire en ligne).
- (en) Smith, Tara, Ebola (Deadly Diseases and Epidemics), Chelsea House Publications, (ISBN 0-7910-8505-8)
- (en) Nancy Sullivan, Zhi-Yong Yang et Gary J. Nabel, « Ebola Virus Pathogenesis: Implications for Vaccines and Therapies », Journal of Virology, vol. 77, no 18, , p. 9733-9737 (PMID 12941881, PMCID 224575, DOI 10.1128/JVI.77.18.9733-9737.2003, lire en ligne).
- Image publiée sur flickr par le NIAID (octobre 2014).
- (en) Adrian M. Casillas, Adeline M. Nyamathi, Anthony Sosa, Cam L. Wilder et Heather Sands, « A Current Review of Ebola Virus: Pathogenesis, Clinical Presentation, and Diagnostic Assessment », Biological Research for Nursing, vol. 4, no 4, , p. 268-275 (PMID 12698919, DOI 10.1177/1099800403252603, lire en ligne).
- (en) Mpia A. Bwaka, Marie-José Bonnet, Philippe Calain, Robert Colebunders, Ann De Roo, Yves Guimard, Kasongo R. Katwiki, Kapay Kibadi, Mungala A. Kipasa, Kivudi J. Kuvula, Bwas B. Mapanda, Matondo Massamba, Kibadi D. Mupapa, Jean-Jacques Muyembe-Tamfum, Edouard Ndaberey, Clarence J. Peters, Pierre E. Rollin et Erwin Van den Enden, « Ebola Hemorrhagic Fever in Kikwit, Democratic Republic of the Congo: Clinical Observations in 103 Patients », Journal of Infectious Diseases, vol. 179, no Suppl. 1, , S1-S7 (PMID 9988155, DOI 10.1086/514308).
- (en) Heinz Feldmann, « Are we any closer to combating Ebola infections? », The Lancet, vol. 375, no 9729, , p. 1850-1852 (PMID 20511001, PMCID 3398603, DOI 10.1016/S0140-6736(10)60597-1, lire en ligne).
- (en) Raymond A. Zilinskas, Biological Warfare : Modern Offense and Defense, , 309 p. (ISBN 978-1-55587-761-3, lire en ligne).
- Maladie à virus Ebola. Principaux points, site de l'OMS.
- Mate SE et al. (2015), NEJM. DOI 10.1056/NEJMoa1509773.
- (en) Ebola Zaire Outbreaks sur le site de virologie humaine à l'université Stanford.
- (en) E. M. Leroy, S. Baize, V. E. Volchkov, S. P. Fisher-Hoch, M.-C. Georges-Courbot, J. Lansoud-Soukate, M. Capron, P. Debré, J. B. McCormick et A. J. Georges, « Human asymptomatic Ebola infection and strong inflammatory response », The Lancet, vol. 355, no 9222, , p. 2210-2215 (PMID 10881895, DOI 10.1016/S0140-6736(00)02405-3, lire en ligne).
- (en) David R. Franz, Peter B. Jahrling, Arthur M. Friedlander, David J. McClain, David L. Hoover, W. Russell Bryne, Julie A. Pavlin, George W. Christopher et Edward M. Eitzen Jr, « Clinical Recognition and Management of Patients Exposed to Biological Warfare Agents », JAMA : the Journal of the American Medical Association, vol. 278, no 5, , p. 399-411 (PMID 9244332, DOI 10.1001/jama.1997.03550050061035, lire en ligne).
- Feldmann H, Sprecher A, Geisbert TW, Ebola, N Engl J Med, 2020;382:1832-1842.
- (en) L. H. Elliott, J. B. McCormick et K. M. Johnson, « Inactivation of Lassa, Marburg, and Ebola viruses by gamma irradiation », Journal of Clinical Microbiology, vol. 16, no 4, , p. 704-708 (PMID 7153317, PMCID 272450, lire en ligne).
- (en) S. W. Mitchell et J. B. McCormick, « Physicochemical inactivation of Lassa, Ebola, and Marburg viruses and effect on clinical laboratory analyses », Journal of Clinical Microbiology, vol. 20, no 3, , p. 486-489 (PMID 6490832, PMCID 271356, lire en ligne).
- (en) Mona R. Loutfy, Mehdi Assmar, Deborah C. Hay Burgess et Kevin C. Kain, « Effects of viral hemorrhagic fever inactivation methods on the performance of rapid diagnostic tests for Plasmodium falciparum », Journal of Infectious Diseases, vol. 178, no 6, , p. 1852-1855 (PMID 9815250, DOI 10.1086/314524, lire en ligne).
- (en) Siddhartha Mahanty, Rizwan Kalwar et Pierre E. Rollin, « Cytokine measurement in biological samples after physicochemical treatment for inactivation of biosafety level 4 viral agents », Journal of Medical Virology, vol. 59, no 3, , p. 341-345 (PMID 10502267, lire en ligne) ; doi:10.1002/(SICI)1096-9071(199911)59:3<341::AID-JMV14>3.0.CO;2-C.
- « Practical recommendations to the attention of healthcare professionals and health authorities regarding the identification of and care delivered to suspected or confirmed carriers of highly contagious viruses (of the Ebola or Marburg type) in the context of an epidemic outbreak in West Africa », Avis du Conseil supérieur de la santé no 9188, Conseil Supérieur de la Santé, (consulté le ).
- (en) Derek J Taylor, Robert W Leach et Jeremy Bruenn, « Filoviruses are ancient and integrated into mammalian genomes », BMC Evolutionary Biology, vol. 10, , p. 193 (PMID 20569424, PMCID 2906475, DOI 10.1186/1471-2148-10-193, lire en ligne).
- (en) Daniel G. Bausch, Jonathan S. Towner, Scott F. Dowell, Felix Kaducu, Matthew Lukwiya, Anthony Sanchez, Stuart T. Nichol, Thomas G. Ksiazek et Pierre E. Rollin, « Assessment of the Risk of Ebola Virus Transmission from Bodily Fluids and Fomites », Journal of Infectious Diseases, vol. 196, no 2, , S142-S147 (PMID 17940942, DOI 10.1086/520545, lire en ligne).
- (en) R. R. Arthur, « Ebola in Africa: discoveries in the past decade », Euro Surveillance : Bulletin Européen sur les Maladies Transmissibles = European Communicable Disease Bulletin, vol. 7, no 3, , p. 33-36 (PMID 12631942).
- (en) Elizabeth K. Leffel et Douglas S. Reed, « Marburg and Ebola viruses as aerosol threats », Biosecurity and Bioterrorism : Biodefense Strategy, Practice, and Science, vol. 2, no 3, , p. 186-191 (PMID 15588056, DOI 10.1089/bsp.2004.2.186, lire en ligne).
- (en) E. Johnson, N. Jaax, J. White et P. Jahrling, « Lethal experimental infections of rhesus monkeys by aerosolized Ebola virus », International Journal of Experimental Pathology, vol. 76, no 4, , p. 227-236 (PMID 7547435, PMCID 1997182, lire en ligne).
- (en) Megumi Fujikawa, « Fujifilm Drug Eyed As Possible Treatment for Ebola Virus », sur The Wall Street Journal Japan, (consulté le ).
- Sissoko D, Laouenan C, Folkesson E et al. Experimental treatment with favipiravir for Ebola virus disease (the JIKI Trial): a historically controlled, single-arm proof-of-concept trial in Guinea, PLoS Med, 2016;13:e1001967-e100196
- (en) Debra C. Quenelle, Bernhardt Lampert, Deborah J. Collins, Terri L. Rice, George R. Painter et Earl R. Kern, « Efficacy of CMX001 against Herpes Simplex Virus Infections in Mice and Correlations with Drug Distribution Studies », Journal of Infectious Diseases, vol. 202, no 10, , p. 1492-1499 (PMID 20923374, PMCID 957530, DOI 10.1086/656717, lire en ligne).
- (en) James Harding Giahyue, « Trials of untested Ebola drugs begin in West Africa », sur Reuters, (consulté le ) : « Medecins Sans Frontieres said on Tuesday it began giving brincidofovir, developed by North Carolina-based Chimerix Inc, to consenting confirmed Ebola patients this month at the ELWA 3 center in Monrovia, the capital of Liberia. ».
- (en) Thomas W. Geisbert, Amy C. H. Lee, Marjorie Robbins, Joan B. Geisbert, Anna N. Honko, Vandana Sood, Joshua C. Johnson, Susan de Jong, Iran Tavakoli, Adam Judge, Lisa E. Hensley et Ian MacLachlan, « Postexposure protection of non-human primates against a lethal Ebola virus challenge with RNA interference: a proof-of-concept study », The Lancet, vol. 375, no 9792, , p. 1896-1905 (PMID 20511019, DOI 10.1016/S0140-6736(10)60357-1, lire en ligne).
- (en) About Investigational TKM-Ebola Therapeutic, présentation commerciale sur le site de la société Tekmira.
- (en) Tekmira Conference Call and Webcast Advisory: Corporate Update and Second Quarter Financial Results sur le site de la société Tekmira, le 7 août 2014.
- « Ebola: un traitement expérimental canadien suscite l'intérêt des Américains », sur lefigaro.fr Le Figaro, (consulté le ).
- Dunning J, Sahr F, Rojek A et al. Experimental treatment of Ebola virus disease with TKM-130803: a single-arm phase 2 clinical trial, PLoS Med, 2016;13:e1001997-e1001997.
- (en) Erik De Clercq, « Ebola virus (EBOV) infection: Therapeutic strategies », Biochemical Pharmacology, vol. 93, no 1, , p. 1-10 (PMID 25481298, DOI 10.1016/j.bcp.2014.11.008, lire en ligne).
- (en) Gary Wong, Xiangguo Qiu, Gene G. Olinger et Gary P. Kobingeremail, « Post-exposure therapy of filovirus infections », Trends in Microbiology, vol. 22, no 8, , p. 456-463 (PMID 24794572, DOI 10.1016/j.tim.2014.04.002, lire en ligne).
- (en) « BioCryst to Launch NHP Ebola Drug Safety, Efficacy Studies 'Within Weeks' », sur Forbes, (consulté le ).
- van Griensven J, Edwards T, de Lamballerie X et al. Evaluation of convalescent plasma for Ebola virus disease in Guinea, N Engl J Med, 2016;374:33-42.
- Mulangu S, Dodd LE, Davey RT Jr et al. A randomized, controlled trial of Ebola virus disease therapeutics, N Engl J Med, 2019;381:2293-2303.
- (en) Mike Bray et Jason Paragas, « Experimental therapy of filovirus infections », Antiviral Research, vol. 54, no 1, , p. 1-17 (PMID 11888653, DOI 10.1016/S0166-3542(02)00005-0, lire en ligne).
- (en) Mike Bray, « Defense against filoviruses used as biological weapons », Antiviral Research, vol. 57, nos 1-2, , p. 53-60 (PMID 12615303, DOI 10.1016/S0166-3542(02)00200-0, lire en ligne).
- (en) Christopher Barton, J. Calvin Kouokam, Amanda B. Lasnik, Oded Foreman, Kenneth E. Palmer et al., « Activity of and Effect of Subcutaneous Treatment with the Broad-Spectrum Antiviral Lectin Griffithsin in Two Laboratory Rodent Models », Antimicrobial Agents and Chemotherapy, vol. 58, no 1, , p. 120-127 (PMID 24145548, PMCID 3910741, DOI 10.1128/AAC.01407-13, lire en ligne).
- (en) John Huggins, Zhen-Xi Zhang et Mike Bray, « Antiviral Drug Therapy of Filovirus Infections: S-Adenosylhomocysteine Hydrolase Inhibitors Inhibit Ebola Virus In Vitro and in a Lethal Mouse Model », Journal of Infectious Diseases, vol. 179, no Suppl. 1, , S240-S247 (PMID 9988190, DOI 10.1086/514316, lire en ligne [PDF]).
- (en) Erik De Clercq, « A Cutting-Edge View on the Current State of Antiviral Drug Development », Medicinal Research Review, vol. 33, no 6, , p. 1249-1277 (PMID 23495004, DOI 10.1002/med.21281, lire en ligne).
- Charlotte Boitiaux, « Ebola : l'expérience "désespérée" d'un médecin libérien », sur France 24, (consulté le ).
- (en) Yasuteru Sakurai, Andrey A. Kolokoltsov, Cheng-Chang Chen, Michael W. Tidwell, Robert A. Davey et al., « Two-pore channels control Ebola virus host cell entry and are drug targets for disease treatment », Science, vol. 347, no 6225, , p. 995-998 (DOI 10.1126/science.1258758, lire en ligne).
- (en) Etienne Gignoux, Andrew S. Azman, Martin de Smet, Philippe Azuma, Moses Massaquoi, Dorian Job, Amanda Tiffany, Roberta Petrucci, Esther Sterk, Julien Potet, Motoi Suzuki, Andreas Kurth, Angela Cannas, Anne Bocquin, Thomas Strecker, Christopher Logue, Thomas Pottage, Constanze Yue, Jean-Clement Cabrol, Micaela Serafini et Iza Ciglenecki, « Effect of Artesunate–Amodiaquine on Mortality Related to Ebola Virus Disease », The New England Journal of Medicine, vol. 374, , p. 23-32 (DOI 10.1056/NEJMoa1504605, lire en ligne).
- (en) Joseph E. Blaney, Andrea Marzi, Mallory Willet, Amy B. Papaneri, Christoph Wirblich, Friederike Feldmann, Michael Holbrook, Peter Jahrling, Heinz Feldmann et Matthias J. Schnell, « Antibody Quality and Protection from Lethal Ebola Virus Challenge in Nonhuman Primates Immunized with Rabies Virus Based Bivalent Vaccine », PLoS Pathogens, vol. 9, no 5, , e1003389 (PMID 23737747, PMCID 3667758, DOI 10.1371/journal.ppat.1003389, lire en ligne).
- (en) Rabies Vaccine Protects Nonhuman Primates Against Deadly Ebola Virus sur le site du NIAID, 15 juillet 2013.
- (en) Gene Garrard Olinger, James Pettitt, Do Kim, Cara Working, Larry Zeitlin et al., « Delayed treatment of Ebola virus infection with plant-derived monoclonal antibodies provides protection in rhesus macaques », Proceedings of the National Academy of Sciences of the United States of America, vol. 109, no 44, , p. 18030-18035 (PMID 23071322, PMCID 3497800, DOI 10.1073/pnas.1213709109, lire en ligne).
- « Le « ZMapp », un traitement contre Ebola expérimenté sur deux Américains infectés », sur lemonde.fr, (consulté le ).
- (en) « Why do two white Americans get the Ebola serum while hundreds of Africans die? », sur The Washington Post, (consulté le ).
- (en) « Liberia says US authorities OK use of experimental Ebola drug », sur CNBC, (consulté le ).
- (en) « Obama: 'Premature' to Say U.S. Should Green-light New Ebola Drug », sur NBC News, (consulté le ).
- (en) « Ethical considerations for use of unregistered interventions for Ebola virus disease (EVD) »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur Organisation mondiale de la santé, (consulté le ).
- (en) Andrew Pollack, « As Ebola’s Toll Rises, Drug Makers Race to Test Medicines », sur New York Times, (consulté le ).
- (en) « Dr Kent Brantly, Nancy Writebol leave hospital after Ebola recovery », sur CBC Television, (consulté le ).
- « VIDEO. Ebola: le prêtre espagnol ayant reçu le sérum expérimental est décédé », sur L'Express, (consulté le ).
- The PREVAIL II Writing Group for the Multi-National PREVAIL II Study Team. A randomized, controlled trial of ZMapp for Ebola virus infection, N Engl J Med, 2016;375:1448-1456.
- (en) Thomas W. Geisbert, Lisa E. Hensley, Peter B. Jahrling, Tom Larsen, George P. Vlasuk et al., « Treatment of Ebola virus infection with a recombinant inhibitor of factor VIIa/tissue factor: a study in rhesus monkeys », Lancet, vol. 362, no 9400, , p. 1953-1958 (PMID 14683653, DOI 10.1016/S0140-6736(03)15012-X, lire en ligne).
- (en) William D. Pratt, Danher Wang, Donald K. Nichols, Min Luo, Jan Woraratanadharm, John M. Dye, David H. Holman et John Y. Dong, « Protection of Nonhuman Primates against Two Species of Ebola Virus Infection with a Single Complex Adenovirus Vector », Clinical and Vaccine Immunology, vol. 17, no 4, , p. 572-581 (PMID 20181765, PMCID 2849326, DOI 10.1128/CVI.00467-09, lire en ligne).
- (en) Gary P. Kobinger, Heinz Feldmann, Yan Zhi, Gregory Schumer, Guangping Gao, Friederike Feldmann, Steven Jones et James M. Wilson, « Chimpanzee adenovirus vaccine protects against Zaire Ebola virus », Virology, vol. 346, no 2, , p. 394-401 (PMID 16356525, DOI 10.1016/j.virol.2005.10.042, lire en ligne).
- (en) « Clinical trial to start soon on GSK Ebola vaccine », sur Reuters, (consulté le ).
- (en) « GlaxoSmithKline announces clinical trials of Ebola vaccine 'later this year' », sur The Guardian, (consulté le ).
- (en) Julie E. Ledgerwood, Adam D. DeZure, Daphne A. Stanley, Laura Novik, Mary E. Enama, Nina M. Berkowitz, Zonghui Hu, Gyan Joshi, Aurélie Ploquin, Sandra Sitar, Ingelise J. Gordon, Sarah A. Plummer, LaSonji A. Holman, Cynthia S. Hendel, Galina Yamshchikov, Francois Roman, Alfredo Nicosia, Stefano Colloca, Riccardo Cortese, Robert T. Bailer, Richard M. Schwartz, Mario Roederer, John R. Mascola, Richard A. Koup, Nancy J. Sullivan, Barney S. Graham et l'équipe VRC 207, « Chimpanzee Adenovirus Vector Ebola Vaccine — Preliminary Report », The Nez England Journal of Medicine, (DOI 10.1056/NEJMoa1410863, lire en ligne).
- (en) Martin Enserink, « Ebola vaccines move closer to ultimate test », sur Science, (consulté le ).
- (en) Bahar Gholipour, « Ebola Vaccines: Here's a Look at the 3 Front-Runners », sur LiveScience, (consulté le ).
- (en) Heinz Feldmann, Steven M Jones, Kathleen M Daddario-DiCaprio, Joan B Geisbert, Ute Ströher, Allen Grolla, Mike Bray, Elizabeth A Fritz, Lisa Fernando, Friederike Feldmann, Lisa E Hensley et Thomas W Geisbert, « Effective Post-Exposure Treatment of Ebola Infection », PLoS Pathogens, vol. 3, no 1, , e2 (PMID 17238284, PMCID 1779298, DOI 10.1371/journal.ppat.0030002, lire en ligne).
- « Un vaccin efficace contre le virus Ebola est à portée de main : communiqué de presse »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?) [html], sur who.int, (consulté le ).
- (en) « Editorial : An Ebola vaccine: first results and promising opportunities » [PDF], sur thelancet.com, (consulté le ).
- (en) Ana Maria Henao-Restrepo, Ira M. Longini, Matthias Egger, Marie Paule Kieny, John-Arne Røtting et al., « Efficacy and effectiveness of an rVSV-vectored vaccine expressing Ebola surface glycoprotein: interim results from the Guinea ring vaccination cluster-randomised trial », Lancet, no (prépublication électronique), (DOI 10.1016/S0140-6736(15)61117-5, lire en ligne [PDF]).
- Fabien Goubet, « Le vaccin anti-Ebola testé aux HUG obtient de bons résultats en Guinée », Le Temps, (lire en ligne).
- Stéphany Gardier, « Ebola : un vaccin démontre une efficacité totale », www.pourquoidocteur.fr, (lire en ligne, consulté le )
- (en) Waranyoo Phoolcharoen, John M. Dye, Jacquelyn Kilbourne, Khanrat Piensook, Melissa M. Herbst-Kralovetz et al., « A nonreplicating subunit vaccine protects mice against lethal Ebola virus challenge », Proceedings of the National Academy of Sciences of the United States of America, vol. 108, no 51, , p. 20695-20700 (PMID 22143779, PMCID 3251076, DOI 10.1073/pnas.1117715108, lire en ligne).
- (en) Ling Xu, Anthony Sanchez, Zhi-Yong Yang, Sherif R. Zaki, Gary J. Nabel et al., « Immunization for Ebola virus infection », Nature Medicine, vol. 4, no 1, , p. 37-42 (PMID 9427604, DOI 10.1038/nm0198-037, lire en ligne).
- (en) Image 7042 sur le site des CDC.
- D'après l'OMS, également à l'origine des autres données présentes dans cette partie de l'article.
- Ebola, le retour, communiqué RFI du 15 mai 2011.
- Le virus Ebola a tué 14 personnes en Ouganda depuis début juillet, article France 24 du 28 juillet 2012.
- Epidémie d’Ebola : l’inquiétude se propage, www.ladepeche.fr, le 4 avril 2014.
- Marina Rafenberg et Marie Salah, « Ebola : “Il faut se remobiliser face à ce nouveau pic” », Le Point, (lire en ligne).
- Fièvre Ebola en Guinée: peur sur Guéckédou, nouvelobs.com, le 2 avril 2014.
- http://www.afro.who.int/en/clusters-a-programmes/dpc/epidemic-a-pandemic-alert-and-response/outbreak-news/4106-ebola-virus-disease-west-africa-22-april-2014.html.
- http://www.afro.who.int/en/clusters-a-programmes/dpc/epidemic-a-pandemic-alert-and-response/outbreak-news/4141-ebola-virus-disease-west-africa-situation-as-of-23-may-2014.html.
- (en) R.J. Schoepp, C.A. Rossi, S.H. Khan, A. Goba et J.N. Fair, « Undiagnosed acute viral febrile illnesses, Sierra Leone », Emerging Infectious Diseases, (PMID 24959946, PMCID 4073864, DOI 10.3201/eid2007.131265).
- « Nigeria : un homme meurt du virus Ebola »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur Euronews, .
- OMS, « Maladie à virus Ebola en Afrique de l’Ouest – Bulletin d’information sur les flambées épidémiques »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur who.int, 27 juillet 2014 traduit en français le 30 juillet (consulté le ).
- Lefigaro.fr avec AFP, « Ebola: 932 décès (nouveau bilan de l'OMS) », Le Figaro, (lire en ligne, consulté le ).
- Pauline Fréour, « Ebola : ce qu'implique la découverte d'un cas hors d'Afrique », sur lefigaro.fr, (consulté le ).
- « Un premier cas d'Ebola en Espagne ».
- Cet article est partiellement ou en totalité issu de l'article intitulé « Virus Ebola » (voir la liste des auteurs).
Voir aussi
modifierBibliographie
modifier- Amy Maxmen, « La première bataille gagnée contre Ebola », Pour la science, hors-série no 113, , p. 38-44
Articles connexes
modifier- Virus Ebola
- Vaccin contre le virus Ebola
- Fièvre hémorragique de Marbourg
- Liste d'épidémies liées au virus Ebola
- Épidémie de maladie à virus Ebola en Afrique de l'Ouest
- En littérature, le roman de Paule Constant, Des chauves-souris, des singes et des hommes (2016)
Liens externes
modifier- Notices dans des dictionnaires ou encyclopédies généralistes :
- Ressources relatives à la santé :
- Virus Ebola, Fiche Technique Santé-Sécurité : Agents Pathogènes, sur le site de l'Agence de la santé publique du Canada.
- « Mawah – Le jour où Ebola est arrivé dans notre village », un scroll doc sur l’histoire de la première apparition d’Ebola dans un petit village en plein cœur du Liberia, basé sur le documentaire "survivre à Ebola" de Carl Gierstorfer, diffusé part arte en
- Avis relatif à la conduite à tenir autour des cas suspects de maladie Ebola, sur le site du Haut Conseil de la santé publique
- Maladie à virus Ebola - Information aux voyageurs sur le site de l'ECDC.
- (en) RAPID RISK ASSESSMENT Outbreak of Ebola virus disease in West Africa, 3e mise à jour, 1er août 2014, sur le site de l'ECDC.
- (en) Outbreak of Ebola in West Africa: ECDC assesses the risk, sur le site de l'ECDC.