Rein
Le rein est un organe de l'appareil urinaire des vertébrés. Il a de multiples fonctions : hormonales, de régulation de la pression sanguine et d'élimination des toxines. Il assure ainsi, par filtration et excrétion d'urine, l'équilibre hydroélectrolytique (homéostasie) du sang et de l'organisme en général. Ses fonctions hormonales comprennent la synthèse de l'érythropoïétine, du calcitriol (forme active de la vitamine D) et de la rénine.
| Système | |
|---|---|
| Région | |
| Vascularisation | |
| Drainage veineux | |
| Innervation | |
| Comprend |
| Nom latin |
Ren |
|---|---|
| Grec |
Nephros |
| MeSH |
D007668 |
| TA98 |
A08.1.01.001 |
| TA2 |
3358 |
| FMA |
7203 |
Chez les amniotes, il est le plus souvent pair et situé dans l'abdomen, dans le rétropéritoine, suivant une symétrie plus ou moins bilatérale. Il est de taille et de conformation très variable en fonction des espèces : lisses chez les humains, lobulés chez les ruminants, diffus chez les oiseaux...
Par abus de langage, le langage courant nomme souvent « reins » la zone des vertèbres lombaires (ex.: « tour de reins » pour parler de lombalgie).
Ambivalence
modifierLa fonction complexe de cet organe vital a peut-être suscité l'ambivalence de sa réputation : objet de culte (il est cité 25 fois dans la Bible où il est considéré, selon l'art divinatoire tiré de l'examen hiéroscopique des reins de l'animal sacrifié, comme le siège de la sagesse, de l'intelligence et des émotions, notamment dans le Livre des Psaumes[1]), il a également longtemps été méprisé car jugé peu noble (assimilé à une passoire qui filtre les déchets pour constituer les urines)[2].
Anatomie chez l'être humain
modifierMorphologie
modifierChez l'être humain, les reins sont des organes aplatis, ovoïdes, dits « en haricot ». La face externe est convexe ; la face interne est concave, et accueille le hile qui se projette au niveau de la 1re vertèbre lombaire : il constitue la zone de transit des éléments vasculo-nerveux et des voies excrétrices urinaires.
La surface des reins est lisse chez l'adulte, de couleur rouge-brun. En moyenne, ils ont pour hauteur 12 cm, largeur 6 cm, épaisseur 3 cm[3] et chacun pèse environ 150 g. Ces mensurations sont très variables d'un individu à l'autre.
Situation
modifierLes reins se situent dans l'espace rétropéritonéal, où ils se projettent par leur face postérieure dans la région lombaire. Celle-ci constitue d'ailleurs la principale voie d'abord chirurgical du rein.
Le rein gauche est placé entre la 11e vertèbre thoracique et la 3e lombaire. Le rein droit quant à lui se projette entre la 12e vertèbre thoracique et l'espace entre la 3e et la 4e lombaire. Ce décalage est dû à la pression du foie sus-jacent sur le rein droit.
Ils s'orientent[3] :
- dans le plan frontal, selon un angle d'environ 18° avec l'axe médian (orientés vers le bas et en dehors) ;
- dans le plan transversal, selon un angle de 40 à 60° avec l'axe sagittal (orientés vers l'avant et en dedans)
Vascularisation
modifierUn seul rein suffit pour vivre ; 5 % des individus n'ont qu'un rein, mais dans ce cas il s'agit le plus souvent du rein droit, mieux vascularisé et grâce à la présence du quadrilatère de Rogie qui favorise la stase veineuse et a des répercussions au niveau génital gauche.
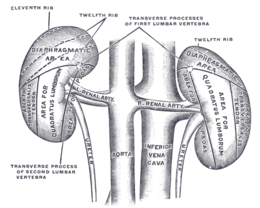
Le rein est vascularisé par les artères et veines rénales et c'est par une échancrure dans la face concave que ces vaisseaux pénètrent dans le rein (hile du rein).
Les artères rénales sont deux artères droite et gauche qui naissent de l’aorte abdominale au niveau de L1. L’artère rénale gauche est plus courte que la droite. Chaque artère rénale donne deux branches terminales : une branche antérieure et une branche postérieure.
Les artères et les veines présentent les subdivisions suivantes, jusqu'au glomérule :
Les veines rénales croisent en avant les artères rénales et se jettent dans la veine cave inférieure au niveau de L2. La veine rénale gauche est plus longue et de gros calibre.
Le parenchyme rénal est entouré d'une capsule dure, très résistante qui le protège. La partie périphérique du parenchyme est le cortex alors que la partie centrale est la médulla. Cette médulla n'est pas continue : elle est interrompue par des prolongements du cortex qui vont jusqu'au sinus rénal.
Innervation
modifierLe rein est innervé par le plexus rénal qui accompagne et entoure l'artère rénale. Il est innervé par le système nerveux sympathique et parasympathique.
L'innervation parasympathique est assurée par le nerf vague (X)[4].
L'innervation sympathique émerge des segments de la moelle spinale T10 à L1. Les fibres pré-synaptiques vont se réunir pour former les nerfs splanchniques, ceux-ci font synapse principalement dans le ganglion aortico-rénal. De là partent les fibres post-synaptiques qui vont innerver le rein[4]. Accessoirement on peut retrouver une innervation du 1er nerf splanchnique lombaire et l'implication des ganglions mésentérique supérieur et rénal.
Pour plus de détails sur l'innervation orthosympathique des viscères de l'abdomen, consulter l'article concernant les plexus prévertébraux.
Physiologie
modifierLe rein a aussi une fonction endocrine (érythropoïétine, système rénine-angiotensine-aldostérone, calcitriol).
En raison de caractéristiques génétiques[5] ou liées aux traits de vie, la capacité des reins varie significativement selon les individus et selon l'âge. Elle est médiocre chez le nouveau-né et décline chez l'adulte avec l'âge. Les capacités fonctionnelles du rein peuvent être dégradées par diverses maladies et par l'exposition à certains toxiques (fluor, plomb, cadmium, autres métaux lourds, alcool ou excès de sodium…). En cas de déficience grave, les derniers recours sont la filtration externe du sang dans un rein artificiel (dialyse), ou la greffe de rein.
Architecture interne du rein
modifierDe l'extérieur vers l'intérieur :
Zone corticale
modifierElle comporte les glomérules, les tubes contournés proximaux et distaux et les tubes collecteurs. Les colonnes de Bertin, dans les espaces entre les pyramides de Malpighi.
Médullaire rénale
modifierLes pyramides rénales ou de Malpighi, dont la base est sous-corticale et la pointe tournée vers l'intérieur, forment les papilles sur lesquelles viennent se ventouser les petits calices. Elles comportent les tubes droits proximaux et distaux ainsi que l'anse de Henle et les canaux de Bellini.
Une pyramide et ses colonnes forment un lobe du rein.
Les néphrons qui se déversent dans le même canal collecteur forment collectivement un lobule du rein.
Calices
modifierLes petits calices recueillent l'urine émise par les pyramides de Malpighi. L'union des petits calices forme les grands calices, il y a trois ou quatre grands calices par rein. Tube abouché à la pointe de la pyramide rénale, et qui en se rejoignant forment le bassinet.
Pelvis rénal ou bassinet
modifierTube en forme d'entonnoir qui se jette dans l'uretère. Il est également appelé pyélon. C'est l'endroit où va passer l'urine à sa sortie du néphron via le tube collecteur. Les bassinets tout comme les calices possèdent un tissu musculaire lisse qui se contracte et propulse l'urine par péristaltisme.
Développement et fonction embryonnaire et fœtale du rein
modifierLe rein est issu de la métamérisation (segmentation puis formation de tubules) du mésoblaste intermédiaire (tissu du disque embryonnaire) en cordon néphrogène au cours de la 3e semaine de développement. Ce cordon se divise en trois régions distinctes dans le temps et l'espace (selon un axe céphalo-caudal) qui vont évoluer successivement:
- le cordon pronéphrogène (le plus céphalique) qui se métamérise en pronéphros. Ce premier rein ne fonctionne pas et dégénère à la fin de la 4e semaine de développement ;
- le cordon mésonéphrogène qui se métamérise après la dégénérescence du pronéphros en mésonéphros. Ce rein fonctionne dès la fin de la 4e semaine de développement, mais il dégénérera également ;
- le cordon métanéphrogène (le plus caudal) qui donne le métanéphros, rein fonctionnel, qui est le rein définitif. Il a la particularité de ne pas se métamériser.
Voir aussi le paragraphe sur l'embryologie du néphron.
Néphron
modifierLe néphron est l'unité structurelle et fonctionnelle de base du rein.
C'est un tubule mince consistant en un amas de capillaires appelés glomérules, entourés d'un bulbe creux, la capsule glomérulaire.
La capsule glomérulaire amène à un long tubule entortillé en deux sections : le tubule contourné proximal, l'anse du néphron, le tubule contourné distal, et le tubule rénal collecteur.
Les tubules collecteurs se déversent dans les calices via les papilles, les calices se jettent dans le pelvis rénal (appelé également pyélon ou bassin), qui est connecté à l'uretère.
Chaque rein humain compte environ un million de néphrons. Le nombre de néphrons, fixé à la naissance, est d'une grande variabilité. Il dépend de multiples facteurs dont l'âge gestationnel, le retard de croissance intra-utérin, l'état nutritionnel maternel.
Formation de l'urine
modifierLe rôle essentiel et le plus connu des reins est la formation de l'urine. Ils éliminent du sang les déchets provenant de la destruction des cellules de l'organisme et de la digestion des aliments [6].
La formation de l'urine et le rejet de celle-ci, comprennent quelques étapes[6]:
- L'artère rénale apporte le sang au rein - Les artères rénales droite et gauche nées de l'aorte apportent une grande quantité de sang aux reins, environ 1700 litres par jour[7],[8], soit un cinquième du débit cardiaque. Elles se divisent en de nombreuses branches pour aboutir à des artérioles microscopiques qui vont alimenter les néphrons ;
- Le néphron filtre le sang et produit l'urine - Chaque rein est constitué d'un million de minuscules canaux juxtaposés appelés néphrons. Chaque néphron comprend un glomérule et un tubule. Le glomérule est un filtre très fin qui retient les globules rouges et les grosses molécules (protéines) mais laisse passer l'eau, les électrolytes (sodium, potassium, calcium...) et les petites molécules (glucose, urée, acide urique, créatinine...). Il en résulte une urine primitive qui va subir des transformations à l'intérieur du tubule. Certaines substances y sont évacuées, d'autres sont réabsorbées, aboutissant à l'urine définitive qui va s'écouler dans les tubes collecteurs ;
- L'urine atteint le bassinet, sorte d'entonnoir - Les tubes collecteurs déversent l'urine dans 8 à 10 calices qui se vident dans le bassinet, sorte d'entonnoir dans lequel s'abouche l'uretère ;
- L'urine est déversée dans deux conduits: les uretères - Les uretères sont des tuyaux de 2,5 mm de diamètre et de 30 cm de long qui, partant du bassinet, vont amener l'urine à la vessie ;
- La vessie stocke puis évacue l'urine par l'urètre - La vessie est un réservoir qui peut contenir jusqu'à 800 ml d'urine. Elle se remplit progressivement et se vide, par un mécanisme déclenché volontairement, laissant échapper l'urine par l'urètre: c'est la miction.
Fonction du rein
modifierHormis sa fonction principale de filtration et d'épuration du sang, le rein intervient à bien des niveaux, notamment dans la régulation de la pression artérielle. Par sa fonction de synthèse de substances spécifiques régulatrices, notamment :
- la rénine synthétisée par le rein et qui va provoquer, via l'angiotensine II (ATII), une stimulation de la sécrétion d'aldostérone, qui est une hormone qui va en cas de baisse de pression artérielle, stimuler la réabsorption de sodium ; or les mouvements d'eau suivent les mouvements de sodium, donc cela va entrainer une réabsorption accrue d'eau qui va faire augmenter la volémie au niveau plasmatique et ainsi faire augmenter la pression dans le sang. Ce n'est qu'un aspect schématique et non exhaustif de la rénine car elle a comme effet également de stimuler la sécrétion de noradrénaline, toujours via l'angiotensine II et ainsi provoquer une vasoconstriction ;
- En cas d'hypertension artérielle (HTA), le rein va synthétiser de la kallikréine pour donner en fin de réaction de la bradykinine (qui est une kinine) qui a des effets vasodilatateurs, donc de réduire la pression au niveau des vaisseaux.
Ceci explique pourquoi l'apport excessif de sel fait augmenter la pression artérielle : les mouvements de sodium dans le rein se font également passivement, donc si on augmente notre apport en sodium (sel), cela entrainera une réabsorption accrue d'eau également provoquant une augmentation de volémie donc de pression car :
PA = DC × Rp
DC = FC × VES
PA = pression artérielle
DC = débit cardiaque
Rp = résistance périphérique
FC = fréquence cardiaque
VES = volume d'éjection systolique (volume éjecté par le ventricule cardiaque gauche à chaque contraction).
On sait que les entrées et sorties en sodium sont équivalentes, la quantité absorbée est éliminée au début mais si l'apport en sel n'est plus ponctuel mais continu, alors une autre limite est fixée et l'élimination se fait moins bien ; ceci augmente avec l'âge.
Statistiques
modifierUn rein adulte reçoit normalement le quart du débit cardiaque à chaque minute. Son rein est irrigué en moyenne chaque jour par plus de 1 700 litres de sang[6] (toutes les quatre minutes, la totalité du sang de l'organisme, soit près de 6 litres, est filtrée en traversant cet organe), soit environ 900 litres de plasma sanguin. Sur ces 900 litres de plasma, 20 % sont filtrés au niveau des glomérules rénaux pour former 180 litres d'urine primitive qui subit par les différents segments du tubule rénal des modifications, essentiellement des phénomènes de réabsorption (plus de 99 % de l'eau et des sels filtrés sont réabsorbés), aboutissant à la production d'1 à 2 litres d'urines définitives. La diurèse quotidienne normale est de 1 à 1,5 L dépendant des apports hydriques[9].[pas clair]
Lors du sommeil, le taux d'ADH sécrété par l'hypophyse augmente, ce qui a pour effet d'augmenter la réabsorption d'eau par le rein, donc de diminuer la quantité d'urine excrétée.
Le débit de filtration glomérulaire normal est de 120 à 130 mL/min (un débit anormal sert à diagnostiquer l'insuffisance rénale chronique) soit les 180 litres d'urine primitive quotidienne[9].
Maladies
modifierL'insuffisance rénale chronique (IRC) semble en augmentation dans les pays riches, probablement secondairement à
- l'augmentation des cas de diabète (diabète sucré) ;
- l'augmentation des cas d'hypertension artérielle ;
- des néphropathies vasculaires liées au vieillissement de la population ;
- un régime trop riche en sel conduisant à une hypertension artérielle qui peut être fatale au rein ;
- l'alcoolisme ;
- l'obésité ;
- une exposition excessive à certains produits néphrotoxiques (toxiques rénaux) : plomb, cadmium en particulier ou médicaments tels que phénacétine ou ciclosporine… éventuellement exacerbée par des produits chélateurs très présents dans notre environnement tels que le glyphosate[10].
Elles peuvent être dues à des anomalies génétiques ou à une malformation survenue lors du développement (polykystose rénale le plus souvent, ou reflux vésico-urétéral chez l'enfant), des infections (fréquemment à la suite d'angines, d'infection urinaire, de tuberculose dans les pays en développement) ou à des intoxications ou séquelles d'intoxications. Certains cancers du rein pourraient être précocement induits par des perturbateurs endocriniens. La défaillance du rein peut apparaître brutalement 10 à 40 ans après le début de l'affection.
Malformation congénitale : l'exposition prénatale à l'alcool peut provoquer une diminution de la quantité de néphrons[11], des reins en fer à cheval[12].
On classe généralement les maladies rénales en :
- maladies glomérulaires (glomérulonéphrites primitives dont la cause initiale n'est pas comprise, ou maladies glomérulaires connues telles que le diabète sucré ou lupus érythémateux, ou couramment dans les pays pauvres les amyloses) ;
- néphropathies interstitielles (infection urinaire à pyélonéphrite, intoxication par des toxiques tels que cadmium ou plomb). Chez la femme, une cystite aggravée est la cause première. Chez l'homme, un cancer ou un grossissement de la prostate freinant l'écoulement de l'urine peut faciliter une infection conduisant à une néphropathie interstitielle ;
- néphropathies vasculaires ; le cas le plus fréquent étant une néphroangiosclérose liée à une hypertension artérielle (près de 10 % de la population dans les pays riches).
Traitements
modifierIntervention chirurgicale
modifierRein artificiel ou dialyse
modifierUn rein artificiel (ou générateur de dialyse) est un dispositif médical permettant d'épurer le sang des patients dont les reins ne fonctionnent plus.
Greffe de rein
modifier- La première réalisée en France eut lieu à Paris sur le jeune Marius Renard en 1952, par l'équipe du docteur Louis Michon à l'Hôpital Necker ; les suites néphrologiques ont été assurées par le professeur Jean Hamburger et Gabriel Richet, mais le jeune homme est rapidement décédé. La méthode aujourd'hui[Quand ?] utilisée est la méthode « de Kuss » (1913-2006).
- Le , le chirurgien américain Joseph Murray réalise la première transplantation rénale réussie au monde, en la pratiquant sur des jumeaux monozygotes, les frères Ronald et Richard Herrick (en) au Peter Bent Brigham Hospital (en)[14].
- Il se réalise environ 3 000 greffes de reins par an en France.
Autre
modifierLe bicarbonate de sodium s'avère efficace pour ralentir la progression de maladie rénale chronique - études ayant exclu les personnes souffrant d'obésité morbide associée, de troubles cognitifs, de septicémie chronique, d'insuffisance cardiaque manifeste ou d'hypertension non contrôlée[15],[16],[17].
Chez les autres animaux
modifierLe système excréteur chez les autres animaux est constitué d'organes excréteurs et des canaux excréteurs associés :
- organes excréteurs non spécialisés (élimination de différents types de solutés sous forme d'urine) : organes néphridiens chez les invertébrés, tubes de Malpighi chez les arthropodes, organe de Bojanus des mollusques, rein des vertébrés ;
- organes excréteurs spécialisés (élimination d'un type de soluté), par exemple les cellules à chlorures des branchies des téléostéens, les glandes à sel des oiseaux.
Galerie
modifierReins de plusieurs animaux obtenus par la technique d'injection de vinyle et corrosion :
-
Reins de porc.
-
Reins de cheval.
-
Reins de bœuf.
-
Reins de chien.
-
Reins de lion.
Notes et références
modifier- Ps 26,2, Ps 73,21 dans la Bible Segond, Ps 26:2 et Ps:73:21 dans la Bible du Rabbinat (traduction française littérale du Tanakh).
- Gilbert Deray, Les pouvoirs extraordinaires du rein, Fayard, , p. 21
- Kamina P. Anatomie clinique (Tome 4) organes urinaires et génitaux, pelvis, coupes du tronc. Éditions Maloine. 2008. (ISBN 978-2-224-03067-4)
- Franck Netter, Atlas d'anatomie humaine, Elsevier Masson, , 624 p. (ISBN 978-2-294-74124-1 et 2-294-74124-2), p. 323
- (en) Dorne J., Walton K. and Renwick A.G. (2004) « Human variability in the renal elimination of foreign compounds and renal excretion-related uncertainty factors for risk assessment » Food and Chemical Toxicology, 42, 2, 275-298.
- Michel Olmer, Vivre avec une maladie des reins, L.I.E.N., , p. 12
- « How does the urinary system work? »
- « Atlas of Anatomic Pathology with Imaging: A Correlative Diagnostic Companion - "The function of the human kidney is to convert over 1,700 L of renal blood flow per day into about 1 L of concentrated fluid" », Krueger et al.,
- Maurice Laville, Néphrologie et urologie, Elsevier Masson, , p. 23
- ayasumana C, Gunatilake S, Senanayake P (2014). Glyphosate, hard water and nephrotoxic metals: are they the culprits behind the epidemic of chronic kidney disease of unknown etiology in Sri Lanka? Int J Environ Res Public Health ;11:2125–47. doi:10.3390/ijerph110202125
- (en) Gray Stephen P, Denton Kate M, Cullen-McEwen Luise, Bertram John F et Moritz Karen M, « Prenatal exposure to alcohol reduces nephron number and raises blood pressure in progeny. », Journal of the American Society of Nephrology : JASN, vol. 21, no 11, , p. 1891-902 (PMID 20829403)
- Philippe Dehaene, La grossesse et l'alcool, Presses universitaires de France, , 127 p. (OCLC 32635508)
- « Sonde urinaire en « double J » | Ramsay Santé », sur ramsaygds.fr (consulté le )
- (en-US) « A transplant makes history », sur Harvard Gazette, (consulté le )
- Martina Gaggl, Daniel Cejka, Max Plischke et Georg Heinze, « Effect of oral sodium bicarbonate supplementation on progression of chronic kidney disease in patients with chronic metabolic acidosis: study protocol for a randomized controlled trial (SoBic-Study) », Trials, vol. 14, , p. 196 (ISSN 1745-6215, PMID 23826760, PMCID PMCPMC3729547, DOI 10.1186/1745-6215-14-196, lire en ligne, consulté le )
- Jiwon Jeong, Soon Kil Kwon et Hye-Young Kim, « Effect of Bicarbonate Supplementation on Renal Function and Nutritional Indices in Predialysis Advanced Chronic Kidney Disease », Electrolytes & Blood Pressure : E & BP, vol. 12, no 2, , p. 80–87 (ISSN 1738-5997, PMID 25606047, PMCID PMCPMC4297707, DOI 10.5049/EBP.2014.12.2.80, lire en ligne, consulté le )
- (en) Muhammad M. Yaqoob, Martin J. Raftery, Mira Varagunam et Ione de Brito-Ashurst, « Bicarbonate Supplementation Slows Progression of CKD and Improves Nutritional Status », Journal of the American Society of Nephrology, vol. 20, no 9, , p. 2075–2084 (ISSN 1046-6673 et 1533-3450, PMID 19608703, DOI 10.1681/ASN.2008111205, lire en ligne, consulté le )
Voir aussi
modifierArticles connexes
modifierLiens externes
modifier
- Ressources relatives à la santé :
- Notices dans des dictionnaires ou encyclopédies généralistes :
- Renaloo, communauté de patients et de proches concernés par l'insuffisance rénale, la dialyse, la greffe.