Pollen
Le pollen (du grec πάλη / palê, « farine, poussière ») constitue, chez les plantes à graines, l'élément mobile mâle produit par la fleur : ce sont des grains minuscules (20 à 55 μm de diamètre en général), de forme plus ou moins ovoïde, initialement contenus dans l'anthère à l'extrémité des étamines.
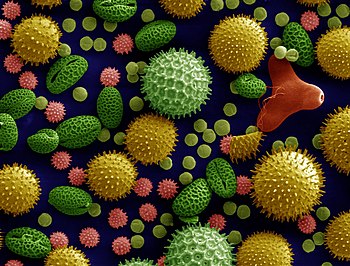
Le grain de pollen est le gamétophyte mâle, il produit et contient les gamètes mâles haploïdes (n)[1], et permet leur déplacement. On le considère parfois à tort comme un gamète. Le grain de pollen est homologue des gamétophytes chez d'autres groupes d'Embryophytes (par exemple du prothalle des fougères) et chez certaines algues. Il fait partie de la phase haploïde du cycle de vie des plantes à graines. Il constitue une génération gamétophytique au sens botanique du terme.
Chez certaines plantes à fleurs, la germination du grain de pollen commence souvent avant même qu'il ne quitte le microsporangium, avec la cellule générative formant les deux cellules « spermatiques ».
En zoologie, un animal est dit pollinivore, polliniphage, pollinophage ou palynophage, lorsqu'il se nourrit de pollen.
Historique
modifierLe pollen et son rôle fertilisateur est connu dès l'Antiquité comme en témoignent les gravures sur pierre du palais assyrien d'Assurbanipal représentant des personnages qui secouent des spathes mâles de dattiers pour recueillir le pollen et féconder artificiellement les spathes femelles[2]. Hérodote mentionne également cette pratique dans l'Égypte antique où la fécondation du dattier est assurée en introduisant des rameaux chargés d'étamines dans les spathes des fleurs femelles. Pline l'Ancien évoque dans son Histoire naturelle[3] le pollen comme un agent fertilisateur[4].
En 1665, Robert Hooke perfectionne le microscope optique et publie son traité Micrographia dans lequel il décrit différents organismes et structures biologiques microscopiques. Marcello Malpighi et Nehemiah Grew observent des grains de pollen avec ce microscope mais ne parviennent pas à déterminer leur rôle dans la reproduction sexuée des plantes. Joseph Gottlieb Kölreuter est le premier à réaliser de véritables expérimentations sur la pollinisation par des insectes qu'il publie entre 1761 et 1766, si bien que Linné impose en 1762 le terme de pollen dans son acception scientifique de « matière fécondante des végétaux » alors qu'il désignait jusque-là une poudre blanche très fine, une farine[5]. Les progrès en microscopie permettent à Christian Konrad Sprengel d'être le premier à décrire les pores et les sillons des grains de pollen dans son ouvrage Das endeckte Geheimnis im Bau und in der Befruchtung der Blumen (1793). Le botaniste Franz Andreas Bauer décrit les formes essentielles de pollen qui accompagnent l'illustration d'espèces botaniques. En 1833, Carl Julius Fritzsche invente les termes d'intine, exine et pollenine dans son ouvrage Dissertatio de plantarum polline. Hugo von Mohl réalise en 1834 le premier traité sur les pollens, avec une classification basée sur ces pores et sillons, classification encore utilisable[6]. Les paléontologues allemands Johann Heinrich Robert Göppert (1837) et Christian Gottfried Ehrenberg (1838) sont les premiers à décrire des grains de pollen fossiles[7]. Le XXe siècle voit l'essor de la palynologie avec les ouvrages majeurs de Roger Philip Wodehouse, Pollen grains[8] et de Gunnar Erdtman (en), Handbook of palynolgy[9], dont la science connaît un nouveau développement grâce à la mise au point du microscope électronique.
Formation et caractéristiques
modifierLe grain de pollen est le gamétophyte mâle. Il apparaît chez les préspermaphytes, qui ne libèrent donc pas de spores puisqu'elles restent sur le sporophyte.
Le pollen sert de nourriture aux butineurs, notamment les abeilles, dont il est la principale source de protéines, en particulier pour leurs larves. Il permet l'identification de l'origine du miel.
Structure et aspect du pollen
modifierLe grain de pollen mature est constitué habituellement :
- de deux ou trois cellules non cloisonnées. Il comporte deux noyaux haploïdes : le plus gros est le noyau végétatif, l'autre le noyau génératif ou reproducteur. La cellule végétative est constituée d'un noyau, d'organites, de petites vacuoles déshydratées et de réserves (amidon, gouttelettes lipidiques). Sa première fonction est d'assurer la survie du grain de pollen, sa seconde fonction de fabriquer le tube pollinique et sa troisième fonction de déclencher la production de l'albumen du futur fruit. La cellule reproductrice, quant à elle, est petite, excentrée et entourée par la cellule végétative. Le noyau est condensé et bloqué en prophase I de méiose. Sa fonction est de fusionner avec l'ovule pour former l'embryon de la future graine.
- d'une double enveloppe externe, sauf chez certaines plantes aquatiques submergées, avec :
- une couche externe très résistante, l'exine qui constitue l'exospore. Elle est constituée de sporopollenine. Cette couche comporte des apertures (points de moindre résistance, qui permettront l'émission du tube pollinique qui fécondera l'ovule. L'exine, fortement cuticularisée résiste à la plupart des dégradations chimiques et biologiques, permettant au pollen d'être diffusé dans l'environnement sans être trop abîmés même si certains pollens meurent néanmoins rapidement. L'ectexine est plus alvéolaire que les autres couches et peut être lisse (dissémination par le vent) ou ornementée (pour accrocher aux poils animaux, aux pattes des insectes, etc.)
Les ornements de l'exine, en forme d'épines, de creux, de « verrues », de crochets ou de motifs propres à chaque espèce permettent souvent l'identification des genres, espèces, ou même de cultivars ou individus. La palynologie est l'étude des grains de pollen permettant d'identifier les plantes qui les ont produits, parfois même des millions d'années après leur production. - La couche interne qui forme l'endospore. Elle est mince et fragile, constituée de cellulose non modifiée et éventuellement d'autres polysaccharides. Elle est appelée l'intine.
- une couche externe très résistante, l'exine qui constitue l'exospore. Elle est constituée de sporopollenine. Cette couche comporte des apertures (points de moindre résistance, qui permettront l'émission du tube pollinique qui fécondera l'ovule. L'exine, fortement cuticularisée résiste à la plupart des dégradations chimiques et biologiques, permettant au pollen d'être diffusé dans l'environnement sans être trop abîmés même si certains pollens meurent néanmoins rapidement. L'ectexine est plus alvéolaire que les autres couches et peut être lisse (dissémination par le vent) ou ornementée (pour accrocher aux poils animaux, aux pattes des insectes, etc.)
- la couche externe peut contenir une pellicule collante d'origine lipidique, qui aurait pour rôle de protéger le grain de pollen de la déshydratation, servir de réserve lors de la réhydratation du pollen et participer à l'activation de la stigmatisation en tant que médiateur lipidique[10].
Le pollen peut se composer d'un grain isolé (monade inaperturé, poré, colpé ou colporé) ou de grains multiples (dyade, tetrade, polyade)[11].
Taille
modifierConcernant la taille, on considère que les pollens les plus petits sont ceux du myosotis (7 µm) et les plus gros, ceux de la courge (150 µm). Les pollens de moins de 10 µm sont réputés plus souvent allergènes : bouleau, aulne, charme, noisetier, châtaignier, chêne, cyprès, frêne, olivier, peuplier, platane, etc.
Composition chimique et biochimique
modifierL'apiculture fait appel à la mélissopalynologie qui est la science du miel et du pollen.
Selon l'origine florale, les conditions climatiques, les caractéristiques du sol où poussent les plantes et la saison, la composition du pollen peut varier. Il comporte :
- 15 à 75 % de glucides (essentiellement glucose et fructose + saccharose « formé » en moindre proportion) ;
- 2,5 à 61 % de protéines[12] ;
- 1 à 20 % de lipides dont une partie d'acides gras essentiels[13] aux propriétés antimicrobiennes et antifongiques ;
- 18 % d'eau ;
- 5 % de minéraux : calcium, chlore, cuivre, fer, magnésium, manganèse, phosphore, potassium, silicium, soufre, sélénium ;
- des vitamines du groupe B en grande quantité ;
- des acides aminés : arginine, histidine, leucine, isoleucine, lysine, méthionine, phénylalanine, thréonine, tryptophane, valine ;
- des vitamines A, C, D, E en quantité plus faible.
Du pollen est toujours présent, en petite quantité, dans le miel, ce qui permet d'identifier ses origines botaniques.
Pollen vecteur d'une partie du microbiome de la plante
modifierToutes les plantes ont un microbiote (microbiote des plantes), généralement en partie endophytique. On pense maintenant que le pollen (riche en substance nutritive) est aussi un vecteur utilisé par la plante pour transporter une partie de son microbiote, via les pollinisateurs et le vent[14].
On a récemment (2016) montré que le type de pollinisation (de même que la pollution, qui peut ainsi rendre le pollen plus allergène) module le degré de diversité biologique du microbiote retrouvé sur le pollen, diversité susceptible de jouer un rôle dans l'évolution adaptative de l'endosphère[14]. Le recul des pollinisateurs et la pollution seraient donc deux enjeux encore mal évalués de ce point de vue. Il apparait que les espèces pollinisées par les insectes ont un microbiote moins diversifié que celles qui sont anémophiles (« ce qui suggère un effet de nivellement par les insectes vecteurs[14] ; La microscopie électronique à balayage ainsi que l'hybridation fluorescente in situ couplée à la microscopie confocale à balayage laser (FISH ‐ CLSM) ont indiqué que la surface du tectum constituait la niche préférée de la colonisation bactérienne »[14].
Viabilité
modifierAvant l'anthèse, la majorité des grains de pollen sont viables, c'est-à-dire qu'ils conservent leur aptitude à germer.
La déhiscence des anthères induit une perte qui peut atteindre plus de 25 % de la viabilité qui est affectée par les stress environnementaux (sécheresse, température, et depuis quelques décennies pollution de l'air [acidification, ozone...]…). Après cette déhiscence, les grains de pollen restent viables en moyenne de 2 à 5 jours en fonction des espèces et des conditions environnementales (soit à peu près la même période au cours de laquelle le stigmate reste réceptif)[15].
Pollen dégradé par la pollution de l'air
modifierSelon une étude récente (2017), plusieurs polluants communs de nos villes, notamment gazeux (O3 et NO2) - même à des niveaux inférieurs aux seuils réglementés de pollution de l'air[16] - peuvent négativement affecter la viabilité du pollen aérotransporté (« lors de son voyage dans l'air, la paroi pollinique subit donc des modifications de ses composants induites par la pollution atmosphérique, ce qui peut compromettre la fonction pollinique »[16].
À titre d'exemple, l'étude (2015) in vitro et in vivo de pollen de tomate (Lycopersicon esculentum Mill. Cv. Triton) a conclu que l'exposition de la fleur ou du pollen à un taux d'ozone (O3) tel que fréquemment observé les jours de pollution par l'ozone troposphérique, diminue considérablement la capacité de germination du pollen, la croissance du tube germinatif et les interactions pollen-stigmatisation.
Le pollen n'est d'ailleurs pas seul en cause. En effet, du pollen provenant de plantes élevé dans une enceinte à l'atmosphère filtrée au charbon activé - a aussi présenté un moindre développement de tube germinatif quand il était mis au contact du stigmates des plantes exposées à des niveaux environnementaux de pollution à l'ozone.
L'effet est — dans tous les cas — un moindre nombre d'ovules viables (qu'ils aient été fécondés ou non) et une mortalité accrue de fruits immatures.
Cette délétion par l'ozone de la fécondabilité est observée quel soit le moment de l'exposition, et dès lors que la plante émettrice ou réceptrice du pollen a été exposée à un taux de pollution par l'ozone tel qu'on en observe couramment en ville, suggérant que l'ozone dégrade à la fois la viabilité du pollen ou le développement des ovules (le futur fruit). En outre, les grappes de fruits issus de plantes exposés à 100 nmol mol−1 d'ozone O3 (10 hd−1) à partir de la floraison ont aussi présenté un moindre poids moyen des tomates et une baisse du nombre de graines, de la teneur en amidon et en acide ascorbique (vitamine C) des fruits ; paramètres qui font évoquer une maturation anormalement accélérée. L'ozone affecte donc tout le processus de reproduction de la plante. Ces résultats ont attiré l’attention des auteurs sur l'importance de mieux comprendre les effets globaux de l'ozone et potentiellement d’autres polluants gazeux, sur la biologie de la reproduction dans l'évaluation des risques induits par la pollution de l'air[17].
Pollinisation
modifierPour germer, le grain de pollen doit atterrir sur le pistil d'une fleur (femelle) de la même espèce.
- Le transport du pollen
- il se fait généralement par un vecteur comme le vent ou les insectes : c'est la pollinisation. La plante peut aussi le disséminer (disperser) elle-même.
Les plantes dont le pollen est disséminé par le vent en produisent de plus grandes quantités. Les plantes pollinisées par des animaux en produisent moins, mais le pollen a plus de chance de se retrouver sur le pistil d'une autre fleur de la même espèce. Pour que la fécondation soit possible, il faut en outre que les étamines soient mûres, ainsi que le pistil.
- La germination du grain de pollen chez les angiospermes
- Le pollen doit être retenu par le stigmate. Pour cela, il existe de petites forces électrostatiques qui retiennent le grain où il y a des substances gluantes (sucres). Il y a également des liaisons spécifiques entre les molécules du grain de pollen et le récepteur au niveau du stigmate.
Le grain de pollen est hydraté par de l'humidité provenant du pistil. Ensuite il forme un tube pollinique : pour cela au niveau des pores du pollen l'endexine s'amincit et lors de la turgescence, le pore du grain de pollen sera percé. La cellule du tube pollinique passe alors entre les deux cellules du stigmate et du style qui présentent des particularités (cellules plutôt lâches, parois cellulosiques non lignifiées, lamelle moyenne plutôt hydratée avec pectine liquéfiée, apparition d'espaces pour le passage du tube pollinique).
La germination peut être inhibée par des mécanismes d'auto-incompatibilité. Il existe différents types d'incompatibilités polliniques : interspécifique, hétéromorphe, homomorphe (gamétophytique ou sporophytique). Certains polluants chimiques peuvent aussi perturber ou inhiber la germination.
La fécondation se fait dans le cas contraire, le tube arrivant jusqu'à l'oosphère. Sur les deux gamètes mâles, chacun étant haploïde (n) :
- l'un des gamètes mâles fécondera l'oosphère également haploïde (n), formant alors un zygote diploïde (2n) [1];
- l'autre gamète mâle fécondera la cellule centrale du gamétophyte femelle qui contient deux noyaux polaires, chacun haploïde (n). Il en résultera la formation d'une cellule triploïde (3n) à l'origine de l'albumen, tissu riche en amidon et autres réserves nutritives essentielles pour le développement de l'embryon[1].
Ce phénomène est caractéristique des angiospermes et s'appelle la « double fécondation »[1].
- Différents types de pollens
-
Pollen de tournesol.
-
Pollen de ricin commun.
-
Oenothera fruticosa
-
Ipomoea purpurea
Allergies
modifierUne certaine présence de grains de pollens dans l'atmosphère que nous respirons est normale (puisqu'une partie importante de la fécondation des plantes se fait grâce au vent (anémogamie). Elle est naturellement plus importante au printemps et en été en zone tempérée, et toute l'année en zone tropicale. Plusieurs dizaines d'épidémies d'asthme de tempêtes ont été décrites dans le monde en 20 ans, encore mal compris, et donc à ce jour impossible à prévoir car toutes les tempêtes n'ont pas cet effet[18].
Chez un nombre croissant de personnes sensibilisées certains pollens déclenchent des allergies (dites pollinoses prenant la forme de rhinites, d'asthmes ou de conjonctivites) avec d'éventuelles allergies croisées[19]. Ce phénomène semble récent ; il est décrit en Angleterre par Bostock (1819) au début de l'ère industrielle peu avant que les premières descriptions de rhinites allergiques soient faites (en 1830 dans la Ruhr puis en Nouvelle-Angleterre, alors qu'en France, aucun cas de rhume des foins n'a été décrit par la littérature médicale ou scientifique avant 1860[19]. Depuis les années 1990 on constate que ces rhinites, qui se sont répandues dans le monde entier, apparaissent concomitamment (dans l'espace et dans le temps[20]) à l'apparition de la pollution chimique et particulaire massive de l'atmosphère, principalement liée au charbon puis au pétrole et à la chimie industrielle, laissant penser qu'il existe un lien entre pollution de l'air et caractère allergène du pollen[21],[22],[23],[24],[25],[26],[27],[28] ; soit qu'on y soit plus sensible, soit qu'il soit plus allergène (comme pour le pollen de cyprès[29]), soit les deux à la fois.
En France vers 2005-2010, la prévalence de la rhinite allergique sans identification d'allergène responsable, était de 31 % (26 % dans le Sud-Ouest et jusqu'à 37 % en zone Méditerranéenne et dans le Nord). Les 18-25 ans sont les plus touchés (39 %) et seuls 22 % des plus de 65 ans sont concernés[30]. Les femmes y sont plus vulnérables (36 % contre 25 %chez les hommes)[30] Cette prévalence a triplé en 25 ans[31],[32].
Depuis la fin du XIXe siècle les pollinoses semblent progresser au même rythme que la pollution globale de l'air et là où cette pollution apparaît ou augmente, notamment en ville ; Ceci fait évoquer d'autres facteurs que la seule présence du pollen, dont la pollution de l'air[33].
De plus, depuis les années 1970 on observe une raréfaction (ou quasi-disparition, localement) des pollinisateurs (abeilles et apidés sauvages et papillons en particulier) et avec le réchauffement les pollens peuvent être produit plus tôt et plus tard dans l'année. Et d'autres pollens, exotiques et parfois allergènes sont présents dans l'air.
Éléments d'explication : dans un contexte artificiel les pollens sont moins rapidement fixés au sol, moins emportés par le ruissellement ou moins absorbés par les mousses ou lichens que dans la nature. Ils se dégradent sous l'action de la pollution acido-particulaire, de l'ozone troposphérique (superoxydant) et d'autres polluants, ou pour des raisons mécaniques (dépôts sur les chaussées et trottoirs)[34]. Des fragments plus petits (<2,5 μm, dans la gamme des particules fines dites PM2.5 qui pénètrent plus profondément les poumons et réputées plus allergènes) sont alors formés et disponibles pour l'inhalation[34] (dont fragments de cuticules de pollen, molécules internes du pollen[35]) plus allergènes et pouvant le devenir plus encore en se combinant avec des polluants automobiles[36] ; et « les polluants atmosphériques peuvent augmenter la quantité d'allergènes présents dans les grains de pollen et leur capacité à se libérer dans l'air, ainsi que l'ont montré différentes expériences, et par suite majorer leur allergénicité »[37]. On trouve par exemple dans l'air des grains d'amidon, allergènes connu et associés à des épidémies d'« asthme d'orage » lors de la saison pollinique de diverses herbacées[19],[38].
« Les polluants atmosphériques agissent sur le pollen »[37] et certains polluants atmosphériques « favorisent la réaction allergique »[37] ; Des études ont montré in vitro que des allergènes intrapolliniques (ex « Lol p I », allergène majeur issu du pollen de nombreuses herbacées) se combinent (dans notre environnement peut-être dans les microgouttelettes d'eau de la brume, dans la pluie et dans les aérosols) à d'autres particules fines allergènes, également massivement présentes lors d'épisodes de pollution de l'air urbain, en particulier les particules fines de carbone émises par les moteurs Diesel sous forme de nanosphères de carbone de 30 à 60 nanomètres (nm) de diamètre se groupant spontanément en agrégats fractaux d'environ 1 à 2 micromètres (µm) de diamètre[34]. C'est un des mécanismes possibles de concentration d'allergènes en suspension dans l'air, pouvant déclencher des crises d'asthme[34]. Les « particules diesel » stimulent la synthèse des IgE et des cytokines impliquées dans l'allergie et le dioxyde de soufre et le monoxyde de carbone, et surtout l'ozone et le dioxyde d'azote, cette fois directement en tant qu'irritant respiratoires pourraient aussi fragiliser les muqueuses et préparer ou renforcer l'inflammation allergique[19]. La hausse du taux de CO2 de l'air (par rapport au taux pré-industriel) semble en outre doper la production de pollen (ex : + 130 % chez l'ambroisie (particulièrement allergène en France)[39]. A noter que certains polluants ont un effet inverse, semblant diminuer l'effet d'allergènes potentiels, dont le pollen.
En 2010 des chercheurs ont comparé le protéome du pollen de deux groupes de bouleaux (ruraux et urbains), toute en évaluant leur allergénicité (par mesure de leur puissance chimiotactique, testée sur des neutrophiles humains, et leurs teneurs en protéines et en allergènes. Vingt-six différences protéiques ont été relevées entre le pollen urbain et rural du bouleau. L'une des protéines qui différaient est "la protéine 14-3-3" qui ressemble à un facteur induit par le stress chez d'autres espèces végétales. Les extraits de pollen urbain avaient une activité chimiotactique plus élevée sur les neutrophiles humains que les extraits de pollens provenant de sites ruraux, confirmant un impact de la pollution de l'air sur le protéome porteur d'allergènes et sur la libération de substances chimiotactiques. L'augmentation des substances pro-inflammatoires telles que les médiateurs lipidiques associés au pollen pourrait contribuer au gradient urbain-rural décrit de la prévalence des allergies. De plus, notre étude suggère que l'allergénicité est déterminée par plus que la seule teneur en allergène[40].
En 2016, des chercheurs ont comparé les types de population microbiennes colonisant le pollen allergénique de zones plus ou moins polluées. Ils ont montré que le microbiome associé au pollen est corrélé aux paramètres de pollution et à l'allergénicité du pollen[41] (des protéines allergéniques et des composés non allergènes du pollen participent à la défense des plantes contre les stress environnementaux et microbiens. L'ADN des communautés de bactéries et micro-champignons colonisant le pollen de la fléole des prés (Phleum pratense) et de bouleaux (Betula pendula) a été analysé, montrant que la biodiversité[42] microbienne de ces pollens était en partie significativement corrélée aux paramètres d'allergénicité du pollen [43]. De plus pour le bouleau, la diversité microbienne des échantillons de pollen était corrélée à la pollution de l'air mesurée in situ pour le dioxyde d'azote (NO2) et moindrement pour l'ammoniac (NH3) et l'ozone troposphérique (O3) ;
Altération de l'allergénicité du pollen due au stress environnemental et microbien.
Le mode de vie intervient aussi : si l'atopie est indéniablement plus importante en milieu urbain (ou pollué[44]), on a montré en Allemagne que le rhume des foins et l'asthme étaient deux fois plus fréquent en ex-Allemagne de l'Ouest que chez les anciens habitants de l'ex-RDA, peut-être plus exposés à la stimulation microbienne dans la petite enfance[44] (ou moins exposé à la circulation automobile ?).
Une taille drastique pendant ou après floraison peut aussi facilite la dispersion des pollens et l'exposition des citadins[45], de même que l'utilisation par temps sec de « canons à air » portables pour le nettoyage des trottoirs.
En France, en 2014 sur la base des conclusions du Groupe de travail « Pollens » du Comité d'experts spécialisé « Evaluation des risques liés aux milieux aériens » l'Anses a recommandé de mieux évaluer l'importance globale du phénomène des pollens rendus plus allergènes par la pollution (en conditions réelles)[46] ; et recommandant d'améliorer la connaissance sur :
- les effets des polluants de l'air (ozone, dioxyde d'azote et nano- et microparticules notamment) sur les plantes et les pollens ; la Recherche s'est longtemps concentré sur les protéines du pollen, mais elles ne sont pas l'unique agent actif du pollen, lequel contient aussi des lipides jouant un rôle majeur dans sa reproduction (médiateurs lipidiques bioactifs). Ces lipides peuvent aussi adsorber des polluants liposolubles et rendre un pollen allergène ou le rendre plus allergènes. On les appelle « médiateurs lipidiques » (ou PALM pour pollen-associated lipid mediators)[47]. Ces PALMs, qui naturellement présents les substances adhésives et médiatrices présentes sur la couche externe du pollen sont aussi des chémo-attracteurs depuis les années 2000 soupçonnés de jouer un rôle dans l'inflammation allergique[48],[49].
En cherchant à mieux comprendre l'action de ces PALMs dans la phase effectrice immédiate des réactions allergiques, on a récemment (2019) identifié une nouvelle (à ce jour inconnue) pour la reconnaissance des glycolipides dérivés du pollen par des cellules immunitaires particulières du groupe des lymphocytes NKT (natural killer T), dites « cellules NKT de type 1 » ou (iNKT our invariants NKT)[47] ; on connait quelques cas où le lipide d'un pollen est allergène en tant que tel[50]. Parfois le lipide en cause provient en réalité de microbes ayant colonisé le pollen[51], ou ce lipide est devenu allergène en absorbant un ou plusieurs allergènes lipophiles[48],[52].
- la co-exposition des personnes allergique aux pollens et à la pollution de l'air ;
- « les facteurs climatiques influençant la quantité de grains de pollen produits et émis ainsi que la production d'allergènes dans le pollen (cinétique, quantité, température, stress, hygrométrie...) et les éventuels liens avec le changement climatique ».
L'institut Pasteur cultive des fleurs aux pollens allergéniques, pour désensibiliser les personnes allergiques et en 2013, le nouveau programme de l'ANSES inclut un programme sur la santé des abeilles, les médicaments vétérinaires, les « risques cumulés des mélanges de pesticides » et les interactions possibles entre pollens et polluants de l'air[53].
Mesure des taux de pollens dans l'air
modifierLes palynologues et les réseaux d'alertes et de mesure de la pollution de l'air ou les organismes mesurant les taux de pollens dans l'air bénéficient des mesures permises par des capteurs de pollens, dont les échantillons sont périodiquement analysés. Un indice pollinique peut être produit et mis à jour et utilisé pour la veille et la prévention concernant le risque d'allergie aux pollens.
- Capteur et indice polliniques
-
Détail.
-
Indice pollinique.
Palynologie
modifierLa palynologie est l'étude scientifique des pollens. Il est possible d'identifier une espèce végétale par l'observation de son pollen. Les caractères observés sont la taille (de 2,5 à 200 micromètres), la forme générale et l'aspect de l'exine : la stratification, les sculptures et granulations de la surface, le nombre, la forme et la disposition des apertures.
Les applications de la palynologie sont nombreuses :
- la palynologie apporte des éléments utiles dans les études de systématique végétale ;
- la paléopalynologie est l'étude des pollens fossiles : elle permet de donner des informations sur le climat et la végétation au cours de l'ère quaternaire ;
- l'aéropalynologie, qui consiste à analyser la présence dans l'air de différents types de pollens, a des applications en médecine (pathologies allergiques) et en agronomie (pollinisation) ;
- la mélissopalynologie est l'étude des pollens présents dans le miel, ce qui permet de détecter les mélanges et les fraudes.
Pollen, source de nourriture
modifierLa plupart des grandes classes de prédateurs et d'arthropodes parasites contiennent des espèces qui se nourrissent de pollen, en dépit de la perception commune que les abeilles sont le principal groupe d'arthropodes consommant du pollen. Beaucoup d'autres hyménoptères adultes autres que les abeilles consomment du pollen, mais seulement une petite partie se nourrit de pollen à l'état de larves.
Les araignées sont normalement considérées comme des carnivores mais le pollen est une importante source de nourriture pour plusieurs espèces, en particulier pour les jeunes araignées, qui attrapent le pollen sur leurs toiles.
Certains acariens prédateurs se nourrissent aussi de pollen, certaines espèces étant en mesure de subsister uniquement avec du pollen, comme Euseius tularensis, qui se nourrit du pollen de dizaines d'espèces de plantes.
Les membres de certaines familles de coléoptères tels que Mordellidae et Melyridae se nourrissent presque exclusivement de pollen, tandis que certaines espèces au sein des familles plus grandes telles que les Curculionidae, Chrysomelidae, Cerambycidae et Scarabaeidae sont des spécialistes de pollen, même si la plupart des membres de leurs familles ne le sont pas (par exemple, seulement 36 de 40 000 espèces de carabes, qui sont généralement prédateurs, mangent du pollen, mais il pourrait s'agir d'une sous-estimation importante car les habitudes alimentaires ne sont connues que pour 1 000 espèces).
De même, les coccinelles se nourrissent principalement d'insectes, mais de nombreuses espèces mangent aussi des pollens, soit pour partie soit pour la totalité de leur régime alimentaire.
Les Hemiptera sont essentiellement herbivores ou omnivores, mais on sait que certaines espèces se nourrissent de pollen (cela a seulement été bien étudié chez les Anthocoridae).
Beaucoup de mouches adultes, en particulier les Syrphidae, se nourrissent de pollen, et trois espèces britanniques de syrphes se nourrissent exclusivement du pollen (les syrphes, comme toutes les mouches, ne peuvent pas manger le pollen directement en raison de la structure de leurs pièces buccales, mais peuvent consommer le contenu de pollen dissous dans un fluide).
Certaines espèces de champignons, telles que l'amadouvier, sont capables de briser les grains de pollen en tant que source d'alimentation secondaire particulièrement riche en azote.
Certaines espèces de papillons Heliconius adultes consomment du pollen, ce qui semble être une source de précieux éléments nutritifs, et ces espèces sont plus désagréables pour les prédateurs que celles ne consommant pas de pollen.
Bien que les chauves-souris, les papillons et les colibris ne consomment pas de pollen en soi, leur consommation de nectar dans les fleurs est un aspect important du processus de pollinisation.
Chez l'homme
modifierCertains producteurs ont commencé à vendre du pollen récolté par les abeilles pour la consommation humaine, souvent commercialisé comme nourriture (plutôt qu'en complément alimentaire).
Les constituants les plus importants sont des hydrates de carbone et des protéines en fonction de l'espèce végétale recueillie par les abeilles. Le miel produit par les abeilles à partir de sources naturelles contient de l'acide paracoumarique, un dérivé antioxydant du pollen.
La Food and Drug Administration américaine (FDA) n'a pas révélé d'effets nocifs de la consommation de pollen d'abeille, à l'exception des allergies habituelles. Toutefois, la FDA ne permet pas de faire des allégations de santé sur ces produits car aucune base scientifique n'a jamais été prouvée. En outre, il y a des dangers possibles non seulement de réactions allergiques mais aussi de contaminations par des pesticides, des champignons ou des bactéries si les procédures de stockage ne sont pas correctes.
Notes et références
modifier- Reece, Jane B., 1944- et Campbell, Neil A., 1946-, Campbell biologie, ERPI, (ISBN 978-2-7613-2856-2, 2-7613-2856-6 et 978-2-7613-5065-5, OCLC 795117676, lire en ligne)
- (en) Mariana Giovino, The Assyrian Sacred Tree. A History of Interpretations, Saint-Paul, , p. 68
- Pline, Histoire naturelle, 13, 34-35
- (en) Gavin Hardy et Laurence Totelin, Ancient Botany, Routledge, , p. 131
- (en) Michael C. F. Proctor, Peter Yeo, Andrew Lack, The natural history of pollination, Timber Press, , p. 17
- (en) Tod F. Stuessy, Plant Taxonomy. The Systematic Evaluation of Comparative Data=, Columbia University Press, , p. 224
- (en) Michael Hesse, Heidemarie Halbritter, Martina Weber, Ralf Buchner, Andrea Frosch-Radivo, Silvia Ulrich, Reinhard Zetter, Pollen Terminology, Springer Science & Business Media, , p. 18
- (en) Roger Philip Wodehouse, Pollen grains : their structure, identification, and significance in science and medicine, McGraw-Hill, , 574 p.
- (en) Gunnar Erdtman, Handbook of palynolgy. Morphology, taxonomy, ecology. An introduction to the study of pollen grains and spores, Hafner, , 574 p.
- (en) Ettore Pacini et Michael Hesse, « Pollenkitt – its composition, forms and functions », Flora - Morphology, Distribution, Functional Ecology of Plants, vol. 200, no 5, , p. 399–415 (DOI 10.1016/j.flora.2005.02.006, lire en ligne, consulté le )
- Voir clé de détermination des pollens.
- Roulston et al, 2000
- Manning, 2001
- Ambika Manirajan B, Ratering S, Rusch V, Schwiertz A, Geissler-Plaum R, Cardinale M, Schnell S (2016) Bacterial microbiota associated with flower pollen is influenced by pollination type, and shows a high degree of diversity and species-specificity. Environ Microbiol 18:5161–5174. doi: 10.1111/1462-2920.13524
- (en) A. Dafni & D. Firmage, « Pollen viability and longevity: practical, ecological and evolutionary implications », Plant Systematics And Evolution, vol. 222, nos 1-4, , p. 113-132.
- (en) Helena Ribeiro, Célia Costa, Ilda Abreu et Joaquim C.G. Esteves da Silva, « Effect of O3 and NO2 atmospheric pollutants on Platanus x acerifolia pollen: Immunochemical and spectroscopic analysis », Science of The Total Environment, vol. 599-600, , p. 291–297 (DOI 10.1016/j.scitotenv.2017.04.206, lire en ligne, consulté le )
- (en) Colin Gillespie, Daniel Stabler, Eva Tallentire et Eleni Goumenaki, « Exposure to environmentally-relevant levels of ozone negatively influence pollen and fruit development », Environmental Pollution, vol. 206, , p. 494–501 (DOI 10.1016/j.envpol.2015.08.003, lire en ligne, consulté le )
- Caillaud, D., Merle, P., Marson, H., & Jeannin, A. (2005). Tempête et asthme. Revue française d'allergologie et d'immunologie clinique, 45(1), 29-32 (résumé).
- Mohamed LAAIDI, Karine LAAIDI, Jean-Pierre BESANCENOT, Synergie entre pollens et polluants chimiques de l'air : les risques croisés ; Environnement, Risques & Santé. Volume 1, Numéro 1, 42-9, Mars - Avril 2002, Synthèses
- (en) Zetterström O (1988) The increased prevalence of allergic airway disease. Allergy ; 43 : 10-1
- Peltre G (1998) Interrelation entre les pollens allergisants et la pollution de l'air. Allerg Immunol ; 30 : 324-6
- M. Laaidi, T. Chinet et P. Aegerter, « Allergies au pollen, pollution et climat : revue de la littérature », Revue Française d'Allergologie, vol. 51, no 7, , p. 622–628 (DOI 10.1016/j.reval.2011.05.004, lire en ligne, consulté le )
- M.C. Kopferschmitt-Kubler et G. Pauli, « Pollens et pollution », Revue Française d'Allergologie et d'Immunologie Clinique, vol. 39, no 4, , p. 283–288 (DOI 10.1016/S0335-7457(99)80054-9, lire en ligne, consulté le )
- Claude Molina, « Qualité de l'air et allergie », Revue Française des Laboratoires, vol. 2003, no 349, , p. 35–42 (DOI 10.1016/S0338-9898(03)80467-5, lire en ligne, consulté le )
- (en) Hélène Sénéchal, Nicolas Visez, Denis Charpin et Youcef Shahali, « A Review of the Effects of Major Atmospheric Pollutants on Pollen Grains, Pollen Content, and Allergenicity », The Scientific World Journal, vol. 2015, , p. 1–29 (ISSN 2356-6140 et 1537-744X, PMID 26819967, PMCID PMC4706970, DOI 10.1155/2015/940243, lire en ligne, consulté le )
- Y. Shahali, P. Poncet et H. Sénéchal, « Pollinose aux Cupressacées et pollution atmosphérique », Revue Française d'Allergologie, vol. 53, no 5, , p. 468–472 (DOI 10.1016/j.reval.2013.01.050, lire en ligne, consulté le )
- M. Choël et N. Visez, « Altérations du grain de pollen par la pollution atmosphérique », Revue Française d'Allergologie, vol. 59, no 8, , p. 555–562 (DOI 10.1016/j.reval.2019.10.003, lire en ligne, consulté le )
- (en) Kathrin Reinmuth-Selzle, Christopher J. Kampf, Kurt Lucas et Naama Lang-Yona, « Air Pollution and Climate Change Effects on Allergies in the Anthropocene: Abundance, Interaction, and Modification of Allergens and Adjuvants », Environmental Science & Technology, vol. 51, no 8, , p. 4119–4141 (ISSN 0013-936X et 1520-5851, PMID 28326768, PMCID PMC5453620, DOI 10.1021/acs.est.6b04908, lire en ligne, consulté le )
- Shahali Y, Pourpak Z, Moin M, Zare A, Majd A. Impacts of air pollution exposure on the allergenic properties of Arizona cypress pollens. J Phys 2009 ; 151 : 1-9.
- Klossek JM, Annesi-Maesano I, Pribil C, Didier A. Un tiers des adultes ont une rhinite allergique en France (enquête INSTANT). Presse Med 2009 ; 38 : 1220-9
- Emanuel MB. Hay fever, a post industrial revolution epidemic : a history of its growth during the 19th century. Clin Allergy 1988 ; 18 : 295-304.
- Guillam MT, Ségala C. (2008) Pollens et effets sanitaires : synthèse des études épidémiologiques. Rev Fr Allergol Immunol Clin 2008 ; 48 : 14-9
- Kopferschmitt-Kubler MC, Pauli G. Pollens et pollution. Rev Fr Allergol Immunol Clin 1999 ; 39 : 283-8
- Knox, R. B., Suphioglu, C., Taylor, P., Desai, R., Watson, H. C., Peng, J. L. and Bursill, L. A. (1997), Major grass pollen allergen Lol p 1 binds to diesel exhaust particles : implications for asthma and air pollution. Clinical & Experimental Allergy, 27: 246–251. doi: 10.1111/j.1365-2222.1997.tb00702.x
- Bieberdorf FW, Gross AL, Weichlein R. Free amino acids content of pollen. Ann Allergy 1961 ; 19 : 869-76.
- Ruffin J, Liu MYG, Sessoms R, Banerjee S, Banerjee UC. Effects of certain atmospheric pollutants (SO2, NO2 and CO) on the soluble amino acids, molecular weight and antigenicity of some airborne pollen grains. Cytobios 1986 ; 46 : 119-29.
- Laaidi, M., Chinet, T., & Aegerter, P. (2011). Allergies au pollen, pollution et climat: revue de la littérature. | Revue Française d'Allergologie| 51(7), 622-628| résumé
- (en) Rossi OVJ, Kinnula VL, Tienari J, Huhti E. Association of severe asthma attacks with weather, pollen, and air pollutants. Thorax 1993 ; 48 : 244-8.
- Ziska LH & Caulfield FA (2000) Rising CO2 and pollen production of common ragweed (Ambrosia artemisiifolia), a known allergy-inducing species: implications for public health. Austr J Plant Physiol ; 27 : 893-8
- Bryce, M., Drews, O., Schenk, M. F., Menzel, A., Estrella, N., Weichenmeier, I., ... & Behrendt, H. (2010). Impact of urbanization on the proteome of birch pollen and its chemotactic activity on human granulocytes. International Archives of Allergy and Immunology, 151(1), 46-55. | résumé
- Obersteiner, A., Gilles, S., Frank, U., Beck, I., Häring, F., Ernst, D., ... & Schmid, M. (2016). Pollen-associated microbiome correlates with pollution parameters and the allergenicity of pollen. PLoS One, 11(2), e0149545.
- ici mesurée par l'indice de Shannon et l'indice de Simpson
- Allergénicité ici évalués par dosage des médiateurs lipidiques Bet v 1 et Phl 5
- D. Charpin, « Pollution atmosphérique et atopie Air pollution and atopy », Revue Française d'Allergologie et d'Immunologie Clinique, vol. 36, no 3, , p.327-335 (DOI doi:10.1016/S0335-7457(96)80103-1).
- Cariñanos P, Casares-Porcel M, Quesada-Rubio JM (2014). Estimating the allergenic pot ential of urban green spaces: a case-study in Granada, Spain. Landsc Urban Plan ; 123 : 134-44.
- Anses (2014) État des connaissances sur l'impact sanitaire lié à l'exposition de la population générale aux pollens présents dans l'air ambiant ; Janvier, voir notamment p6/11
- Nestor González Roldán, Regina Engel, Sylvia Düpow et Katharina Jakob, « Lipid Mediators From Timothy Grass Pollen Contribute to the Effector Phase of Allergy and Prime Dendritic Cells for Glycolipid Presentation », Frontiers in Immunology, vol. 10, , p. 974 (ISSN 1664-3224, PMID 31134071, PMCID PMC6514527, DOI 10.3389/fimmu.2019.00974, lire en ligne, consulté le ).
- (en) Merima Bublin, Thomas Eiwegger et Heimo Breiteneder, « Do lipids influence the allergic sensitization process? », Journal of Allergy and Clinical Immunology, vol. 134, no 3, , p. 521–529 (PMID 24880633, PMCID PMC4151997, DOI 10.1016/j.jaci.2014.04.015, lire en ligne, consulté le ).
- (en) Claudia Traidl-Hoffmann, Anna Kasche, Thilo Jakob et Michael Huger, « Lipid mediators from pollen act as chemoattractants and activators of polymorphonuclear granulocytes », Journal of Allergy and Clinical Immunology, vol. 109, no 5, , p. 831–838 (DOI 10.1067/mai.2002.124655, lire en ligne, consulté le ).
- (en) Mohamed Elfatih H. Bashir, Jan Hsi Lui, Ravishankar Palnivelu et Robert M. Naclerio, « Pollen Lipidomics: Lipid Profiling Exposes a Notable Diversity in 22 Allergenic Pollen and Potential Biomarkers of the Allergic Immune Response », PLoS ONE, vol. 8, no 2, , e57566 (ISSN 1932-6203, PMID 23469025, PMCID PMC3585183, DOI 10.1371/journal.pone.0057566, lire en ligne, consulté le )
- (en) B. Heydenreich, I. Bellinghausen, B. König et W.-M. Becker, « Gram-positive bacteria on grass pollen exhibit adjuvant activity inducing inflammatory T cell responses », Clinical & Experimental Allergy, vol. 42, no 1, , p. 76–84 (DOI 10.1111/j.1365-2222.2011.03888.x, lire en ligne, consulté le )
- (en) Jesper E. Mogensen, Reinhard Wimmer, Jørgen N. Larsen et Michael D. Spangfort, « The Major Birch Allergen, Bet v 1, Shows Affinity for a Broad Spectrum of Physiological Ligands », Journal of Biological Chemistry, vol. 277, no 26, , p. 23684–23692 (ISSN 0021-9258 et 1083-351X, DOI 10.1074/jbc.M202065200, lire en ligne, consulté le ).
- ANSES (2013) L'Anses présente ses priorités de travail pour l'année 2013 ; 18/03/2013, consulté 21/03/2013
Voir aussi
modifierBibliographie
modifier- Peltre G. Interrelation entre les pollens allergisants et la pollution de l'air. Allerg Immunol 1998 ; 30 : 324-6.
- Schinko HAE, Medinger W, Hager W. Oberflachenfracht von Pollen im Ballungsraum. Atemwegs- und Lungendkr 1995 ; 21 : S54-6.
- (en) A. K. Shukla, M. R. Vijayaraghavan, B. Chaudhry, Biology of Pollen, APH Publishing, , 133 p. (lire en ligne)
- (en) Amots Dafni, Michael Hesse et Ettore Pacini, Pollen and Pollination, Springer Science & Business Media, , 336 p. (lire en ligne)
Articles connexes
modifierLiens externes
modifier- Site du RNSA (France), réseau national surveillance aérobiologique qui fournit des cartes et des calendriers polléniques : http://www.pollens.fr/accueil.php
- (en) PalDat - Palynological Database - an online publication on recent pollen
- (en) The Global Pollen Project. The Open Platform for Pollen Identification
- [vidéo] CETTE CHOSE PEUT NOUS RENDRE TRÈS MALADE ! sur YouTube, chaîne Dr Nozman.