Narirutine
La narirutine est un composé organique de la famille des flavanones, un sous-type de flavonoïdes. C'est plus précisément un hétéroside de flavanone, le 7-O-rutinoside de la naringinine (4',5,7-trihydroxyflavanone).
| Narirutine | |
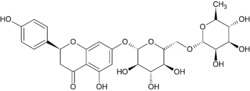
| |
| Identification | |
|---|---|
| Nom UICPA | (S)-7-[[6-O-(6-désoxy-α-L-mannopyranosyl)-β-D-glucopyranosyl]oxy]-2,3-dihydro-5-hydroxy-2-(4-hydroxyphényl)-4H-1-benzopyran-4-one |
| Nom systématique | (2S)-5-hydroxy-2-(4-hydroxyphényl)-7-[(2S,3R,4S,5S,6R)-3,4,5-trihydroxy-6-[[(2R,3R,4R,5R,6S)-3,4,5-trihydroxy-6-méthyloxan-2-yl]oxyméthyl]oxan-2-yl]oxy-2,3-dihydrochromén-4-one |
| Synonymes |
Naringinine 7-O-rutinoside, isonaringénine, |
| No CAS | |
| No ECHA | 100.034.655 |
| No CE | 238-138-0 |
| PubChem | 442431 |
| SMILES | |
| InChI | |
| Apparence | poudre blanche[1] |
| Propriétés chimiques | |
| Formule | C27H32O14 |
| Masse molaire[2] | 580,534 6 ± 0,028 g/mol C 55,86 %, H 5,56 %, O 38,58 %, |
| Propriétés physiques | |
| T° ébullition | 180 °C[1] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
La narirutine a été isolée (1965[3]) dans le grapefruit (Citrus paradisi)[4], elle est présente dans le fruit jeune de Citrus grandis[1] (« pomélo ») ou le jus de la plupart des agrumes, jus d'orange (de 15 à 85 mg/l)[5],[6],[7], jus de lime[8], jus de mandarine[9], le citron Meyer, les agrumes japonais sambokan, kabosu, sudachi, yuko, yuzu, hébesu[10].
Présence dans les plantes
modifierDans une publication sur la variation du niveau de flavonoïdes et des limonoïdes des feuilles des cultivars de mandariniers selon les phases de l'alternance biennale des universitaires uruguayens ont mesuré (2022) des niveaux très variables de narirutine les années on ou off chez les mandariniers alternants. Ils ont proposé d'en faire un biomarqueur[11].
Potentiel pharmacologique
modifierElle pourrait posséder de propriétés antiallergiques, anti-inflammatoires, anti-prolifératives et antioxydantes[3].
Une recherche (2021) in silico sur l'interaction de la narirutine avec huit récepteurs distincts impliqués dans le contrôle et les complications du diabète, et son potentiel d'inhibition de l'alpha-amylase et l'alpha-glucosidase laisse penser qu'elle peut contribuer activement à la gestion du diabète et de ses complications[12].
Notes et références
modifier- Fiche Sigma-Aldrich du composé Narirutin, consultée le 14 septembre 2020.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- https://cdn.caymanchem.com/cdn/insert/25124.pdf
- HPLC Analysis of Flavonoids in Grapefruit Juice on Ascentis® C18
- Interferences with naringin and neohesperidin analysis by high performance liquid chromatography. Widmer W.W and Martin S.F., 1993
- HPLC Analysis of Flavonoids in Orange Juice on Ascentis® C18
- « Narirutin - an overview | ScienceDirect Topics », sur www.sciencedirect.com (consulté le )
- HPLC Analysis of Flavonoids in Lime Juice on Ascentis® C18
- (en) Mayra Lucía Anticona Barreto, « Analysis of polyphenols content and antioxidant capacity from hybrids mandarin peel », The 2nd International Electronic Conference on Foods, (lire en ligne, consulté le )
- 三宅 義明, « 地域特産カンキツ類が含有する機能性物質の特徴 », Ffiジャーナル, vol. 227, no 1, , p. 043–049 (DOI 10.34457/ffij.227.1_043, lire en ligne, consulté le )
- (en) Cecilia Rodríguez Ceraolo, Valeria Vázquez, Ignacio Migues et María Verónica Cesio, « Flavonoids and Limonoids Profiles Variation in Leaves from Mandarin Cultivars and Its Relationship with Alternate Bearing », Agronomy, vol. 12, no 1, , p. 121 (ISSN 2073-4395, DOI 10.3390/agronomy12010121, lire en ligne, consulté le )
- (en) Ashraf Ahmed Qurtam, Hamza Mechchate, Imane Es-safi et Mohammed Al-zharani, « Citrus Flavanone Narirutin, In Vitro and In Silico Mechanistic Antidiabetic Potential », Pharmaceutics, vol. 13, no 11, , p. 1818 (ISSN 1999-4923, DOI 10.3390/pharmaceutics13111818, lire en ligne, consulté le )