Encéphalomyélite Myalgique/Syndrome de Fatigue Chronique
L'encéphalomyélite myalgique/syndrome de fatigue chronique (EM/SFC), également connu sous le nom de maladie d'intolérance systémique à l'effort, ou syndrome post-viral, est une maladie systémique caractérisée par le malaise post-effort, consistant en une incapacité à tolérer l'effort physique et cognitif. Cette maladie a été identifié dans les pays anglo-saxons au milieu des années 1980[1].
| Causes | Inconnue, Herpèsvirus humain type 6, Herpèsvirus humain type 7, Borna disease virus (d) ou virus d'Epstein-Barr |
|---|---|
| Symptômes | Myalgie, arthralgie, céphalée, obnubilation de la conscience, frissonnement (en), sueurs nocturnes, chronic widespread pain (d), post-exertional malaise (en), ganglion lymphatique, mal de gorge (en), elevated tumor necrosis factor (d), elevated interleukin-2 (d), elevated interleukin-4 (d), elevated transforming growth factor-β (d) et elevated c-reactive protein (d) |
| Traitement | Rintatolimod (en) et pyridostigmine |
|---|---|
| Médicament | Venlafaxine, coenzyme Q10, oxybate de sodium (en) et rintatolimod (en) |
| Spécialité | Neurologie et rhumatologie |
| CISP-2 | A04 |
|---|---|
| CIM-10 | G93.3 |
| CIM-9 | 780.71 |
| DiseasesDB | 1645 |
| MedlinePlus | 001244 |
| eMedicine |
235980 ped/2795 |
| MeSH | D015673 |
| Patient UK | Myalgic-encephalomyelitischronic-fatigue-syndrome-mecfs-pro |
L'Organisation mondiale de la santé (OMS) reconnaît cette maladie dans son code diagnostique CIM-10 sous le nom « syndrome de fatigue post-virale, encéphalomyélite myalgique bénigne » (numéro G93.3), et la place au rang des troubles neurologiques.
Terminologie modifier
L'appellation recommandée par l'Académie nationale de médecine aux États-Unis est celle d'intolérance systémique à l'effort (Systemic exertion intolerance disease, ou SEID), reflétant le symptôme de base, à savoir le malaise post-effort, consistant en une incapacité à tolérer l'effort physique et cognitif.
L'ancienne appellation « syndrome de fatigue chronique » (chronic fatigue syndrome en anglais), toujours largement usitée, fait l'objet de critiques car elle s'avère porteuse de préjugés négatifs qui n'avaient pas été anticipés au moment où elle a été choisie. Ainsi le Dr. Anthony Komaroff, dans une interview publiée en 2016 par les CDC américains (Centers for Disease Control and Prevention), indique comment cette appellation a été choisie sans réflexion approfondie à la fin des années 1980 par le comité scientifique des CDC dont il faisait partie. Il pense désormais que c'était une grosse erreur, car elle banalise et stigmatise à la fois la maladie, et la fait paraître sans importance, peut-être même sans réalité. Il se prononce en faveur de la nouvelle dénomination : « intolérance systémique à l'effort » (Systemic exertion intolerance disease)[2].
Le terme d'encéphalomyélite myalgique, qui signifie une inflammation de la moelle épinière et du cerveau avec des douleurs musculaires, est lui aussi sujet à discussion : il existe une variété de définitions correspondant à des ensembles de critères diagnostiques différents[3].
Causes possibles ou soupçonnées modifier
Causes possibles modifier
Les causes du syndrome de fatigue chronique ne sont actuellement pas connues[4].
Plusieurs hypothèses évoqueraient une origine virale, mais ces hypothèses n'ont pour le moment pas été vérifiées :
- une origine virale notamment attribuée au rétrovirus XMRV a été évoquée (Xenotropic MLV - Related Virus, variante du virus de la leucémie murine), mais les hypothèses de l'article initial n'ont jamais pu être reproduites ensuite[5],[6],[7],[8],[9] ;
- des infections virales ont été détectées chez les personnes atteintes de fatigue chronique, on détecte par exemple des virus de la famille des herpèsvirus (Epstein-Barr, HHV-6, HHV-7, cytomégalovirus), des entérovirus dans l'estomac (virus de la famille Coxsackie B et Echovirus), ainsi que le Parvovirus B19[10], sans que de liens puissent être établis pour le moment.
Caractéristiques biologiques modifier
En raison de la grande complexité de ce syndrome et de l'ignorance d'une cause bien définie qui lui serait attribuée, les symptômes de l'EM / SFC ont parfois été confondus avec plusieurs maladies sans rapport[11].
Plusieurs marqueurs biologiques ont été relevés, permettant d'isoler les caractéristiques biologiques et psycho-sociales de la maladie :
- anomalies métaboliques : des examens métaboliques ont indiqué, par des anomalies dans les protéines et le sang, que les voies métaboliques des personnes EM / SFC étaient altérées au point de montrer des dysfonctions dans les mécanismes de production énergétique de base[12] ;
- malaise post-effort : des études ayant pour objet l'utilisation de l'oxygène dans la cellule montrent le passage de l'état aérobique à l'état anaérobique chez les patients EM / SFC, mettant en évidence des anomalies permettant de distinguer cette maladie, par exemple, de la dépression[12] ;
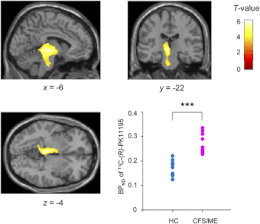
- inflammation neurologique : des examens par imagerie par résonance magnétique ont montré une réduction des volumes de matière grise et blanche, montrant des dommages neurologiques, ce qui correspond aux problèmes de mémoire à court terme et autres troubles cognitifs relevés chez les patients. Un haut niveau de douleur et de troubles cognitifs est lié à la suractivité des cellules gliales[12] ;
- inflammation systémique : de hauts niveaux de cytokines dans le sang ainsi que dans le liquide cérébrospinal des patients indiquent une inflammation générale ;
- immunodéficience : des analyses montrent des niveaux réduits d'une protéine essentielle pour le bon fonctionnement des lymphocytes NK, une cellule du système immunitaire servant à réguler les niveaux d'infection[12] ;
- auto-immunité : le comportement des lymphocytes T chez les patients EM / SFC à l'égard de la sélection des cibles est comparable aux modifications observées chez les gens atteints de cancer et de sclérose en plaques. La diminution des lymphocytes B, lesquelles produisent les anticorps, au moyen du Rituximab, a produit des effets notables chez certains patients[12] ;
- altération du microbiome intestinal : plusieurs études montrent une altération des bactéries intestinales chez les patients EM / SFC[12] ;
- une fatigue chronique est également associée à la myofasciite à macrophages[13].
Des examens métabolomiques permettent de mettre en évidence une signature chimique correspondant au syndrome de fatigue chronique. Les résultats d'études avec groupe contrôle montrent qu'il existe chez les malades un phénomène analogue au dauer, dans lequel les cellules entrent en état hypométabolique afin de résister à un stress extérieur, au prix d'une réduction de la qualité de vie et de nombreuses fonctions[14].
Symptômes et diagnostic modifier
Critères de l'Académie nationale de médecine des États-Unis (2015) modifier
- Réduction ou altération substantielle de la capacité à s'engager dans les mêmes activités que dans la période pré-maladie, persistant depuis plus de six mois et accompagnée d'une fatigue, d'apparition précoce, dont la cause n'est pas liée à des efforts excessifs en cours, et qui n'est pas atténuée par le repos.
- Malaise post-effort.
- Sommeil non réparateur.
Au moins l'un des deux symptômes suivants doit être présent :
Critères du consensus canadien sur l'EM / SFC de 2003 publiés par Santé Canada modifier
- Fatigue :
- Épuisement physique et mental ;
- Niveau d'activité réduit de façon substantielle par rapport à avant la maladie.
- Malaise et / ou fatigue post-effort :
- Peu d'endurance, et fatigabilité physique ou mentale ;
- Symptômes post-effort (malaise, épuisement, douleur, aggravation des autres symptômes) ;
- Récupération anormalement longue.
- Dysfonctionnement du sommeil :
- Sommeil non reposant ;
- Autres problèmes de sommeil.
- Douleur :
- Douleur musculaire ou articulatoire ;
- Douleur répandue et migratoire ;
- Maux de tête significatifs.
- Manifestations neurocognitives (au moins deux) :
- Confusion ;
- Troubles de la concentration ou de la mémoire à court terme ;
- Désorientation ;
- Difficultés avec le traitement de l'information et de la catégorisation ;
- Difficultés pour trouver le mot juste ;
- Ataxie, fasciculation, faiblesse musculaire ;
- Surcharges cognitives et sensorielle (hypersensibilité au bruit, photophobie) ;
- Surcharges émotionnelles pouvant mener à des phénomènes d'asthénie, ou à de l'anxiété.
- Au moins un symptôme dans deux des trois catégories suivantes :
- symptômes du système nerveux autonome :
- Intolérance orthostatique : hypotension à médiation neuronale (NMH), syndrome de tachycardie orthostatique posturale (POTS), hypotension posturale différée,
- Impression d'étourdissement,
- Pâleur extrême,
- Nausée, syndrome de l'intestin irritable ou syndrome du côlon irritable (SII ou IBS),
- Troubles urinaires,
- Palpitations,
- Difficulté de respiration à l'effort ;
- symptômes neuroendocriniens :
- Problème de stabilité de la température corporelle (température du corps inférieure à la normale avec fluctuations diurnes importantes, épisodes de transpiration, extrémités froides, sensations fiévreuses répétées),
- Intolérance aux températures extrêmes,
- Changement de poids, changement de l'appétit,
- Perte d'adaptabilité et aggravation due au stress ;
- symptômes immunitaires :
- Ganglions lymphatiques sensibles,
- Mal de gorge récurrent,
- Symptômes grippaux récurrents,
- Malaise général,
- Nouvelles intolérances à des aliments, médicaments, produits chimiques.
- symptômes du système nerveux autonome :
- Symptômes persistant pendant au moins six mois.
Critères de Fukuda (1994) modifier
Il est important de noter que les critères de Fukuda sont plus larges que les définitions modernes de l’EM/SFC, et donc ils peuvent diagnostiquer des patients qui ne seraient plus considérés comme souffrant de l’EM/SFC de nos jours[15].
- Fatigue ressentie pendant une période de six mois consécutifs ou plus et la fatigue n'est pas due à un effort continu actuel ou à d'autres conditions médicales associées à la fatigue.
- La fatigue interfère de manière significative avec la tenue des activités quotidiennes et le travail, éventuellement en lien avec des troubles musculo-squelettiques (TMS).
4 des 8 symptômes suivants :
- trouble de la mémoire ou de la concentration ;
- pharyngite ;
- ganglions cervicaux ou axillaires ;
- myalgies (douleurs musculaires) ;
- polyarthralgies non inflammatoires (douleurs aux articulations) ;
- céphalées (maux de tête) ;
- sommeil non réparateur ;
- malaise après effort physique.
Exclure :
- maladie organique présente ou passée ;
- maladie psychiatrique avérée.
Pronostic modifier
La maladie est une maladie chronique, qui n’a pas de traitement approuvé et est donc une maladie à vie.[16]
Une augmentation de la mortalité due à cette maladie est possible, vu un risque d'incident cardiovasculaire[17] et suicidaire accru[18]. Le syndrome a longtemps été confondu avec la conséquence de la dépression car l'invalidité provoquée et la non reconnaissance de la maladie détériorent l'humeur[19]. En 2010, un procès a été ouvert en Angleterre pour un suicide assisté d'une jeune femme porteuse de l’EM[20].
Traitements modifier
Il existe différentes approches pour cette maladie, qui n'ont cela dit pas démontré leur efficacité, telles que l'utilisation de compléments alimentaires (par exemple le Q10 ou le magnésium), la thérapie cognitivo-comportementale (TCC) basée sur des exercices de pensée positive couplée avec de l'exercice physique[21],[22],[23], les exercices de gymnastique médicale ou les thérapies d'adaptation et de simulation.
Controverses sur les traitements modifier
Une étude britannique a montré des effets positifs de la thérapie cognitivo-comportementale. D'après cette étude deux patients sur trois ne nécessitaient plus de traitement après une période de deux ans, selon des essais de PACE. L'étude n'a par contre pas adapté les critères du SFC pour choisir les participants. En conséquence, cet études ne différencie pas assez entre la fatigue en général, due à d'autres maladies en dehors du SFC. Cependant, le symptôme phare de la maladie représente la malaise après excercion, ce qui met en question les résultats de cet études[24].
Le manque de respect des protocoles de base des essais thérapeutique et de la méthodologie lors des essais PACE ont donc été dénoncées par plusieurs spécialistes[25].
Les médecins ayant participé à l'élaboration du Consensus canadien de 2003 sur le syndrome de fatigue chronique réfutent le présupposé thérapeutique selon lequel « la physiopathologie de l'EM / SFC [serait] entièrement réversible et ne se perpétue[rait] qu'en raison de l'interaction de processus cognitifs, comportementaux et émotionnels », comme quoi la TCC aurait dans ce contexte un « potentiel curatif », les malades devant être pris en charge à la manière des personnes atteintes de « syndromes somatiques fonctionnels »[26].
Ces médecins en appellent notamment à la mise en place de stratégies d'autothérapie dans la relation soignant / soigné, par exemple l'autodéveloppement et les exercices autogérés. Les programmes d'exercices graduels dont la cadence échappe au patient ainsi que les thérapies qui présupposent que celui-ci a une perception incorrecte de sa maladie sont vus comme néfastes[26].
Certains spécialistes invoquent les observations mettant en avant une pathologie du système nerveux central ainsi que l'hypothèse d'une infection chronique, afin d'écarter l'hypothèse selon laquelle ces syndromes seraient créés ou amplifiés par une détresse psychiatrique sous-jacente[27].
Situation médicale en France modifier
Le professeur de Korwin, du département de médecine interne et d'immunologie clinique au CHU de Nancy-hôpitaux de Brabois-BPC et président du conseil de l'Association française du syndrome de fatigue chronique (ASFC) dénonce l'absence de fonds dévolus à la recherche sur cette maladie en France, le manque de recherches via l'INSERM, ainsi que le manque de protocoles diagnostiques réalisés pour permettre de rendre les symptômes objectifs, comme l'absence de biopsies musculaires pour des patients devenus incapables de se mouvoir normalement. Il évoque les appels abusifs à des causes psychiatriques ainsi que l'impuissance des médecins à faire face à une maladie non suffisamment reconnue, pour laquelle il n'existe pas de traitement de référence et avec de nombreuses hypothèses étiologiques[28].
Personnalités historiques modifier
Florence Nightingale a été citée pour avoir souffert, à partir de 1854, et de l'âge de trente-cinq à soixante ans, de douleurs dans la poitrine, de maux de tête, de fatigue musculaire rapide, de douleurs chroniques dans le haut du dos, et de l'impossibilité de se concentrer si plusieurs personnes étaient présentes dans la pièce[29], symptômes rapprochés des suites d'une infection par la brucellose ou la fièvre de Crimée.
La Nightingale Research Foundation, fondée en 1988 et destinée à la recherche sur l'encéphalomyélite myalgique / syndrome de fatigue chronique et les maladies du type fibromyalgie, située à Ottawa, porte son nom afin de commémorer sa volonté de continuer à contribuer à la société malgré l'obligation de passer la plupart de son temps alitée[30].
Le pianiste et compositeur Keith Jarrett a été obligé de suspendre son activité, puis de mettre un terme à sa carrière après avoir été atteint par le syndrome de fatigue chronique[31].
L'écrivaine américaine Ann Bannon, autrice de romans de gare lesbiens, souffrait de ce syndrome[32].
L'écrivaine américaine Laura Hillenbrand, notamment connue pour sa série de romans consacrée au cheval de course Seabiscuit (adaptée au cinéma en 2003 sous le titre Pur Sang, la légende de Seabiscuit), souffre d'un syndrome de fatigue chronique contracté durant son adolescence et jamais guéri depuis. Elle évoque cet aspect de sa vie dans l'article A Sudden Illness paru dans The New York Times en 2003[33].
Évocations dans les arts modifier
Dans la série télévisée américaine Les Craquantes, diffusée de 1985 à 1992, le diptyque d'épisodes « Sick and Tired » (« Malade et fatiguée »), diffusé en septembre 1989, montre le personnage de Dorothy Zbornak affectée par de symptômes déroutants qui l'entraînent dans un parcours médical compliquée. Elle finit par être diagnostiquée comme souffrant d'un syndrome de fatigue chronique[34].
Le film The Lost King de Stephen Frears, sorti en 2022, s'inspire des recherches de Philippa Langley pour retrouver la tombe du roi britannique Richard III. Dans le film, Philippa Langley est atteinte du syndrome de fatigue chronique et doit lutter pour maintenir une vie professionnelle tout en faisant reconnaître son handicap.
Notes et références modifier
- (en) G. Holmes, J. Kaplan, N. Gantz, A. Komaroff, L. Schonberger, S. Straus, J. Jones, R. Dubois, C. Cunningham-Rundles, S. Pahwa, G. Tosato, L. S. Zegans, D. T. Purtilo, N. Brown, R. T. Schooley et I. Brus, « Chronic fatigue syndrome: a working case definition », Annals of Internal Medicine, vol. 108, no 3, , p. 387-389 (lire en ligne)
- Beyond the Data – Chronic Fatigue Syndrome: Advancing Research and Clinical Education. Lien youtube (en anglais) : https://www.youtube.com/watch?v=hRdn4A2SGic&t=485s
- Propositions de modifications de la CIM-10 relative au Syndrome de fatigue chronique, à l'Encéphalomyélite myalgique, et au Syndrome de fatigue postvirale
- (en-US) « Myalgic Encephalomyelitis/Chronic Fatigue Syndrome (ME/CFS) | CDC », sur cdc.gov, (consulté le ).
- (en) Vincent C. Lombardi, Francis W. Ruscetti, Jaydip Das Gupta, Max A. Pfost, Kathryn S. Hagen, Daniel L. Peterson, Sandra K. Ruscetti, Rachel K. Bagni, Cari Petrow-Sadowski, Bert Gold, Michael Dean, Robert H. Silverman et Judy Mikovits, « Detection of an Infectious Retrovirus, XMRV, in Blood Cells of Patients with Chronic Fatigue Syndrome », Science, vol. 326, no 5952, , p. 585-589 (PMID 19815723, DOI 10.1126/science.1179052, résumé, lire en ligne)
- G. Simmonset et al., « Failure to Confirm XMRV/MLVs in the Blood of Patients with Chronic Fatigue Syndrome: A Multi-Laboratory Study », Science, vol. 334, no 814, (DOI 10.1126/science.1213841)
- (en) O. Erlwein, S. Kaye, M. O. McClure, J. Weber, G. Wills, D. Collier, S. Wessely et A. Cleare, « Failure to detect the novel retrovirus XMRV in chronic fatigue syndrome », PLoS One, vol. 5, no 1, (résumé, lire en ligne)
- (en) Frank J. M. van Kuppeveld, Arjan S. de Jong, Kjerstin H. Lanke, Gerald W. Verhaegh, Willem J. G. Melchers, Caroline M. A. Swanink, Gijs Bleijenberg, Mihai G. Netea, Jochem M. D. Galama et Jos W. M. van der Meer, « Prevalence of xenotropic murine leukaemia virus-related virus in patients with chronic fatigue syndrome in the Netherlands: retrospective analysis of samples from an established cohort », BMJ, vol. 340, no c1018, (résumé, lire en ligne)
- (en) Konstance Knox, Donald Carrigan, Graham Simmons, Fernando Teque, Yanchen Zhou, John Hackett Jr., Xiaoxing Qiu, Ka-Cheung Luk, Gerald Schochetman, Allyn Knox, Andreas M. Kogelnik et Jay A. Levy, « No Evidence of Murine-Like Gammaretroviruses in CFS Patients Previously Identified as XMRV-Infected », Science, American Association for the Advancement of Science, vol. 333, no 6038, , p. 94-97 (ISSN 0036-8075 et 1095-9203, DOI 10.1126/science.1204963, résumé, lire en ligne)
- « Syndrome De Fatigue Chronique — Feuille De Route De Tests Et De Traitements »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur sites.google.com (consulté le ).
- Aude Rambaud, « Que sait-on du syndrome de fatigue chronique ? », sur sante.lefigaro.fr.
- Rochelle Joslyn, « ME/CFS Research Roundup: Brief highlights of biomedical research to date », sur medium.com, (consulté le ).
- (en) Authier FJ, Sauvat S, Champey J. et al., « Chronic fatigue syndrome in patients with macrophagic myofasciitis. Concise communications », Arthritis Rheum., vol. 48, , p. 569–72.
- Committee on the Diagnostic Criteria for Myalgic Encephalomyelitis/Chronic Fatigue Syndrome, Board on the Health of Select Populations et Institute of Medicine, Beyond Myalgic Encephalomyelitis/Chronic Fatigue Syndrome: Redefining an Illness, National Academies Press (US), coll. « The National Academies Collection: Reports funded by National Institutes of Health », (ISBN 978-0-309-31689-7, PMID 25695122, lire en ligne)
- (en) Hannah E. Davis, Lisa McCorkell, Julia Moore Vogel et Eric J. Topol, « Long COVID: major findings, mechanisms and recommendations », Nature Reviews Microbiology, vol. 21, no 3, , p. 133–146 (ISSN 1740-1534, PMID 36639608, PMCID PMC9839201, DOI 10.1038/s41579-022-00846-2, lire en ligne, consulté le )
- (en) Stephanie. McManimen et al., « Mortality in Patients with Myalgic Encephalomyelitis and Chronic Fatigue Syndrome », Center for Community Research, DePaul University., vol. 4, no 4, , p. 195-207 (résumé)
- (en) W. R. Smith, C. Noonan et D. Buchwald, « Mortality in a cohort of chronically fatigued patients », Psychological Medecine, vol. 36, no 9, , p. 1301-1306 (résumé)
- (en) S. B. Harvey, M. Wadsworth, S. Wessely et M. Hotopf, « The relationship between prior psychiatric disorder and chronic fatigue: evidence from a national birth cohort study », Psychological Medecine, vol. 38, no 7, , p. 933-940 (résumé)
- (en) Alastair M. Santhouse, Matthew Hotopf et Anthony S. David, « Chronic fatigue syndrome », BMJ, vol. 340, no c738, (résumé)
- (en) D. Chambers, A. M. Bagnall, S. Hempel et C. Forbes, « Interventions for the treatment, management and rehabilitation of patients with chronic fatigue syndrome/myalgic encephalomyelitis: an updated systematic review », Journal of the Royal Society of Medecine, vol. 99, , p. 506-520 (résumé, lire en ligne)
- Associated Press, « Remise en question les traitements contre la fatigue chronique », sur cyberpresse.ca, .
- (en) P. D White, K. A. Goldsmith, A. L. Johnson, L. Potts, R. Walwyn, J. C. DeCesare, H. L. Baber, M. Burgess, L. V. Clark, D. L. Cox, J. Bavinton, B. J. Angus, G. Murphy, M. Murphy, H. O'Dowd, D. Wilks, P. McCrone, T. Chalder et M. Sharpe, « Comparison of adaptive pacing therapy, cognitive behaviour therapy, graded exercise therapy, and specialist medical care for chronic fatigue syndrome (PACE): a randomised trial », The Lancet, (lire en ligne)
- (en) Sharpe M, Goldsmith KA, Johnson AL, Chalder T, Walker J, White PD, « Rehabilitative treatments for chronic fatigue syndrome: long-term follow-up from the PACE trial », Lancet Psychiatry, , S2215-0366(15)00317-X. Prépublication en ligne (PMID 26521770, DOI 10.1016/S2215-0366(15)00317-X)
- « Qu'est-ce que le PACE trial et pourquoi vous devriez vous y intéresser », sur EM Action, (consulté le ).
- Abrégé du Consensus canadien sur l'encéphalomyélite myalgique / syndrome de fatigue chronique par l'Association québécquoise de l'encéphalomyélite myalgique (2008)
- The biology of chronic fatigue syndrome, Anthony L. Komaroff, 2000
- ASFC ADENUM, « Table ronde Unrest - 12/05/2018 - partie III » (consulté le ).
- Roberto Patarca-Montero, Medical Etiology, Assessment, and Treatment of Chronic Fatigue and Malaise, Haworth Press, 2004, p. 4. (ISBN 078902196X)
- (en) « About | Nightingale Research Foundation », sur website-1 (consulté le ).
- « L'actualité du jazz : Keith Jarrett, le retour de l'enfer », sur francemusique.fr, .
- P. Cain P, "Ann Bannon". Leading the parade: Conversations with America's most influential lesbians and gay men, Scarecrow Press, Inc., 2007, p. 155–63. (ISBN 978-0-8108-5913-5).
- A Sudden Illness, article de Laura Hillenbrand dans The New York Times le 7 juillet 2003. Page conservée sur l'Internet Archive dans son état du 29 mai 2013. Page consultée le 3 septembre 2023.
- Golden Girls, Chronic Fatigue Syndrome, and the Legacies of Hysteria, article d'Amanda Stayton et Bridget Keown sur Nursing Clio le 25 septembre 2018. Page consultée le 3 septembre 2023.
Voir aussi modifier
Articles connexes modifier
Bibliographie modifier
- [Cozon 2014] Grégoire Cozon, Le syndrome de fatigue chronique, Lyon, Michel servet, , 94 p. (ISBN 978-2-84812-002-7 et 2-84812-002-9).
- [A. Jason 2003] (en) Leonard A. Jason, Patricia A. Fennel, Renee R. Taylor, Handbook of Chronic Fatigue Syndrome, John Wiley & Sons, , 94 p. (ISBN 0-471-41512-X).
Articles de presse modifier
- [Gicquel 2018] Jérôme Gicquel, « Qu’est ce que le syndrome de fatigue chronique qui toucherait près de 150.000 Français? », 20 minutes, .
- [Prigent 2019] Anne Prigent, « Fatigue chronique: un syndrome encore trop méconnu », Le Figaro, .
- [Bennarosh 2015] Sophie Bennarosh, « Comment je vis avec le Syndrome de Fatigue Chronique », Huffpost, .
Liens externes modifier
- Ressources relatives à la santé :
- Notice dans un dictionnaire ou une encyclopédie généraliste :
- Rapport d'évaluation de 2009 de l'AETMIS (Canada) sur le syndrome de fatigue chronique
- Consensus canadien sur l’EM/SFC
- Association Française du Syndrome de Fatigue Chronique
- La Journée internationale de reconnaissance de l'encéphalomyélite myalgique sur le site informations.handicap.fr
- Le Syndrome de fatigue chronique par la Revue Medicale Suisse
- « Le syndrome de fatigue chronique ; L’EM/SFC, une maladie trop peu (re)connue », Daniela Schmidt-Langels, 2021, ARTE.