Triméthylgallium
Le triméthylgallium (TMG), Ga(CH3)3, est un composé organométallique à base de gallium. C'est la source organométallique préférée en gallium pour l'épitaxie organométallique en phase vapeur (MOVPE) des composés semi-conducteur contenant du gallium, comme l'arséniure de gallium (GaAs), le nitrure de gallium (GaN), le phosphure de gallium (GaP), l'antimoniure de gallium (GaSb), l'arséniure de gallium-indium (GaInAs), le nitrure de gallium-indium (InGaN), etc.
| Triméthylgallium | |||
| |||
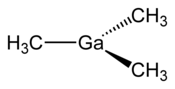
| Structure du triméthylgallium | |||
| Identification | |||
|---|---|---|---|
| No CAS | |||
| No ECHA | 100.014.452 | ||
| No CE | 215-897-6 | ||
| PubChem | 15051 | ||
| SMILES | |||
| InChI | |||
| Apparence | liquide incolore pyrophorique | ||
| Propriétés chimiques | |||
| Formule | C3H9Ga [Isomères] |
||
| Masse molaire[1] | 114,827 ± 0,004 g/mol C 31,38 %, H 7,9 %, Ga 60,72 %, |
||
| Propriétés physiques | |||
| T° fusion | −15,8 °C[2] | ||
| T° ébullition | 92,5 °C[2] | ||
| Masse volumique | 1,132 g·cm-3[2] à 25 °C | ||
| Pression de vapeur saturante | 19,3 kPa[2] à 20 °C | ||
| Précautions | |||
| SGH[2] | |||
| H250, H260, H314, P280, P231+P232, P303+P361+P353, P305+P351+P338, P370+P378 et P422 |
|||
| Transport[2] | |||
|
|||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
Le TMG est connu pour être pyrophorique, c.à.d. qu'il prend feu spontanément au contact de l'air. Même les solutions d'hydrocarbure de TMG, une fois suffisamment saturées, sont connues pour prendre feu spontanément au contact de l'air.
Le TMG est connu pour réagir violemment avec l'eau et d'autres composés capables de fournir un ion hydrogène libre actif (c'est-à-dire un proton). Par conséquent, le TMG doit être manipulé avec le soin et l'attention nécessaires, par exemple, entreposé dans un endroit frais et sec entre 0 °C et 25 °C, sous atmosphère inerte[3].
Utilisation
modifierDans la fabrication de semi-conducteurs, le triméthylgallium est utilisé en épitaxie en phase gazeuse dans le dépôt de couches de GaAs ou de GaN épitaxiées[4].
Notes et références
modifier- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Fiche Sigma-Aldrich du composé Trimethylgallium, consultée le 24 novembre 2018.
- Journal of Crystal Growth (2004); DOI doi:10.1016/j.jcrysgro.2004.09.007
- [1], air liquide, consulté le 7 septembre 2009



