Chimie combinatoire dynamique
Par définition moderne, la Chimie combinatoire dynamique (CDC) également connue sous le nom de chimie dynamique constitutionnelle (CDC) est une méthode pour faciliter la génération de molécules de nouvelle génération formées par liaisons réversibles de blocs de construction simples sous contrôle thermodynamique[1],[2].
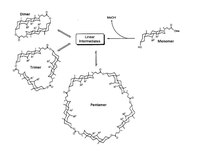
Ce principe est connu pour sélectionner le produit le plus thermodynamiquement stable à partir d'un mélange à l'équilibre constitué d'un certain nombre de composants, un concept couramment utilisé en chimie de synthèse pour contrôler la sélectivité de la réaction[3].
Structure
modifierLa bibliothèque de ces blocs de construction à conversion réversible est appelée bibliothèque combinatoire dynamique (DCL) [4],[5].
Tous les constituants d'un DCL sont en équilibre et leur distribution est déterminée par leur stabilité thermodynamique au sein du DCL. L'interconversion de ces blocs de construction peut impliquer des interactions covalentes ou non covalentes .
Lorsqu'un DCL est exposé à une influence externe (comme des protéines ou des acides nucléiques ), l'équilibre se déplace et les composants qui interagissent avec l'influence externe sont stabilisés et amplifiés, permettant à plus de composé actif de se former.
Histoire
modifierNaissance
modifierBien que cette approche ait sans doute été utilisée dans les travaux de Fischer[6] et Werner[7] dès le XIXe siècle, leurs études respectives sur les glucides et la chimie de coordination étaient limitées à la spéculation rudimentaire, nécessitant la justification de la thermodynamique moderne [8],[9].
Ce n'est que lorsque la chimie supramoléculaire a révélé les premiers concepts de reconnaissance moléculaire, de complémentarité et d'auto-organisation que les chimistes ont pu commencer à utiliser des stratégies pour la conception rationnelle et la synthèse de cibles macromoléculaires[10].
Formalisation moderne
modifierLe concept de la synthèse des matrices a été développé et rationalisé grâce aux travaux pionniers de Busch dans les années 1960, qui ont clairement défini le rôle d'une matrice d'ions métalliques dans la stabilisation du produit thermodynamique souhaité, permettant son isolation depuis le mélange complexe en équilibre[11],[12].
Bien que les travaux de Busch aient aidé à établir la méthode des gabarits comme une puissante voie de synthèse vers des structures macrocycliques stables, cette approche est restée exclusivement dans le domaine de la chimie inorganique jusqu'au début des années 1990, lorsque Sanders et al. a d'abord proposé le concept de chimie combinatoire dynamique. Leur travail a conduit à une association entre la modélisation thermodynamique en tandem et la chimie combinatoire, pour générer un ensemble complexe de macrocycles de porphyrine et d'imine en utilisant une sélection modeste de blocs de construction simples.
Sanders a ensuite développé cette première version de la chimie combinatoire dynamique comme stratégie de synthèse organique; le premier exemple étant la macrolactonisation thermodynamiquement contrôlée d'oligocholates pour assembler des macrocycles cycliques dérivés de stéroïdes capables d'interconversion via l'échange de composants[13]. Les premiers travaux de Sanders et al. a utilisé la transestérification pour générer des bibliothèques combinatoires dynamiques. L'utilisation des esters pour la médiation des échanges de composants est une action regrettable, car les processus de transestérification sont intrinsèquement lents et nécessitent des conditions anhydres vigoureuses[2]. Cependant, leurs recherches ultérieures ont identifié que les liaisons covalentes disulfure et hydrazone présentent des processus d'échange de composants efficaces et présentent ainsi un moyen fiable de générer des bibliothèques combinatoires dynamiques capables de templation thermodynamique. Cette chimie constitue désormais la base de nombreuses recherches dans le domaine en développement de la chimie covalente dynamique et est devenue ces dernières années un outil puissant pour la découverte de récepteurs moléculaires.
Orientation des protéines
modifierL'un des principaux développements dans le domaine du DCC est l'utilisation de protéines (ou d'autres macromolécules biologiques, telles que les acides nucléiques ) pour influencer l'évolution et la génération de composants au sein d'un DCL[15],[16],[17],[18],[19],[20]. Le DCC dirigé par des protéines fournit un moyen de générer, d'identifier et de classer de nouveaux ligands protéiques, et a donc un énorme potentiel dans les domaines de l'inhibition enzymatique et de la découverte de médicaments[21].
Réactions covalentes réversibles
modifierLe développement du DCC dirigé par les protéines n'a pas été simple car les réactions réversibles utilisées doivent se produire en solution aqueuse à pH et température biologiques, et les composants du DCL doivent être compatibles avec les protéines[15],[21].
Plusieurs réactions réversibles ont été proposées et / ou appliquées dans le DCC dirigé sur les protéines. Ceux-ci incluaient la formation d'ester boronate[14],[22],[23], échange de disélénides-disulfures[24], formation de sulfure[25],[26],[27], formation d'hémithiolacétal[28],[29], formation d'hydrazone[30],[31], formation d'imine [32],[33],[34] et échange thiol-énone[35].
DCL pré-équilibré
modifierPour les réactions réversibles qui ne se produisent pas dans des tampons aqueux, l'approche DCC pré-équilibrée peut être utilisée. Le DCL a été initialement généré (ou pré-équilibré) dans un solvant organique, puis dilué dans un tampon aqueux contenant la protéine cible pour la sélection. Des réactions réversibles à base organique, y compris des réactions de diels-Alder [36] et des réactions de métathèse croisée d'alcène[37], ont été proposées ou appliquées au DCC dirigé par les protéines en utilisant cette méthode.
Réactions non covalentes réversibles
modifierDes réactions réversibles non covalentes, telles que la coordination métal - ligand[38],[39], ont également été appliquées dans le DCC dirigé sur les protéines. Cette stratégie est utile pour l'étude de la stéréochimie optimale du ligand au site de liaison de la protéine cible[40].
Réactions réversibles catalysées par des enzymes
modifierDes réactions réversibles catalysées par des enzymes, telles que des réactions de formation / hydrolyse de liaisons amides catalysées par des protéases [41] et les réactions d'aldols catalysées par l' aldolase [42],[43] ont également été appliquées au DCC dirigé sur les protéines.
Méthodes analytiques
modifierLe système DCC dirigé par des protéines doit pouvoir être soumis à un dépistage efficace[15],[21]. Plusieurs techniques analytiques ont été appliquées à l'analyse des DCL dirigées vers les protéines. Il s'agit notamment de la HPLC[25],[29],[30],[33], spectrométrie de masse[22],[26],[27],[31], spectroscopie RMN[14],[23],[28], et cristallographie aux rayons X[44].
Approche multi-protéique
modifierBien que la plupart des applications du DCC dirigé vers les protéines à ce jour impliquent l'utilisation d'une seule protéine dans le DCL, il est possible d'identifier des ligands protéiques en utilisant plusieurs protéines simultanément, tant qu'une technique analytique appropriée est disponible pour détecter les espèces de protéines qui interagissent avec les composants DCL[45]. Cette approche peut être utilisée pour identifier des inhibiteurs spécifiques ou des inhibiteurs d'enzymes à large spectre.
Autres applications
modifierLe DCC est utile pour identifier les molécules aux propriétés de liaison inhabituelles et fournit des voies de synthèse vers des molécules complexes qui ne sont pas facilement accessibles par d'autres moyens. Ceux-ci comprennent des matériaux intelligents, des foldamères, des molécules auto-assemblées avec des architectures imbriquées et de nouveaux matériaux souples[2]. L'application du DCC pour détecter les composés bioactifs volatils, c'est-à - dire l'amplification et la détection de l' odeur, a été proposée dans un document conceptuel[46]. Récemment, le DCC a également été utilisé pour étudier les origines abiotiques de la vie[47].
Voir également
modifierNotes et références
modifier- Schaufelberger, F.; Timmer, B. J. J.; Ramström, O. Principles of Dynamic Covalent Chemistry. In Dynamic Covalent Chemistry: Principles, Reactions, and Applications; Zhang, W.; Jin, Y., Eds.; John Wiley & Sons: Chichester, 2018; Chapter 1, pp 1–30.
- Corbett, P. T., Leclaire, J., Vial, L. et West, K. R., « Dynamic combinatorial chemistry », Chem. Rev., vol. 106, no 9, , p. 3652–3711 (PMID 16967917, DOI 10.1021/cr020452p)
- Rowan, Cantrill, Cousins et Sanders, « Dynamic Covalent Chemistry », Angewandte Chemie International Edition, vol. 41, no 6, , p. 898–952 (ISSN 1521-3773, PMID 12491278, DOI 10.1002/1521-3773(20020315)41:6<898::AID-ANIE898>3.0.CO;2-E)
- Komáromy, D.; Nowak, P.; Otto, S. Dynamic Combinatorial Libraries. In Dynamic Covalent Chemistry: Principles, Reactions, and Applications; Zhang, W.; Jin, Y., Eds.; John Wiley & Sons: Chichester, 2018; Chapter 2, pp 31–119.
- Lehn, J.-M.; Ramström, O. Generation and screening of a dynamic combinatorial library. PCT. Int. Appl. WO 20010164605, 2001.
- Kunz, « Emil Fischer—Unequalled Classicist, Master of Organic Chemistry Research, and Inspired Trailblazer of Biological Chemistry », Angewandte Chemie International Edition, vol. 41, no 23, , p. 4439–4451 (ISSN 1521-3773, PMID 12458504, DOI 10.1002/1521-3773(20021202)41:23<4439::AID-ANIE4439>3.0.CO;2-6)
- Constable et Housecroft, « Coordination chemistry: the scientific legacy of Alfred Werner », Chem. Soc. Rev., vol. 42, no 4, , p. 1429–1439 (PMID 23223794, DOI 10.1039/c2cs35428d)
- Anderson, Anderson et Sanders, « Expanding roles for templates in synthesis », Accounts of Chemical Research, vol. 26, no 9, , p. 469–475 (ISSN 0001-4842, DOI 10.1021/ar00033a003)
- Hoss et Vögtle, « Template Syntheses », Angewandte Chemie International Edition in English, vol. 33, no 4, , p. 375–384 (ISSN 1521-3773, DOI 10.1002/anie.199403751)
- Lehn, « From supramolecular chemistry towards constitutional dynamic chemistry and adaptive chemistry », Chem. Soc. Rev., vol. 36, no 2, , p. 151–160 (PMID 17264919, DOI 10.1039/b616752g)
- Thompson et Busch, « Reactions of Coordinated Ligands. VI. Metal Ion Control in the Synthesis of Planar Nickel(II) Complexes of α-Diketo-bis-mercaptoimines », Journal of the American Chemical Society, vol. 86, no 2, , p. 213–217 (ISSN 0002-7863, DOI 10.1021/ja01056a021)
- Thompson et Busch, « Reactions of Coördinated Ligands. II. Nickel(II) Complexes of Some Novel Tetradentate Ligands », Journal of the American Chemical Society, vol. 84, no 9, , p. 1762–1763 (ISSN 0002-7863, DOI 10.1021/ja00868a073)
- Brady, Bonar-Law, Rowan et Suckling, « ?Living? macrolactonisation: thermodynamically-controlled cyclisation and interconversion of oligocholates », Chemical Communications, vol. 0, no 3, , p. 319–320 (DOI 10.1039/cc9960000319)
- Leung, I. K. H., Demetriades, M., Hardy, A. P. et Lejeune, C., « NMR reporter ligand screening for inhibitors of 2OG oxygenases », J. Med. Chem., vol. 56, no 2, , p. 547–555 (PMID 23234607, PMCID 4673903, DOI 10.1021/jm301583m)
- Greaney, M. F.; Bhat, V. T. Protein-directed dynamic combinatorial chemistry. In Dynamic combinatorial chemistry: in drug discovery, bioinorganic chemistry, and materials sciences; Miller, B. L., Ed.; John Wiley & Sons: New Jersey, 2010; Chapter 2, pp 43–82.
- Huang, R. et Leung, I. K. H., « Protein-directed dynamic combinatorial chemistry: a guide to protein ligand and inhibitor discovery », Molecules, vol. 21, no 7, , p. 910 (PMID 27438816, PMCID 6273345, DOI 10.3390/molecules21070910)
- Frei, P., Hevey, R. et Ernst, B., « Dynamic Combinatorial Chemistry: A New Methodology Comes of Age », Chem. Eur. J., vol. 25, no 1, , p. 60–73 (PMID 30204930, DOI 10.1002/chem.201803365)
- Jaegle, M., Wong, E. L., Tauber, C. et Nawrotzky, E., « Protein-templated fragment ligations - from molecular recognition to drug discovery », Angew. Chem. Int. Ed., vol. 56, no 26, , p. 7358–7378 (PMID 28117936, DOI 10.1002/anie.201610372)
- Mondal, M. et Hirsch, A. K., « Dynamic combinatorial chemistry: a tool to facilitate the identification of inhibitors for protein targets », Chem. Soc. Rev., vol. 44, no 8, , p. 2455–2488 (PMID 25706945, DOI 10.1039/c4cs00493k)
- Herrmann, A., « Dynamic combinatorial/covalent chemistry: a tool to read, generate and modulate the bioactivity of compounds and compound mixtures », Chem. Soc. Rev., vol. 43, no 6, , p. 1899–1933 (PMID 24296754, DOI 10.1039/c3cs60336a)
- Hochgürtel, M.; Lehn, J.-M. Dynamic combinatorial diversity in drug discovery. In Fragment-based approaches in drug discovery; Jahnke, W., Erlanson, D. A., Ed.; Wiley-VCH: Weinheim, 2006; Chapter 16, pp 341–364.
- Demetriades, M., Leung, I. K. H., Chowdhury, R. et Chan, M. C., « Dynamic combinatorial chemistry employing boronic acids/boronate esters leads to potent oxygenase inhibitors », Angew. Chem. Int. Ed., vol. 51, no 27, , p. 6672–6675 (PMID 22639232, DOI 10.1002/anie.201202000)
- Leung, I. K. H., Brown Jr, T., Schofield, C. J. et Claridge, T. D. W., « An approach to enzyme inhibition employing reversible boronate ester formation », Med. Chem. Commun., vol. 2, no 5, , p. 390–395 (DOI 10.1039/C1MD00011J)
- Rasmussen, B., Sørensen, A., Gotfredsen, H. et Pittelkow, M., « Dynamic combinatorial chemistry with diselenides and disulfides in water », Chem. Commun., vol. 50, no 28, , p. 3716–3718 (DOI 10.1039/C4CC00523F, lire en ligne)
- Ramström, O. et Lehn, J.-M, « In situ generation and screening of a dynamic combinatorial carbohydrate library against concanavalin A », ChemBioChem, vol. 1, no 1, , p. 41–48 (PMID 11828397, DOI 10.1002/1439-7633(20000703)1:1<41::AID-CBIC41>3.0.CO;2-L)
- Liénard, B. M. R., Selevsek, N., Oldham, N. J. et Schofield, C. J., « Combined mass spectrometry and dynamic chemistry approach to identify metalloenzyme inhibitors », ChemMedChem, vol. 2, no 2, , p. 175–179 (PMID 17206734, DOI 10.1002/cmdc.200600250)
- Liénard, B. M. R., Hüting, R., Lassaux, P. et Galleni, M., « Dynamic combinatorial mass spectrometry leads to metallo-β-lactamase inhibitors », J. Med. Chem., vol. 51, no 3, , p. 684–688 (PMID 18205296, DOI 10.1021/jm070866g)
- Caraballo, R., Dong, H., Ribeiro, J. P. et Jiménez-Barbero, J., « Direct STD NMR identification of β-galactosidase inhibitors from a virtual dynamic hemithioacetal system », Angew. Chem. Int. Ed., vol. 49, no 3, , p. 589–593 (PMID 20013972, DOI 10.1002/anie.200903920)
- Clipson, A. J., Bhat, V. T., McNae, I. et Caniard, A. M., « Bivalent enzyme inhibitors discovered using dynamic covalent chemistry », Chem. Eur. J., vol. 18, no 34, , p. 10562–10570 (PMID 22782854, DOI 10.1002/chem.201201507, lire en ligne)
- Hochgürtel, M., Niesinger, R., Kroth, H. et Piecha, D., « Ketones as building blocks for dynamic combinatorial libraries: highly active neuraminidase inhibitors generated via selective pressure of the biological target », J. Med. Chem., vol. 46, no 3, , p. 356–358 (PMID 12540234, DOI 10.1021/jm025589m)
- Sindelar, M., Lutz, T. A., Petrera, M. et Wanner, K. T., « Focused pseudostatic hydrazone libraries screened by mass spectrometry binding assay: optimizing affinities toward γ-aminobutyric acid transporter 1 », J. Med. Chem., vol. 56, no 3, , p. 1323–1340 (PMID 23336362, DOI 10.1021/jm301800j)
- Yang, Z., Fang, Z., He, W. et Wang, Z., « Identification of inhibitors for vascular endothelial growth factor receptor by using dynamic combinatorial chemistry », Bioorg. Med. Chem. Lett., vol. 26, no 7, , p. 1671–1674 (PMID 26920800, DOI 10.1016/j.bmcl.2016.02.063)
- Zameo, S., Vauzeilles, B. et Beau, J.-M., « Direct composition analysis of a dynamic library of imines in an aqueous medium », Eur. J. Org. Chem., vol. 2006, no 24, , p. 5441–5444 (DOI 10.1002/ejoc.200600859)
- Herrmann, A., « Dynamic mixtures and combinatorial libraries: imines as probes for molecular evolution at the interface between chemistry and biology », Org. Biomol. Chem., vol. 7, no 16, , p. 3195–3204 (PMID 19641772, DOI 10.1039/B908098H)
- Shi, B., Stevenson, R., Campopiano, D. J. et Greaney, M. F., « Discovery of glutathione S-transferase inhibitors using dynamic combinatorial chemistry », J. Am. Chem. Soc., vol. 128, no 26, , p. 8459–8467 (PMID 16802811, DOI 10.1021/ja058049y)
- Boul, P. J., Reutenauer, P. et Lehn, J.-M., « Reversible Diels-Alder reactions for the generation of dynamic combinatorial libraries », Org. Lett., vol. 7, no 1, , p. 15–18 (PMID 15624966, DOI 10.1021/ol048065k)
- Poulsen, S.-A. et Bornaghi, L. F., « Fragment-based drug discovery of carbonic anhydrase II inhibitors by dynamic combinatorial chemistry utilizing alkene cross metathesis », Bioorg. Med. Chem., vol. 14, no 10, , p. 3275–3284 (PMID 16431113, DOI 10.1016/j.bmc.2005.12.054)
- Sakai, S., Shigemasa, Y. et Sasaki, T., « A self-adjusting carbohydrate ligand for GalNAc specific lectins », Tetrahedron Lett., vol. 38, no 47, , p. 8145–8148 (DOI 10.1016/S0040-4039(97)10187-3)
- Sakai, S., Shigemasa, Y. et Sasaki, T., « Iron(II)-assisted assembly of trivalent GalNAc clusters and their interactions with GalNAc-specific lectins », Bull. Chem. Soc. Jpn., vol. 72, no 6, , p. 1313–1319 (DOI 10.1246/bcsj.72.1313, lire en ligne)
- Kilpin, K. J. et Dyson, P. J., « Enzyme inhibition by metal complexes: concepts, strategies and applications », Chem. Sci., vol. 4, no 4, , p. 1410–1419 (DOI 10.1039/C3SC22349C)
- Swann, P. G., Casanova, R. A., Desai, A. et Frauenhoff, M. M., « Nonspecific protease-catalyzed hydrolysis/synthesis of a mixture of peptides: product diversity and ligand amplification by a molecular trap », Biopolymers, vol. 40, no 6, , p. 617–625 (PMID 9140201, DOI 10.1002/(sici)1097-0282(1996)40:6<617::aid-bip3>3.0.co;2-z)
- Lins, R. J., Flitsch, S. L., Turner, N. J. et Irving, E., « Enzymatic generation and in situ screening of a dynamic combinatorial library of sialic acid analogues », Angew. Chem. Int. Ed., vol. 41, no 18, , p. 3405–3407 (PMID 12298046, DOI 10.1002/1521-3773(20020916)41:18<3405::AID-ANIE3405>3.0.CO;2-P)
- Lins, R. J., Flitsch, S. L., Turner, N. J. et Irving, E., « Generation of a dynamic combinatorial library using sialic acid aldolase and in situ screening against wheat germ agglutinin », Tetrahedron, vol. 60, no 3, , p. 771–780 (DOI 10.1016/j.tet.2003.11.062)
- Valade, A., Urban, D. et Beau, J.-M., « Two galatosyltransferases' selection of different binders from the same uridine-based dynamic combinatorial library », J. Comb. Chem., vol. 9, no 1, jan–feb 2007, p. 1–4 (PMID 17206823, DOI 10.1021/cc060033w)
- Das, M., Tianming, Y., Jinghua, D. et Prasetya, F., « Multi-Protein Dynamic Combinatorial Chemistry: A Novel Strategy that Leads to Simultaneous Discovery of Subfamily-Selective Inhibitors for Nucleic Acid Demethylases FTO and ALKBH3 », Chem. Asian J., vol. 13, no 19, , p. 2854–2867 (PMID 29917331, DOI 10.1002/asia.201800729)
- Herrmann, A., « Dynamic Mixtures: Challenges and Opportunities for the Amplification and Sensing of Scents », Chem. Eur. J., vol. 18, no 28, , p. 8568–8577 (PMID 22588709, DOI 10.1002/chem.201200668)
- (en) Chandru, Guttenberg, Giri et Hongo, « Simple prebiotic synthesis of high diversity dynamic combinatorial polyester libraries », Communications Chemistry, vol. 1, no 1, (ISSN 2399-3669, DOI 10.1038/s42004-018-0031-1)