Triéthanolamine
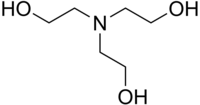
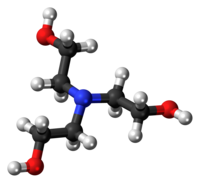
La triéthanolamine est aussi connue sous le nom de trolamine, ou le nom systématique 2,2',2-nitrilotriéthanol. Sa formule brute est C6H15NO3.
| Triéthanolamine | |
  |
|
| Identification | |
|---|---|
| Synonymes |
2,2',2-nitrilotriéthanol, |
| No CAS | |
| No ECHA | 100.002.773 |
| No CE | 203-049-8 |
| Code ATC | |
| SMILES | |
| InChI | |
| Apparence | Liquide hygroscopique incolore visqueux ou cristaux d'odeur caractéristique[1]. |
| Propriétés chimiques | |
| Formule | C6H15NO3 [Isomères] |
| Masse molaire[3] | 149,188 2 ± 0,007 g/mol C 48,3 %, H 10,13 %, N 9,39 %, O 32,17 %, |
| Moment dipolaire | 3,57 D[2] |
| Diamètre moléculaire | 0,674 nm[2] |
| Propriétés physiques | |
| T° fusion | 21,6 °C[1] |
| T° ébullition | 335,4 °C[1] |
| Paramètre de solubilité δ | 21,6 J1/2 cm−3/2 (30 °C)[2] |
| Miscibilité | dans l'eau : miscible[1] |
| Masse volumique | 1,124 2 g cm−3[4] |
| T° d'auto-inflammation | 324 °C[1] |
| Point d’éclair | 179 °C[1] |
| Limites d’explosivité dans l’air | 3,6–7,2 %vol[1] |
| Pression de vapeur saturante | 0,01 hPa (20 °C)[réf. souhaitée] |
| Thermochimie | |
| Cp | |
| Propriétés optiques | |
| Indice de réfraction | 1,483[2] |
| Précautions | |
| SIMDUT[7] | |
Produit non contrôlé |
|
| NFPA 704 | |
| Classification du CIRC | |
| Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[6] | |
| Écotoxicologie | |
| LogP | –2,3[1] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Il s'agit d'un composé organique qui est une amine tertiaire et un triol. Comme d'autres amines, la triéthanolamine agit en tant que base faible due à la seule paire d'électrons sur l'atome d'azote.
Brûlures
modifierLa trolamine est le principe actif de la Biafine, crème utilisée contre les brûlures et les plaies superficielles. D'après la Banque de données automatisée sur les médicaments[8], la trolamine a un effet analgésique en association avec de l'aspirine. C'est aussi un émulsifiant.
Cosmétique
modifierCet ingrédient est employé comme compensateur de pH dans des préparations cosmétiques pour une vaste gamme de produits — lotion pour la peau, gels pour les yeux, crèmes hydratantes, shampoings, crème dépilatoire, mousse à raser, etc. La triéthanolamine est un allergène reconnu, à pouvoir allergisant modéré.
Comme toutes les amines, elle peut créer des nitrosamines, mais ceci demeure peu probable avec les basses concentrations utilisées dans les produits cosmétiques. L'efficacité des crèmes antiride repose sur la pénétration du produit dans les couches profondes de la peau, mais certains contestent cette capacité de pénétration. Il n'y a pas d'étude gouvernementale sur l'innocuité de la triéthylamine[Quoi ?] sur la peau à long terme. Les seules études qui existent ont été produites par les compagnies pharmaceutiques elles-mêmes[9]. Les nitrosamines sont considérées comme cancérigènes. Le manque de données sur ce produit[Lequel ?] empêche d'évaluer de façon adéquate son effet mutagène.
Elle est énumérée sous le programme 3, partie B, de la convention chimique sur les armes car elle peut être employée dans la fabrication du gaz moutarde.
Risques
modifierLa triéthanolamine est inflammable. Le feu qui en résulte peut être éteint avec du dioxyde de carbone, de la mousse, de la poudre chimique sèche ou de la mousse d'alcool ; il ne faut jamais utiliser d'eau pulvérisée car elle pourrait provoquer la formation d'écume. De plus, il faut éviter d'utiliser de la mousse pulvérisée sur un bassin chaud en flamme.
La triéthanolamine est incompatible avec les acides ainsi qu'avec les oxydants forts tels que l'ozone et l'oxygène liquide.
L'exposition à la triéthanolamine ou à ses vapeurs pourrait engendrer l'irritation de la peau, des yeux et des voies respiratoires. Une exposition répétée ou prolongée à ce produit peut avoir une action dégraissante sur la peau. Il peut aussi causer des rougeurs, des gerçures et de la desquamation.
Notes et références
modifier- TRIETHANOLAMINE, Fiches internationales de sécurité chimique
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, Angleterre, John Wiley & Sons, , 239 p. (ISBN 978-0-471-98369-9, LCCN 98018212).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) J. G. Speight et Norbert Adolph Lange, Lange's Handbook of Chemistry, New York, McGraw-Hill, , 16e éd., 1623 p. (ISBN 978-0-07-143220-7, LCCN 84643191), p. 2.289.
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams : Organic Compounds C8 to C28, vol. 2, Huston, Texas, Gulf Pub. Co., , 396 p. (ISBN 978-0-88415-858-5, LCCN 96036328).
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Évaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme », sur monographs.iarc.fr, CIRC, (consulté le ).
- « Triéthanolamine » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009.
- www.biam2.org/www/Sub2163.html
- Archives - La facture, Radio-Canada.ca.




