Disilyne
Le disilyne est un composé chimique de formule semi-développée HSi≡SiH. C'est le plus simple des hydrures de silicium insaturés, possédant une triple liaison –Si≡Si–, analogue structurel silicié de l'acétylène HC≡CH.
| Disilyne | |
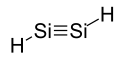
| |
| Structure du disilyne soulignant en particulier la configuration trans de la triple liaison. | |
| Identification | |
|---|---|
| No CAS | |
| PubChem | 71420045 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | Si2H2 |
| Masse molaire[1] | 58,186 9 ± 0,000 7 g/mol H 3,46 %, Si 96,54 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Par extension, les disilynes constituent une classe de molécules issues de la substitution des atomes d'hydrogène du disilyne par des résidus carbonés. Si ce terme désigne généralement des composés comportant une triple liaison silicium≡silicium[2], il peut également désigner des composés comportant une triple liaison silicium≡carbone[3].
À l'instar des disilènes, qui sont plus stables que le disilène H2Si=SiH2, certains disilynes sont suffisamment stables pour avoir pu être synthétisés et caractérisés.
-
Structure du premier disilyne publié[4].
Le premier disilyne à avoir été publié, en 2004[4], est un composé de structure R12R2Si–Si2–SiR2R12, avec R1 = HC(Si(CH3)3)2 et R2 = –CH(CH3)2. Il a été obtenu par réduction du précurseur tétrabromé à l'aide de potassium-graphite. Il s'agit d'un composé cristallin vert émeraude sensible à l'humidité et à l'air, qui se décompose en fondant à partir de 128 °C, dans lequel la cristallographie aux rayons X a permis d'identifier que les quatre atomes de silicium centraux ne sont pas alignés mais adoptent une configuration trans avec un angle –Si≡Si–Si– de 137°. La triple liaison Si≡Si a une longueur de 206 pm — environ 4 % de moins qu'une double liaison Si=Si — tandis que les liaisons simples Si–Si ont une longueur de 237 pm.
Les calculs prédisent un ordre de liaison de 2,6. Un autre mode de calcul de l'ordre de liaison montre que celle-ci ferait intervenir deux paires d'électrons, avec une troisième paire dans une orbitale non liante[5],[6],[7].
Notes et références
modifier- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Egon Wiberg, Arnold Frederick Holleman, Inorganic Chemistry, Elsevier, 2001. (ISBN 0-12-352651-5)
- (en) Miriam Karni et Yitzhak Apeloig, « The quest for a stable silyne, RSi ≡ CR′. The effect of bulky substituents », Silicon Chemistry, vol. 1, , p. 59-65 (DOI 10.1023/A:1016091614005, lire en ligne)
- (en) Akira Sekiguchi, Rei Kinjo et Masaaki Ichinohe, « A Stable Compound Containing a Silicon-Silicon Triple Bond », Science, vol. 305, no 5691, , p. 1755-1757 (lire en ligne) DOI 10.1126/science.1102209
- (en) Carlo A. Pignedoli, Alessandro Curioni et Wanda Andreoni, « Disproving a Silicon Analog of an Alkyne with the Aid of Topological Analyses of the Electronic Structure and Ab Initio Molecular Dynamics Calculations », ChemPhysChem, vol. 6, no 9, , p. 1795-1799 (PMID 16144004, DOI 10.1002/cphc.200500064, lire en ligne)
- (en) Gernot Frenking, Andreas Krapp, Shigeru Nagase, Nozomi Takagi et Akira Sekiguchi, « Comment on “Disproving a Silicon Analog of an Alkyne with the Aid of Topological Analyses of the Electronic Structure and Ab Initio Molecular Dynamics Calculations” », ChemPhysChem, vol. 7, no 4, , p. 799-800 (PMID 16596606, DOI 10.1002/cphc.200500689, lire en ligne)
- (en) Carlo A. Pignedoli, Alessandro Curioni et Wanda Andreoni, « Reply to Comment on “Disproving a Silicon Analog of an Alkyne with the Aid of Topological Analyses of the Electronic Structure and Ab Initio Molecular Dynamics Calculations” », ChemPhysChem, vol. 7, no 4, , p. 801-802 (DOI 10.1002/cphc.200600025, lire en ligne)
![Structure du premier disilyne publié[4].](http://upload.wikimedia.org/wikipedia/commons/thumb/e/ef/Sekiguchi-silyne-from-xtal-3D-balls.png/351px-Sekiguchi-silyne-from-xtal-3D-balls.png)