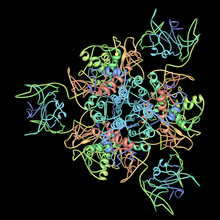
Aspartate carbamyltransférase
L'aspartate carbamyltransférase est une transférase qui catalyse la réaction :
| N° EC | EC |
|---|---|
| N° CAS |
| IUBMB | Entrée IUBMB |
|---|---|
| IntEnz | Vue IntEnz |
| BRENDA | Entrée BRENDA |
| KEGG | Entrée KEGG |
| MetaCyc | Voie métabolique |
| PRIAM | Profil |
| PDB | RCSB PDB PDBe PDBj PDBsum |
| GO | AmiGO / EGO |
Cette enzyme intervient à la première étape de la biosynthèse des pyrimidines[2].
Chez Escherichia coli, l'aspartate carbamyltransférase est constituée de 12 sous-unités ayant une masse totale de 300 kDa[3] : six sous-unités catalytiques C de 34 kDa et six sous-unités régulatrices R de 17 kDa. Ce complexe C6R6 est organisé en deux trimères catalytiques C3 et trois dimères régulateurs R2. L'agencement de ces sous-unités permet à cette enzyme de présenter une très forte régulation allostérique par rapport à ses substrats[4].
Cette enzyme, qui ne suit pas la cinétique de Michaelis-Menten, offre un exemple de régulation allostérique à l'étape initiale d'une voie métabolique. Elle bascule entre, d'une part, un état tendu T à faible affinité pour les substrats et faible activité enzymatique et, d'autre part, l'état relâché R à affinité et activité élevées. La liaison des substrats aux sous-unités catalytiques déplace l'équilibre vers l'état R, tandis que la liaison du CTP aux sous-unités régulatrices déplace l'équilibre vers l'état T. La liaison d'ATP aux sous-unités régulatrices déplace en revanche l'équilibre vers l'état R.
Notes et références
modifier- (en) Richard B. Honzatko, James L. Crawford, Hugo L. Monaco, Jane E. Ladner, Brian F.P. Ewards, David R. Evans, Stephen G. Warren, Don C. Wiley, Robert C. Ladner et William N. Lipscomb, « Crystal and molecular structures of native and CTP-liganded aspartate carbamoyltransferase from Escherichia coli », Journal of Molecular Biology, vol. 160, no 2, , p. 219-263 (PMID 6757446, DOI 10.1016/0022-2836(82)90175-9, lire en ligne)
- (en) J. P. Simmer, R. E. Kelly, A. G. Rinker, Jr, B. H. Zimmermann, J. L. Scully, H. Kim et D. R. Evans, « Mammalian dihydroorotase: nucleotide sequence, peptide sequences, and evolution of the dihydroorotase domain of the multifunctional protein CAD », Proceedings of the National Academy of Sciences of the United States of America, vol. 87, no 1, , p. 174-178 (PMID 1967494, PMCID 53223, DOI 10.1073/pnas.87.1.174, lire en ligne)
- (en) Christine P. Macol Hiro Tsuruta Boguslaw Stec et Evan R. Kantrowitz, « Direct structural evidence for a concerted allosteric transition in Escherichia coli aspartate transcarbamoylase », Nature Structural Biology, vol. 8, no 5, , p. 423-426 (PMID 11323717, DOI 10.1038/87582, lire en ligne)
- (en) Kerstin Helmstaedt, Sven Krappmann et Gerhard H. Braus, « Allosteric Regulation of Catalytic Activity: Escherichia coli Aspartate Transcarbamoylase versus Yeast Chorismate Mutase », Microbiology and Molecular Biology Reviews, vol. 65, no 3, , p. 404-421 (PMID 11528003, PMCID 99034, DOI 10.1128/MMBR.65.3.404-421.2001, lire en ligne)