alpha-PVP
| α-PVP | ||
| ||
 | ||
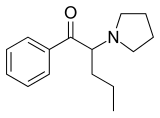
| Structure de l'α-PVP | ||
| Identification | ||
|---|---|---|
| Nom UICPA | (RS)-1-phényl-2-(1-pyrrolidinyl)-1-pentanone | |
| Synonymes |
A-PVP, a-PVP, APVP |
|
| No CAS | ||
| PubChem | 11148955 | |
| SMILES | ||
| InChI | ||
| Propriétés chimiques | ||
| Formule | C15H21NO |
|
| Masse molaire[1] | 231,333 3 ± 0,014 g/mol C 77,88 %, H 9,15 %, N 6,05 %, O 6,92 %, |
|
| Écotoxicologie | ||
| DL50 | 38.5 mg/kg (souris, IV)[2] | |
| Caractère psychotrope | ||
| Catégorie | Stimulant | |
| Mode de consommation |
IV, per-os (voie orale), insufflation (sniff) |
|
| Autres dénominations |
flakka |
|
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
L'alpha-PVP (alpha-pyrrolidinovalérophénone) est la plus puissante drogue psychostimulante de la famille des cathinones. C'est un analogue déméthylé de la pyrovalérone.
Elle a été préparée et fit l'objet de recherches pour la première fois dans les années 1960 et est, depuis, restée inconnue jusqu'à ce qu'elle apparaisse comme drogue de synthèse à partir des années 2010 sous le nom de Flakka, provoquant une vague de crises psychotiques et d'accidents[3], très médiatisés.
Elle provoque de l'hypertension, de la tachycardie, une stimulation intellectuelle et physique, de l'anxiété et à forte dose induit une forte modification du comportement.
Chimie modifier
La 1-phényl-2-(1-pyrrolidinyl)-1-pentanone est une cathinone et est l'analogue déméthylé de la pyrovalérone, ancien médicament dorénavant classé comme stupéfiant. La présence d'un carbone asymétrique en position 3 conduit à la formation de deux isomères R et S.
L'α-PVP et son sel chlorhydrate se présentent sous la forme d'une poudre blanche, cristalline, soluble dans le PBS, l'éthanol et le DMF.
Elle est synthétisée à partir de la valérophénone en deux étapes.
Pharmacologie modifier
Les données pharmacologiques concernant l'α-PVP sont peu nombreuses et portent principalement sur des modèles animaux.
Pharmacocinétique modifier
L'alpha-PVP semble posséder une bonne biodisponibilité orale et provoquer des effets psychotropes plus rapidement que la méthamphétamine[4]. Elle semble être métabolisée par le foie, par des enzymes de la famille des cytochromes P450, les CYP 2B6, 2D6, 2C19, 3A4, ce qui produit une dizaine de métabolites, principalement par 2-hydroxylation, déshydrogénation ou rupture du cycle pyrrolidine[5].
Pharmacodynamie modifier
L'alpha-PVP est un stimulant puissant du système nerveux central, ce qui est dû à son action sur la noradrénaline, la dopamine, et sur la sérotonine.
Elle agit sur les transporteurs NET et DAT des catécholamines comme la noradrénaline ou la dopamine[6], comme un agoniste des récepteurs D1 et D2 de la dopamine[7], des récepteurs à la noradrénaline mais se comporte également comme un inhibiteur sélectif de la recapture des catécholamines[8],[9].
En agissant sur les récepteurs à la dopamine et sur la phosphorylation de la protéine CERB dans le noyau accumbens, l'α-PVP stimule le circuit de récompense chez le rat[10].
À l'instar de la cocaïne, des amphétamines ou des autres cathinones, l'α-PVP agirait comme un catécholaminergique et comme un sérotoninergique, ce qui produit une cascade d'effets sympathicomimétiques.
L'α-PVP se lie aux transporteurs SERT de la sérotonine et agit in-vitro comme agoniste de ses récepteurs 5-HT1A (Ki= 5,2 μM)[11].
Elle produit des effets stimulants dose-dépendants chimiquement plus similaires à ceux de la MDPV ou de la cocaïne[6] qu'à ceux de l'amphétamine[12].
En suit une vasoconstriction, une hausse de la pression artérielle, une tachycardie et, à fortes doses, des comportements paradoxaux, étranges, agressifs voire violents.
Ont été remarqués des anomalies de l'équilibre acido-basique, des troubles de la coagulation (pouvant mener à des accidents vasculaires cérébraux), un taux plasmatique de créatinine phosphokinase (CPK) élevé, souvent due à une activité musculaire intense, et à une élévation du taux de lactates[13].
Peuvent se produire :
- gesticulation et mouvements désordonnés[14] ;
- paranoïa, psychose, hallucinations[15] ;
- hyperthermie (fièvre).
Plusieurs cas de morts dues à l'alpha-PVP ont déjà été répertoriés[16],[17].
Références modifier
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Seeger E. Verfahren zur Herstellung von α - Pyrrolidinoketonen und deren Salzen. Patent No. DE 1161274. Dr. Karl Thomae GmbH, Biberach an der Riss, Germany, 1964
- Trista Haupt Wright et Chad Harris, « Twenty-One Cases Involving Alpha-Pyrrolidinovalerophenone (α-PVP) », Journal of Analytical Toxicology, vol. 40, no 5, , p. 396–402 (ISSN 1945-2403, PMID 27185821, DOI 10.1093/jat/bkw029, lire en ligne, consulté le )
- Julie A. Marusich, Timothy W. Lefever, Bruce E. Blough et Brian F. Thomas, « Pharmacological effects of methamphetamine and alpha-PVP vapor and injection », Neurotoxicology, vol. 55, , p. 83–91 (ISSN 1872-9711, PMID 27237056, PMCID PMC4949132, DOI 10.1016/j.neuro.2016.05.015, lire en ligne, consulté le )
- Christoph Sauer, Frank T. Peters, Claudia Haas et Markus R. Meyer, « New designer drug alpha-pyrrolidinovalerophenone (PVP): studies on its metabolism and toxicological detection in rat urine using gas chromatographic/mass spectrometric techniques », Journal of Mass Spectrometry: JMS, vol. 44, no 6, , p. 952–964 (ISSN 1096-9888, PMID 19241365, DOI 10.1002/jms.1571, lire en ligne, consulté le )
- Douglas A. Smith, S. Stevens Negus, Justin L. Poklis et Bruce E. Blough, « Cocaine-like discriminative stimulus effects of alpha-pyrrolidinovalerophenone, methcathinone and their 3,4-methylenedioxy or 4-methyl analogs in rhesus monkeys », Addiction Biology, vol. 22, no 5, , p. 1169–1178 (ISSN 1369-1600, PMID 27060605, DOI 10.1111/adb.12399, lire en ligne, consulté le )
- Asuka Kaizaki, Sachiko Tanaka et Satoshi Numazawa, « New recreational drug 1-phenyl-2-(1-pyrrolidinyl)-1-pentanone (alpha-PVP) activates central nervous system via dopaminergic neuron », The Journal of Toxicological Sciences, vol. 39, no 1, , p. 1–6 (ISSN 1880-3989, PMID 24418703, lire en ligne, consulté le )
- Madras BK, Meltzer PC, Butler D. Madras BK, Meltzer PC et Butler D (2005), Pyrovalerone analogs and therapeutic uses thereof, brevet no WO 2005/034878 A2, President and Fellows of Harvard College, États-Unis, Organix, Inc., 2005.
- (en) Meltzer PC, Butler D, Deschamps JR et Madras BK, « 1-(4-Methylphenyl)-2-pyrrolidin-1-ylpentan-1-one (pyrovalerone ) analogs: a promising class of monoamine uptake inhibitors », J. Med. Chem., (PMID 16480278, DOI 10.1021/jm050797a, lire en ligne)
- Kyoko Hataoka, Asuka Kaizaki-Mitsumoto et Satoshi Numazawa, « Alpha-PVP induces the rewarding effect via activating dopaminergic neuron », The Journal of Toxicological Sciences, vol. 42, no 5, , p. 539–543 (ISSN 1880-3989, PMID 28904288, DOI 10.2131/jts.42.539, lire en ligne, consulté le )
- Julie A. Marusich, Kateland R. Antonazzo, Jenny L. Wiley et Bruce E. Blough, « Pharmacology of novel synthetic stimulants structurally related to the bath salts constituent 3,4-methylenedioxypyrovalerone (MDPV) », Neuropharmacology, vol. 87, , p. 206–213 (ISSN 1873-7064, PMID 24594476, PMCID PMC4152390, DOI 10.1016/j.neuropharm.2014.02.016, lire en ligne, consulté le )
- (en) WHO, « 1-Phenyl-2-(pyrrolidin-1-yl)pentan-1-one (α-PVP) », Bulletin de l'OMS - Comité d'expertise sur l'abus des drogues, 16-20 novembre 2015, p. 11 (lire en ligne)
- Rimako Umebachi, Hiromichi Aoki, Mariko Sugita et Takayuki Taira, « Clinical characteristics of α-pyrrolidinovalerophenone (α-PVP) poisoning », Clinical Toxicology (Philadelphia, Pa.), vol. 54, no 7, , p. 563–567 (ISSN 1556-9519, PMID 27227375, DOI 10.3109/15563650.2016.1166508, lire en ligne, consulté le )
- Video Ditore, « New DRUG called Flakka, zombie live on streets », (consulté le )
- Reynaldo Kalachian, « Flakka drug effects! », (consulté le )
- « Flakka, la nouvelle drogue qui fait des ravages aux États-Unis », sur SudOuest.fr (consulté le )
- « Flakka : la nouvelle drogue venue des États-Unis qui déferle sur la France », sur Atlantico.fr (consulté le )