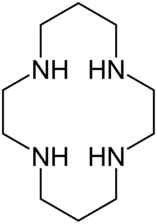
Éther azacouronne
Un éther azacouronne, azaéther couronne ou éther couronne aza, est un composé chimique analogue à un éther couronne dont les atomes d'oxygène formant les liaisons éther sont remplacés par des atomes d'azote formant des fonctions amine, d'où le préfixe aza[1],[2]. Par exemple, aux éthers couronnes de formule générale (CH2CH2O)n correspondent des éthers azacouronnes de formule générale (CH2CH2NH)n, où n = 3, 4, 5 ou 6. Le 1,4,7-triazacyclononane (n = 3), le cyclène[3] (n = 4) et l'hexaaza-18-couronne-6 (en)[4] (n = 6) ont été particulièrement étudiés.
Synthèse
modifierLa synthèse des éthers azacouronnes rencontre les difficultés associées à la production des macrocycles[5]. Le cycle à 18 atomes du (CH2CH2NH)6 (en) peut être produit en combinant deux triamines[4]. En réagissant avec le chlorure de tosyle, la diéthylènetriamine donne un dérivé portant deux groupes sulfonamides secondaires. Ces composés peuvent être utilisés comme synthons pour la macrocyclisation.
Variétés
modifierIl existe de nombreux types d'éthers azacouronnes :
- les éthers azacouronnes ont souvent des ponts éthylène (CH2)2 triméthylène (CH2)3. Le cyclame (en) (1,4,8,11-tétraazacyclotétradécane) contient les deux ;
- les éthers azacouronnes peuvent contenir des amines tertiaires. Par exemple, le 1,4,7-triméthyl-1,4,7-triazacyclononane ne contient que des amines tertiaires. Les cryptands, qui sont intermédiaires tridimensionnels entre éthers couronnes et éthers azacouronnes, contiennent deux amines tertiaires ;
- certains macrocycles contiennent à la fois des fonctions éther et des amines[6]. C'est par exemple le cas de l'éther diaza-18-couronne-6 [(CH2CH2O)2(CH2CH2NH)]2[7] ;
- les amines tertiaires permettent des configurations « en lasso » augmentant les capacités de complexation de ces composés[8].
Notes et références
modifier- (en) Andrea Bencini, Antonio Bianchi, Enrique Garcia-España, Mauro Micheloni et José Antonio Ramirez, « Proton coordination by polyamine compounds in aqueous solution », Coordination Chemistry Reviews, vol. 1, no 188, , p. 97-156 (DOI 10.1016/S0010-8545(98)00243-4, lire en ligne)
- (en) Roland Reichenbach-Klinke et Burkhard König, « Metal complexes of azacrown ethers in molecular recognition and catalysis », Journal of the Chemical Society, Dalton Transactions, no 2, , p. 121-130 (DOI 10.1039/b106367g, lire en ligne)
- (en) David P. Reed et Gary R. Weisman, « 1,4,7,10-Tatraazacyclododecane », Organic Syntheses, vol. 78, , p. 73 (DOI 10.15227/orgsyn.078.0073, lire en ligne)
- (en) T. J. Atkins1, J. E. Richman et W. F. Oettle, « Macrocyclic Polyamines: 1,4,7,10,13,16-Hexaäzacycloöctadecane », Organic Syntheses, vol. 58, , p. 86 (DOI 10.15227/orgsyn.058.0086, lire en ligne)
- (en) Krzysztof E. Krakowiak, Jerald S. Bradshaw et Daria J. Zamecka-Krakowiak, « Synthesis of aza-crown ethers », Chemical Reviews, vol. 89, no 4, , p. 929-972 (DOI 10.1021/cr00094a008, lire en ligne)
- (en) Hans K. Frensdorff, « Stability constants of cyclic polyether complexes with univalent cations », Journal of the American Chemical Society, vol. 93, no 3, , p. 600-606 (DOI 10.1021/ja00732a007, lire en ligne)
- (en) Vincent J. Gatto, Steven R. Miller et George W. Gokel, « 4,13-Diaza-18-Crown-6 », Organic Syntheses, vol. 68, , p. 227 (DOI 10.15227/orgsyn.068.0227, lire en ligne)
- (en) George W. Gokel, Leonard J. Barbour, Riccardo Ferdani et Jiaxin Hu, « Lariat Ether Receptor Systems Show Experimental Evidence for Alkali Metal Cation−π Interactions », Accounts of Chemical Research, vol. 35, no 10, , p. 878-886 (PMID 12379140, DOI 10.1021/ar000093p, lire en ligne)