Procédé des chambres de plomb
Le procédé des chambres de plomb a été la première méthode industrielle de production d'acide sulfurique en grande quantité. Ce procédé a été mis au point au milieu du XVIIIe siècle en Angleterre et a été le principal mode de fabrication de l'acide sulfurique pendant deux siècles[3]. Il a été remplacé par le procédé contact, plus efficace et moins polluant.

(A, B) fours à rôtir pour pyrite,
(C) four à salpêtre avec 2 bols pour acide sulfurique et salpêtre pour libérer les gaz nitreux,
(D) tour « Glover »,
(E,F,G) chambres à plomb,
(H) la tour « Gay-Lussac »[1].
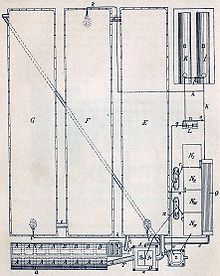
(I, K) chaudière à vapeur,
(L) pompe à air comprimé,
(M) récipient sous pression,
(N) récipient pour acide « Glover »,
(O) refroidisseur à tube[2].
Le principe consiste à oxyder le dioxyde de soufre par un oxydant plus fort que le dioxygène, en l’occurrence des oxydes d'azote.
Principe
modifierPour fabriquer de l'acide sulfurique, il faut du trioxyde de soufre SO3 que l'on mélange à de l'eau pour faire un oléum, c'est-à-dire de l'acide sulfurique concentrée saturée en SO3. Le point de départ est en général du soufre élémentaire ou plus rarement un composé soufré, on peut opérer la combustion de ce soufre avec du dioxygène. Mais comme la réaction de combustion se fait à haute température, on obtient du dioxyde de soufre SO2, molécule stable à haute température.
Il faut oxyder le dioxyde de soufre en trioxyde de soufre, si on utilise le dioxygène :
- (R1) SO2 + 0,5 O2 SO3.
Cette réaction n'est pas favorable dans le sens direct à haute température, mais si on reste à basse température, la vitesse de réaction devient tellement lente qu'elle n'est plus réalisable industriellement.
Le principe du procédé des chambres de plomb était d'utiliser un oxydant plus fort que le dioxygène, comme par exemple NO2 :
- (R2) SO2 + NO2 SO3 + NO.
La clé du procédé est que NO peut être séparé et recyclé puisqu'il s'oxyde spontanément en NO2 à température ambiante. Cette réactivité particulière de NO est liée au fait que c'est un radical.
- (R3) NO + 0,5 O2 → NO2
On constate que le bilan des deux réactions (R2) et (R3) correspond à la réaction (R1) et que le dioxyde d'azote est recyclé. Le mécanisme correspondant aux réactions (R2) et (R3) est dû à Berzelius.
La chimie réelle du procédé est en fait plus complexe. Le chimiste allemand Georg Lunde propose le mécanisme suivant en se basant sur le fait que NO et NO2 sont présents dans le réacteur :
- (R4) NO + NO2 → N2O3
- (R5) SO2 + H2O + N2O3 + O2 → 2 (NO)HSO4
- (R6) 2 (NO)HSO4 + H2O → H2SO4 + N2O3.
L'étape clé est la formation de l'acide nitrosylsulfurique ((NO)HSO4). D'autres réactions sont possibles mettant en jeu les différents oxydes d'azote.
Mise en œuvre
modifierLe procédé a connu de très nombreuses évolutions durant les deux siècles où il a été exploité. Il a été initialement développé par John Roebuck en 1746 à Birmingham (Grande-Bretagne). Le nom du procédé vient du fait qu'il a remplacé les bouteilles en verre utilisées jusque-là par des chambres en bois qui avaient une paroi intérieure en plomb pour être étanches et résistantes aux acides. La demande en acide sulfurique augmentait très rapidement et il devenait impossible de concevoir des réacteurs en verre suffisamment grands pour répondre à cette demande.
On injectait SO2, NO2 et de la vapeur d'eau dans le réacteur, et on pulvérisait sur ce mélange de l'eau et de l'acide sulfurique à 65 %. SO2 et NO2 passaient en solution aqueuse et l'oxydation de SO2 selon la réaction (R2) était observée au bout de trente minutes. Le monoxyde d'azote formé est très peu soluble dans l'eau, il passait dans la phase gazeuse ou il était ré-oxydé en NO2 selon la réaction (R3). On avait une boucle de recyclage du NO, l'ajout d'eau et de SO3 permettait de produire de l'acide sulfurique.
Le dioxyde de soufre venait de la combustion de soufre ou du grillage de pyrite, il était très chaud et devait être refroidi pour être transformé en SO3. Les oxydes d'azote étaient produits par attaque acide de nitrate de sodium ; après la Première Guerre mondiale, ce procédé fut remplacé par l'oxydation d'ammoniac.
Un inconvénient majeur de ce procédé était qu'une partie des oxydes d'azote était perdue avec le gaz en sortie de procédé. En 1827, Gay-Lussac conçoit une tour d'absorption des oxydes d'azote par l'acide sulfurique[4]. Dans cette tour, NO, NO2 et N2O3 réagissent avec l'acide sulfurique pour former de l'acide nitrosylsulfurique. Ceci permettait de limiter les pertes en oxyde d'azote. Il a cependant fallu attendre 1859 et l'introduction de la tour Glover, du nom de son inventeur, pour que la tour Gay-Lussac montre son efficacité. Le principe de la tour Glover est de récupérer l'acide nitrosylsulfurique liquide et de l'utiliser pour refroidir le flux gazeux chaud de SO2. Cette tour a quatre actions :
- le flux gazeux chaud de SO2 est refroidi, ce qui est nécessaire pour pouvoir se transformer en SO3 ;
- lors de ce refroidissement, de la vapeur d'eau, nécessaire pour la réaction (R5), est produite ;
- l'évaporation de l'eau permet d'obtenir de l'acide sulfurique plus concentré ;
- lors de cette concentration, les oxydes d'azote absorbés sous forme de (NO)HSO4 sont libérés et H2SO4 est produit.
Références
modifier- (de) H. Ost: Lehrbuch der Technischen Chemie, Verlag von Robert Oppenheim, Berlin, 1890, p. 53.
- (de)H. Ost: Lehrbuch der Technischen Chemie, Verlag von Robert Oppenheim, Berlin, 1890, p. 54.
- T. K. Derry et T. I. Williams, A Short History of Technology: From the Earliest Times to A.D. 1900., New York, Dover, .
- (en) M. M. Martin, Industrial Chemical Process Analysis and Design, Elsevier, , chap. 7 (« Sulfuric acid »), p. 347-404.