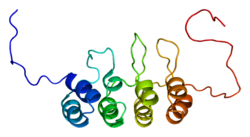p16
Le p16 est une protéine suppresseuse de tumeur également connue sous le nom d'inhibiteur de kinase cycline-dépendante 2A (CDKN2A)[5].
Mécanismes d'action
modifierElle est un inhibiteur du complexe CDK4/CDK6-Cycline D. Ce complexe phosphoryle pRB (protéine du rétinoblastome), ce qui a pour conséquence de l'empêcher de se lier au facteur de transcription E2F. Celui-ci peut alors activer la transcription de nombreux gènes favorisant le passage de la cellule de la phase G1 à la phase S.
p16 agit comme un inhibiteur de la kinase cycline-dépendante en empêchant son interaction avec la cycline D, interdisant par conséquent la progression du cycle cellulaire[6],[7]. La régulation négative de p16 peut conduire au cancer via la dérégulation de la progression du cycle cellulaire. Le gène p16 est fréquemment muté dans de nombreux cancers et une régulation négative de l'expression de p16 est associée à un risque accru de cancers[7],[8]
Gène
modifierCette protéine est codée par le gène CDKN2A situé sur le bras court du chromosome 9 (9p21.3) .
Infections virales
modifierVirus du papillome humain
modifierDans les cellules infectées par le VPH, la protéine E7 entre en compétition pour se lier aux protéines régulatrices du cycle cellulaire la protéine du rétinoblastome , entraînant la libération d'E2F1 de pRb et l'activation du cycle cellulaire[7],[9] La perturbation de la voie pRb-E2F1 par E7 induit la surexpression et l'accumulation de p16 dans les cellules à travers une boucle de rétroaction négative[10],[7]. L'expression cytoplasmique et nucléaire forte et diffuse de p16 dans les carcinomes épidermoïdes cervicaux est principalement associée à une infection par HR-HPV. Par conséquent, p16 est considéré comme un marqueur de substitution de l'infection persistante par le HR-HPV et une surexpression de p16 a été observée dans la majorité des précancers cervicaux et des cancers[11],[12],[7]
Notes et références
modifier- GRCh38: Ensembl release 89: ENSG00000147889 - Ensembl, May 2017
- GRCm38: Ensembl release 89: ENSMUSG00000044303 - Ensembl, May 2017
- « Publications PubMed pour l'Homme », sur National Center for Biotechnology Information, U.S. National Library of Medicine
- « Publications PubMed pour la Souris », sur National Center for Biotechnology Information, U.S. National Library of Medicine
- Serrano M, Hannon GJ, Beach D. A new regulatory motif in cell-cycle control causing specific inhibition of cyclin D/CDK4. Nature. 1993;366:704-7
- 24. Kalof AN, Cooper K. p16INK4a immunoexpression: surrogate marker of high-risk HPV and high-grade cervical intraepithelial neoplasia. Adv Anat Pathol. 2006;13:190-4
- (en) Li Yu, Lingyan Fei, Xubin Liu et Xufang Pi, « Application of p16/Ki-67 dual-staining cytology in cervical cancers », Journal of Cancer, vol. 10, no 12, , p. 2654–2660 (ISSN 1837-9664, PMID 31258773, PMCID PMC6584925, DOI 10.7150/jca.32743, lire en ligne, consulté le )
- 26. Leversha MA, Fielding P, Watson S, Gosney JR, Field JK. Expression of p53, pRB, and p16 in lung tumours: a validation study on tissue microarrays. J Pathol. 2003;200:610-9
- Pauck A, Lener B, Hoell M, Kaiser A, Kaufmann AM, Zwerschke W. et al. Depletion of the cdk inhibitor p16INK4a differentially affects proliferation of established cervical carcinoma cells. J Virol. 2014;88:5256-62
- Klaes R, Benner A, Friedrich T, Ridder R, Herrington S, Jenkins D. et al. p16INK4a immunohistochemistry improves interobserver agreement in the diagnosis of cervical intraepithelial neoplasia. Am J Surg Pathol. 2002;26:1389-99
- von Keyserling H, Kuhn W, Schneider A, Bergmann T, Kaufmann AM. p16INK(4)a and p14ARF mRNA expression in Pap smears is age-related. Mod Pathol. 2012;25:465-70
- Yu L, Wang L, Zhong J, Chen S. Diagnostic value of p16INK4A, Ki-67, and human papillomavirus L1 capsid protein immunochemical staining on cell blocks from residual liquid-based gynecologic cytology specimens. Cancer Cytopathol. 2010;118:47-55