Bis(trifluorométhanesulfonyl)imidure de lithium
composé chimique
Le bis(trifluorométhanesulfonyl)imidure de lithium, ou LiTSFI, est un composé chimique de formule Li+ [N(SO2CF3)2]−. Il s'agit d'un sel hydrophile très soluble dans l'eau qui peut être utilisé comme électrolyte plus sûr que l'hexafluorophosphate de lithium LiPF6[4]. Il est formé d'un cation de lithium Li+ et d'un anion bistriflimidure [N(SO2CF3)2]−.
| Bis(trifluorométhanesulfonyl)- imidure de lithium | |
| |
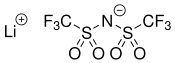
| Structure du bis(trifluorométhanesulfonyl)imidure de lithium | |
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.101.430 |
| No CE | 415-300-0 |
| PubChem | 3816071 |
| SMILES | |
| InChI | |
| Apparence | poudre blanche[1] |
| Propriétés chimiques | |
| Formule | C2F6LiNO4S2 |
| Masse molaire[2] | 287,087 ± 0,015 g/mol C 8,37 %, F 39,71 %, Li 2,42 %, N 4,88 %, O 22,29 %, S 22,34 %, |
| Propriétés physiques | |
| T° fusion | 234 à 238 °C[1] |
| Solubilité | 10 g/L[1] à 20 °C |
| Masse volumique | 1,334 g/cm3[1] à 20 °C |
| Précautions | |
| SGH[1] | |
| H314, H373, H412, P273, P280, P301+P330+P331, P302+P352, P305+P351+P338 et P308+P310 |
|
| NFPA 704[3] | |
| Transport[1] | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Sa très bonne solubilité dans l'eau fait du LiTFSI un sel de lithium utilisé comme électrolyte en solution aqueuse pour accumulateurs lithium-ion aqueux (en)[5],[6].
Notes et références
modifier- Entrée « Lithium bis(trifluoromethylsulfonyl)imide » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 6 novembre 2022 (JavaScript nécessaire)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « Fiche du composé Lithium bis(trifluoromethylsulfonyl)imide, 98+% », sur Alfa Aesar (consulté le ).
- (en) Julian Kalhoff, Dominic Bresser, Marco Bolloli, Fannie Alloin, Jean-Yves Sanchez et Stefano Passerini, « Enabling LiTFSI-based Electrolytes for Safer Lithium-Ion Batteries by Using Linear Fluorinated Carbonates as (Co)Solvent », ChemSusChem, vol. 7, no 10, , p. 2939-2946 (PMID 25138922, DOI 10.1002/cssc.201402502, lire en ligne).
- (en) Liumin Suo, Oleg Borodin, Tao Gao, Marco Olguin, Janet Ho, Xiulin Fan, Chao Luo, Chunsheng Wang et Kang Xu, « “Water-in-salt” electrolyte enables high-voltage aqueous lithium-ion chemistries », Science, vol. 350, no 6263, , p. 938-943 (PMID 26586759, DOI 10.1126/science.aab1595, S2CID 206637574, lire en ligne).
- (en) Leland Smith et Bruce Dunn, « Opening the window for aqueous electrolytes », Science, vol. 350, no 6263, , p. 918 (PMID 26586752, DOI 10.1126/science.aad5575, S2CID 206643843, lire en ligne).





