Syringine
| Syringine | |
| |
| Identification | |
|---|---|
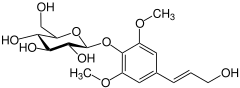
| Nom systématique | 4-[(1E)-3-hydroxyprop-1-én-1-yl]-2,6-diméthoxyphényl β-D-glucopyranoside |
| Synonymes |
éleuthéroside B, lilacine, iléxanthine A, ligustrine, magnolénine, méthoxyconiférine, syringoside |
| No CAS | |
| No ECHA | 100.120.487 |
| PubChem | 5316860 |
| ChEBI | 9380 |
| SMILES | |
| InChI | |
| Apparence | cristaux incolores, en forme d'aiguille[1] |
| Propriétés chimiques | |
| Formule | C17H24O9 |
| Masse molaire[2] | 372,367 1 ± 0,018 g/mol C 54,83 %, H 6,5 %, O 38,67 %, |
| Propriétés physiques | |
| T° fusion | 192 °C[1] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
La syringine est un composé phytochimique isolé pour la première fois de l'écorce du lilas commun (Syringa vulgaris)[1],[3]. Dérivée de l'alcool sinapylique, l'un des principaux monolignols, elle est présente dans un grand nombre de plantes où elle joue le rôle de métabolite.
Histoire, noms et occurrence naturelle modifier
Le chimiste allemand Alphons Meillet a isolé la substance de l'écorce du lilas commun en 1841 et l'a nommée « lilacine », en référence à la couleur violette des fleurs[4],[5]. Franz J. Bernays a isolé la substance des feuilles et des branches vertes de la même plante et l'a nommée « syringine », en référence au nom latin (Syringa vulgaris)[6],[7].
Elle est présente dans un grand nombre d'autres plantes, et en a souvent reçu des noms en rapport. Elle est par exemple présente dans les racines du ginseng de Sibérie (Eleutherococcus senticosus) et fait partie de la famille de substances appelées « éleuthérosides ». À ce titre elle est parfois désignée sous le nom d'« éleuthéroside B ». Elle est également connue sous le nom d'« iléxanthine A » pour sa présence dans le houx (Ilex aquifolium), « ligustrine » pour sa présence dans l'écorce des troènes (Ligustrum) ou encore « magnolénine » pour sa présence dans les magnolias.
On la trouve également dans les racines du pissenlit, et donc dans le café de pissenlit[8].
Du fait de sa structure identique à un groupe méthoxyle près, elle est enfin parfois appelée aussi méthoxyconiférine
Propriétés modifier
La syringine se présente sous la forme de cristaux incolores en forme d'aiguilles qui fondent vers 192 °C[1]. Chimiquement, elle est constituée d'une molécule d'alcool sinapylique lié par une liaison osidique à une molécule de glucose en position C4. C'est donc un glucoside, appartenant à la famille des hétérosides de phénylpropanoïde. Elle est structurellement proche et a donné son nom au syringol, au syringalcool, au syringaldéhyde, à l'acide syringique ou encore à l'acétosyringone.
Elle a un rôle d'agent hépatoprotecteur[9], et pourrait avoir des effets antidiabétiques[8] ; elle a notamment permis de réduire la concentration de glucose dans le sang des rats chez qui on avait provoqué un diabète par injection de streptozotocine[10].
Notes et références modifier
- (de) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en allemand intitulé « Syringin » (voir la liste des auteurs).
- Merck Index, 11th Edition, 8997
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Hee-Juhn Park, Won-Tae Jung, Purusotam Basnet, Shigetoshi Kadota et Tsuneo Namba, « Syringin 4-O-β-Glucoside, a New Phenylpropanoid Glycoside, and Costunolide, a Nitric Oxide Synthase Inhibitor, from the Stem Bark of Magnolia sieboldii », Journal of Natural Products, vol. 59, no 12, , p. 1128–1130 (PMID 8988596, DOI 10.1021/np960452i)
- Alphons Meillet, « Lilacin », Justus Liebigs Annalen der Chemie, vol. 40, no 3, , p. 319–320 (DOI 10.1002/jlac.18410400342)
- Alphons Meillet, « Ueber das Lilacin, das bittre Princip der Lilas (Syringa vulgaris) », Archiv der Pharmazie, vol. 79, no 3, , p. 354–356 (DOI 10.1002/ardp.18420790312)
- Franz J. Bernays, « Ueber das Syringin », Pharmaceutisches Central Blatt, vol. 12, , p. 938–939 (lire en ligne)
- Franz J. Bernays, « Ueber einen neuen krystallisirbaren Pflanzenstoff, das Syringin aus der Syringa vulgaris », Repertorium für die Pharmacie, , p. 348–351 (lire en ligne)
- Shanmuga Sundaram Chinna Krishnan, Iyyam Pillai Subramanian et Sorimuthu Pillai Subramanian, « Isolation, characterization of syringin, phenylpropanoid glycoside from Musa paradisiaca tepal extract and evaluation of its antidiabetic effect in streptozotocin-induced diabetic rats », Biomedicine & Preventive Nutrition, vol. 4, no 2, , p. 105–111 (DOI 10.1016/j.bionut.2013.12.009)
- fiche CheBI
- Ho-Shan Niu, I-Min Liu, Juei-Tang Cheng, Che-Ling Lin, Feng-Lin Hsu, « Hypoglycemic Effect of Syringin from Eleutherococcus senticosus in Streptozotocin-Induced Diabetic Rats », Planta Medica, vol. 74, , p. 109–113 (DOI 10.1055/s-2008-1034275)