Molécule hypervalente
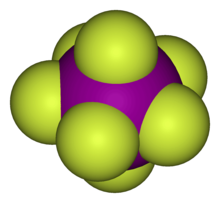
Une molécule hypervalente est une espèce chimique considérée comme comportant un atome qui, en ayant plus de huit électrons dans sa couche de valence, ne respecte pas la règle de l'octet. L'ion triiodure I3−, le trifluorure de chlore ClF3, l'ion phosphate PO43−, le pentachlorure de phosphore PCl5, l'hexafluorure de soufre SF6 ou encore l'heptafluorure d'iode IF7 sont des exemples de molécules hypervalentes. Ce concept a été introduit en 1969 par Jeremy I. Musher pour les molécules formées par les éléments des colonnes 15 à 18 dans tous leurs états d'oxydation autres que l'état le plus bas[1].
Afin de rendre compte de ces structures, des théories ont été proposées visant à aménager la règle de l'octet. Le concept de liaison à trois centres et quatre électrons a été proposé dans ce but en 1951 : il est fondé sur une orbitale liante occupée, une orbitale haute occupée non liante et une orbitale basse vacante antiliante. Ce modèle a reçu le soutien de J.I. Musher[2].
La nomenclature N-X-L, introduite en 1980[3], est souvent utilisée pour classer les composés hypervalents :
- N = nombre d'électrons de valence impliqués dans les liaisons
- X = symbole chimique de l'atome central
- L = nombre de ligands sur l'atome central
Quelques exemples :
Le terme hypervalent a été contesté par le chimiste canadien Ronald Gillespie, qui estime que « puisqu'il n'y a pas de différence fondamentale entre les liaisons de molécules hypervalentes et non hypervalentes, il n'y a pas de raison pour continuer à utiliser le terme hypervalent »[4]. Le Prof. Paul von Ragué Schleyer a suggéré de désigner ces molécules comme hypercoordonnées, afin de ne pas présupposer du type des liaisons impliquées dans leur structure.
Il a été montré que, dans les molécules hypercoordonnées avec des ligands électronégatifs telles que PF5, ces ligands tendent à dépouiller l'atome central de ses électrons de sorte que celui-ci retrouve huit électrons dans sa couche de valence, voire moins. De plus, de telles molécules à fluorure n'ont pas d'équivalent à hydrure ; ainsi, le phosphorane PH5 est une molécule instable, contrairement au pentafluorure de phosphore PF5.
Notes et références modifier
- Musher, J.L. The Chemistry of Hypervalent Molecules Angew. Chem. Int. Ed. Engl. 1969, 8, 54-68. [1]
- The Origin of the Term "Hypervalent" Jensen, William B. J. Chem. Educ. 2006 83 1751. Link
- Perkins,C. W.; Martin, J. C.; Arduengo, A. J.; Lau, W.; Alegria, A,; Kochi, J. K.; An Electrically Neutral a-Sulfuranyl Radical from the Homolysis of a Perester with Neighboring Sulfenyl Sulfur: 9-S-3 species J.Am. Chem. Soc. 1980, 102, 7753-7759 DOI 10.1021/ja00546a019
- Gillespie, R. J.; Silvi, B. The octet rule and hypervalence: two misunderstood concepts. Coord. Chem. Rev. 2002, 233-234, 53-62. [2]