Mélarsoprol
| Mélarsoprol | |
| |
| Identification | |
|---|---|
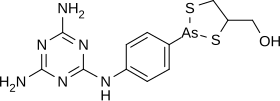
| Nom UICPA | (2-(4-((4,6-diamino-1,3,5-triazin-2-yl)amino)phenyl)-1,3,2-dithiarsolan-4-yl)methanol |
| No CAS | |
| No ECHA | 100.007.086 |
| No CE | 207-793-4 |
| Code ATC | P01 |
| PubChem | 10311 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C12H15AsN6OS2 [Isomères] |
| Masse molaire[1] | 398,339 ± 0,022 g/mol C 36,18 %, H 3,8 %, As 18,81 %, N 21,1 %, O 4,02 %, S 16,1 %, |
| Données pharmacocinétiques | |
| Demi-vie de distrib. |
35 heures[réf. souhaitée] |
| Excrétion | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le mélarsoprol (DCI) est un médicament utilisé dans le traitement de la maladie du sommeil (trypanosomiase)[3].
Historique modifier
Ce traitement a été découvert en 1949 par Ernst Friedheim (es). Malgré sa dangerosité, son utilisation était moins risquée pour le patient que les autres traitements disponibles à l'époque[4].
Indication modifier
Il n'est plus utilisé qu'en seconde ligne dans la maladie du sommeil (résistance ou intolérance aux autres traitements)[5]. Il existe également des formes résistantes à ce médicament[6].
Effets indésirables modifier
Comportant de l'arsenic, un produit toxique, le mélarsoprol est un traitement hautement dangereux qui est seulement administré par injection sous la surveillance d'un médecin. Il n'est utilisé que pour les trypanosomiases qui ont évolué vers la deuxième phase de la maladie avec des atteintes neurologiques.
Les effets indésirables du mélarsoprol sont variés, fréquents et peuvent être graves : convulsions, fièvre, pertes de conscience, éruptions cutanées, nausées et vomissements. Dans 5[7] à 9 %[8] des cas, ils entraînent la mort (encéphalopathie).
Le mélarsoprol, de surcroît, est extrêmement douloureux à l'injection, qui se fait donc la plupart du temps sous anesthésie.
Administration modifier
L'injection se fait lentement à cause de la causticité du produit, due notamment au propylène glycol utilisé comme solvant d'injection, qui peut attaquer les tissus aux alentours du site d'injection. L'administration se fait à raison de trois séries qui durent chacune trois jours consécutifs. Les injections se font à partir de seringue en verre car le composé dissout les plastiques habituellement utilisés pour les seringues. La dose journalière est de 3,6 mg·kg-1. Une période d'attente de huit à dix jours est maintenue entre chaque série.
Alternatives modifier
L'éflornithine est un traitement plus récent et beaucoup moins dangereux indiqué dans la maladie du sommeil[9]. Il peut être utilisé dans le traitement des infections à Trypanosoma brucei gambiense[10]. Il est cependant plus cher et difficilement disponible sur le marché. Son utilisation est bien sûr recommandée partout où elle est possible, et plus particulièrement dans les zones de résistance au mélarsoprol[11].
Affaire médiatique modifier
La production d'Eflornithine a été arrêtée en 1995 par Aventis car il n'était pas rentable. Néanmoins, le laboratoire a continué la production de la molécule sous forme de crème Vaniqa pour diminuer la pilosité excessive du visage chez les femmes. Cela a créé un scandale médiatique et il y a eu pression pour que la molécule soit reproduite dans le traitement des trypanosomiases. Entre 2001 et 2006, il y a eu un partenariat entre l'OMS, les ONG et le laboratoire Sanofi pour envoyer des dons d'Eflornithine dans les pays endémiques.
Divers modifier
Le mélarsoprol fait partie de la liste des médicaments essentiels de l'Organisation mondiale de la santé (liste mise à jour en )[12]. Le Mélarsoprol est utilisé dans la saison 1 épisode 7 de Docteur House pour une patiente atteinte de la maladie du Sommeil.
Notes et références modifier
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- B. Cristau, M. Placidi et P. Audibert, « Élimination biliaire chez le rat de quelques médicaments organoarséniés », dans Journal de pharmacologie, vol. 4, 1973, pp. 199-207.
- (en) Sylvie Bisser, François‐Xavier N'Siesi, Veerle Lejon, Pierre‐Marie Preux, Simon Van Nieuwenhove, Constantin Miaka Mia Bilenge et Philippe Büscher, « Equivalence trial of melarsoprol and nifurtimox monotherapy and combination therapy for the treatment of second-stage Trypanosoma brucei gambiense sleeping sickness », J. Infect. Dis., vol. 195, no 3, , p. 322–329 (PMID 17205469, DOI 10.1086/510534)
- (en) « Page Not Found », sur accessmedicine.com via Wikiwix (consulté le ).
- Büscher P, Cecchi G, Jamonneau V, Priotto G, Human african trypanosomiasis, Lancet, 2017;390:2397-2409
- Graf FE, Ludin P, Wenzler T et al. Aquaporin 2 mutations in Trypanosoma brucei gambiense field isolates concur with decreased susceptibility to pentamidine and melarsoprol, PLoS Negl Trop Dis, 2013;7;e2475
- « Melarsoprol versus Eflornithine for Treating Late-stage Gambian Trypanosomiasis in the Republic of the Congo », dans Bulletin of the World Health Organization, vol. 84, no 10, Genève, octobre 2006.
- Kuepfer I, Schmid C, Allan M et al. Safety and efficacy of the 10-day melarsoprol schedule for the treatment of second stage Rhodesiense sleeping sickness, PLoS Negl Trop Dis, 2012;6:e1695
- (en) François Chappuis, Nitya Udayraj, Kai Stietenroth, Ann Meussen et Patrick A. Bovier, « Eflornithine is Safer than Melarsoprol for the Treatment of Second-stage Trypanosoma brucei gambiense Human African Trypanosomiasis », Clin. Infect. Dis., vol. 41, no 5, , p. 748–751 (PMID 16080099, DOI 10.1086/432576)
- (en) M. G. Etchegorry, J. P. Helenport, B. Pecoul, J. Jannin et D. Legros, « Availability and Affordability of Treatment for Human African Trypanosomiasis », dans Trop. Med. Int. Health., vol. 6, 2001, pp. 957-959.
- (en) M. Balasegaram, H. Young, F. Chappuis, G. Priotto, M. E. Raguenaud et F. Checchi, « Effectiveness of Melarsoprol and Eflornithine as First-line Regimens for Gambiense Sleeping Sickness in Nine Médecins sans Frontières Programmes », dans Trans. R. Soc. Trop. Med. Hyg., vol. 103, 2009, pp. 280-290.
- WHO Model List of Essential Medicines, 18th list, avril 2013