Hyperparathyroïdie
| Médicament | Paricalcitol, Dihydrotachystérol (en), calcitriol, doxercalciferol (en) et denosumab |
|---|---|
| Spécialité | Endocrinologie |
| CIM-10 | E21 |
|---|---|
| CIM-9 | 252.0 |
| OMIM | 145001 et 610071 145000, 145001 et 610071 |
| DiseasesDB | 20710 |
| MedlinePlus | 001215 |
| eMedicine |
127351 med/3200 |
| MeSH | D006961 |
| Patient UK | Hyperparathyroidism-pro |
L'hyperparathyroïdie est une production anormalement élevée d'hormone parathyroïdienne (PTH) par les glandes parathyroïdes. Celle-ci peut être primaire ou secondaire.
L'augmentation de PTH entraîne une augmentation du taux de calcium plasmatique. Cette hypercalcémie est due à l'augmentation de la résorption osseuse par les ostéoclastes, la réduction de l'élimination rénale du calcium et l'augmentation de l'absorption intestinale de calcium. L'hypercalcémie chronique peut causer une néphrocalcinose et une insuffisance rénale. La résorption osseuse excessive provoque une ostéomalacie.
Causes modifier
Hyperparathyroïdie primaire modifier
L'hyperparathyroïdie primaire est due à un dysfonctionnement au sein des glandes parathyroïdes elles-mêmes, avec hypersécrétion de PTH. Elle est due dans 85 % des cas à un adénome sécrétant d'une glande parathyroïde, le restant des cas correspondant surtout à une hyperplasie de plusieurs de ces glandes[1].
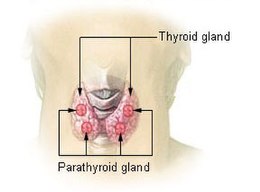
La parathyroïde est, le plus souvent, située derrière la glande thyroïde mais il existe des localisations atypiques dans environ 15 % des cas[2], rendant le diagnostic plus délicat. L'adénome est exceptionnellement cancéreux. Il existe de rares cas familiaux dont certains dans le cadre d'une néoplasie endocrinienne multiple type 1 ou de type 2a.
Certains médicaments interfèrent avec la parathormone. Ainsi les diurétiques thiazidiques pourraient favoriser l'apparition d'une hyperparathyroïdie primaire[3]. De même, l'utilisation chronique de sels de lithium provoque une augmentation du taux de parathormone[4]. L'irradiation de la région cervicale peut également favoriser une hyperparathyroïdie[5].
Il existe également une cause génétique pour l'hyperparathyroïdie : l'hyperparathyroïdie néonatale sévère. Cette condition est due à une mutation du gène codant le récepteur sensible au calcium. La mutation est de type récessive, et lorsque l'individu est hétérozygote de ce gène, il est prédisposé à une hypercalcémie hypocalciurique bénigne familiale. Néanmoins, lorsque l'individu possède le gène muté en double (homozygote), il est atteint d'hyperparathyroïdie néonatale sévère. Cette condition est menaçante chez l'individu puisque les glandes parathyroïdes ne répondent plus aux variations de concentration de Ca2+ plasmatique. En effet, le récepteur sensible au calcium est un récepteur qui joue un rôle essentiel dans l'homéostasie du calcium et dans la régulation de la sécrétion de la PTH : ce récepteur est un récepteur couplé à une protéine G (RCPG) de classe C. Lorsque le calcium augmente dans le milieu extracellulaire, il agit sur les récepteurs sensibles aux calcium (RCPG) présents à la surface de la membrane des cellules parathyroïdiennes. La liaison (de faible affinité) au récepteur active une protéine Gq, qui enclenche la voie de transduction par la phospholipase C (de type Beta). La phospholipase C clive alors un phospholipide membranaire très important dans la transduction de signal : le PIP2 (Le phosphatidylinositol 1,4-biphosphate). Le PIP2 est clivé en DAG (diacylglycérol) et IP3 (inositol 1,4,5-triphosphate). L'IP3 agit sur des récepteurs présents au niveau du réticulum endoplasmique, site de séquestration du Ca2+, et augmente la concentration de Ca2+ cytoplasmique. Cette élévation du calcium, même moindre, a un effet inhibiteur sur la libération des vésicules contenant la PTH. Le récepteur sensible au calcium est donc très important dans la libération de la PTH par les glandes parathyroïdiennes. En cas de mutation, la glande est totalement insensible aux variations de calcium et ne peut donc pas y répondre. Le Ca2+ agissant par feedback négatif sur la sécrétion de la PTH, la maladie résulte en une hypercalcémie sévère et un taux plasmatique de PTH anormalement élevé.
Hyperparathyroïdie secondaire modifier
L'hyperparathyroïdie secondaire est due dans la moitié des cas à un déficit en vitamine D, avec un facteur aggravant en cas d'insuffisance rénale chronique[6]. Le rein étant normalement chargé de synthétiser le calcitriol, en cas d'insuffisance rénale, une hyperparathyroïdie secondaire peut se développer par hyperplasie réactionnelle ce qui permet de compenser en partie ce défaut, en synthétisant davantage de parathormone (les deux hormones étant hypercalcémiantes). L'hyperphosphatémie développée en réponse à une maladie rénale chronique contribue également à l'hyperparathyroïdie secondaire[7].
Il peut aussi exister une hyperparathyroïdie secondaire par hyperplasie réactionnelle d'origine alimentaire, en cas de carence en calcium et d'excès en phosphore. Celle-ci permet alors aussi de compenser ces défauts.
Enfin, ce phénomène peut survenir dans le cadre d'un syndrome paranéoplasique, lorsque les cellules cancéreuses sécrètent des substances PTH-like.
Hyperparathyroïdie tertiaire modifier
L'hyperparathyroïdie est dite tertiaire lorsque la sécrétion de PTH devient autonome par rapport à la calcémie. Elle s'observe après une hyperparathyroïdie secondaire ou au stade terminal de néphropathies au long cours[7].
Physiopathologie modifier
L'augmentation de l'hormone parathyroïdienne entraîne une augmentation de la résorption osseuse par les ostéoclastes ce qui a pour conséquence une augmentation du calcium plasmatique et une diminution des phosphates plasmatiques (mécanisme indirect par la 1-alpha-hydroxylase pour les phosphates).
La calciurèse et la phosphaturie sont augmentées.
Épidémiologie modifier
La prévalence de l'hyperparathyroïdie primaire est d'environ trois personnes sur 1 000 dans la population générale. Elle est plus élevée chez la femme de 55 à 75 ans[8].
Signes et symptômes modifier
Près de quatre cinquièmes des patients en hyperparathyroïdie sont asymptomatiques[1] et la maladie est découverte lors d'un bilan sanguin fait pour une tout autre raison et montrant une hypercalcémie.
La lyse osseuse peut provoquer une ostéoporose pouvant se compliquer de fractures. Elle peut ne pas s'accompagner d'hypercalcémie et serait, dans ce cas, une forme débutante d'hyperparathyroïdie[9].
L'hypercalcémie peut être cause d'une insuffisance rénale, de lithiases, de troubles digestifs (à type de nausées et constipations le plus souvent), de pancréatites. Un taux important de calcium sanguin peut conduire à des troubles de la vigilance ou à des troubles cognitifs (perte de mémoire et difficultés à se concentrer). Si ce taux est modérément élevé, on peut n'avoir qu'une simple asthénie.
Outre ces symptômes, l'hyperparathyroïdie peut s'accompagner de troubles du sommeil, de douleurs osseuses, de dépression ou de céphalées[7].
L'adénome parathyroïdien est, en règle générale, non palpable.
Diagnostic modifier
Biologie modifier
Le diagnostic se fait essentiellement par la mesure du taux de PTH et de calcium dans le sang.
Le dosage de la calcémie doit être couplé avec celui de l'albumine sanguine pour calculer la « calcémie corrigée », une hyperalbuminémie pouvant élever artificiellement le taux de calcium sanguin. L'excrétion urinaire du calcium est augmentée, sauf dans les cas rares d'hypercalcémie familiale hypocalciurique.
Le dosage de la parathormone montre des taux élevés ou « normal haut ».
L'estimation de la fonction rénale (dosage de la créatinine sanguine) permet de déceler une insuffisance rénale qui peut être cause d'hyperparathyroïdie secondaire.
Imagerie modifier
La localisation de l'adénome sécrétant est importante pour déterminer la stratégie du traitement. L'échographie et la scintigraphie au sestamibi sont les deux imageries historiquement les plus utilisés dans cette indication. Elles possèdent une sensibilité et une spécificité équivalente[10]. Depuis peu la TEP à la 18F-choline couplée au scanner tend à remplacer la scintigraphie au sestamibi grâce à ses performances diagnostiques excellentes[11],[12].
Traitement modifier
Le traitement des hyperparathyroïdies primaire et tertiaire consiste au retrait chirurgical de l'adénome, qu'il soit unique ou multiple[7]. Celui de l'hyperparathyroïdie secondaire est celui de la cause (insuffisance rénale, carence en vitamine D).
Chirurgie modifier
Afin d’être traitée, l’hyperparathyroïdie primaire requiert une intervention chirurgicale nommée parathyroïdectomie. Il existe différentes approches chirurgicales, qui vont de la chirurgie classique (incision conséquente de 4 à 5 cm), à une chirurgie communément appelée chirurgie mini-invasive (incision de 2 à 3 cm) mais nécessitant la localisation précise de l'adénome en pré-opératoire. Ce dernier type de chirurgie a une efficacité comparable à l'approche classique[13].
Outre la normalisation du taux de PTH et de la calcémie, la chirurgie pourrait réduire le risque de fractures dans les cas d'hyperparathyroïdie primaire asymptomatique[13].
En cas d'exérèse de l'ensemble des adénomes ectopiques, la réimplantation d'un fragment de glande parathyroïdique dans le muscle sternocléïdomastoïdien ou en sous-cutané dans l'avant-bras peut être envisagée afin d'éviter le risque d'hypoparathyroïdie[7].
Traitement non invasif de l'hyperparathyroidie modifier
L’ablation non invasive des adénomes parathyroïdiens peut utiliser le principe des ultrasons focalisés de haute intensité (HIFU) par application d'une quantité d’énergie acoustique à un espace confiné, aboutissant ainsi à une nécrose localisée des tissus par effet thermique.
Traitement médical modifier
Il repose sur les médicaments diminuant la résorption osseuse, en l'absence de chirurgie : estrogènes[14], bisphosphonates, raloxifène[15]. Le cinacalcet[16] et l'ételcalcétide se fixent sur les récepteurs au calcium de la parathyroïde, inhibant la sécrétion de cette dernière.
L'utilisation des bisphosphonates est contre-indiquée après une chirurgie parathyroïdienne[17].
Voir aussi modifier
Notes et références modifier
- (en) Pallan S, Omair Rahman M, Khan AA, « Diagnosis and management of primary hyperparathyroidism » BMJ 2012;344:e1013
- (en) Phitayakorn R, McHenry CR, « Incidence and location of ectopic abnormal parathyroid glands » Am J Surg. 2006;191:418-23
- (en) Wermers RA, Kearns AE, Jenkins GD, Melton LJ 3rd. « Incidence and clinical spectrum of thiazide-associated hypercalcemia » Am J Med. 2007;120:911.e9-15.
- (en) Haden ST, Stoll AT, McCormick S, Scott J, Fuleihan G el-H, « Alterations in parathyroid hormone dynamics in lithium-treated subjects » J Clin Endocrinol Metab. 1997;82:2844-8
- (en) Schneider AB, Gierlowski TC, Shore-Freedman E, Stovall M, Ron E, Lubin J, « Dose-response relationships for radiation-induced hyperparathyroidism » J Clin Endocrinol Metab. 1995;80:254-7
- Alain Krivitzky, « Déficit vitaminique D et hyperparathyroïdie primaire : quelles conséquences pour la prise en charge ? Mises au point cliniques d’Endocrinologie », sur sfendocrino.org,
- « Hyperparathyroïdie - Troubles endocriniens et métaboliques », sur Édition professionnelle du Manuel MSD (consulté le )
- (en) Adami S, Marcococci C, Gatti D, « Epidemiology of primary hyperparathyroidism in Europe » J Bone Miner Res. 2002;17(suppl 2):N18-23
- (en) Lowe H, McMahon DJ, Rubin MR, Bilezikian JP, Silverberg SJ, « Normocalcemic primary hyperparathyroidism: further characterization of a new clinical phenotype » J Clin Endocrinol Metab. 2007;92:3001-5
- (en) Cheung K, Wang TS, Farrokhyar F, Roman SA, Sosa JA, « A meta-analysis of preoperative localization techniques for patients with primary hyperparathyroidism » Ann Surg Oncol. 2012;19:577-83
- (en) Luca Giovanella, Lorenzo Bacigalupo, Giorgio Treglia et Arnoldo Piccardo, « Will 18F-fluorocholine PET/CT replace other methods of preoperative parathyroid imaging? », Endocrine, vol. 71, no 2, , p. 285–297 (ISSN 1355-008X et 1559-0100, DOI 10.1007/s12020-020-02487-y, lire en ligne, consulté le )
- (de) Gregor Schweighofer-Zwink, Lukas Hehenwarter, Gundula Rendl et Lukas Rettenbacher, « Darstellung und Lokalisation von Nebenschilddrüsenadenomen mit F‑18 Cholin PET/CT », Wiener Medizinische Wochenschrift, vol. 169, nos 1-2, , p. 15–24 (ISSN 0043-5341 et 1563-258X, DOI 10.1007/s10354-018-0660-0, lire en ligne, consulté le )
- (en) Udelsman R, Pasieka J Sturgeon C, Young JCM, Clark O, « Surgery for asymptomatic primary hyperparathyroidism » J Clin Endocrinol Metab. 2009;94:366-72
- (en) Grey AB, Stapleton JP, Evans MC, Tatnell MA, Reid IR, « Effect of hormone replacement therapy on bone mineral density in postmenopausal women with mild primary hyperparathyroidism. A randomized, controlled trial » Ann Intern Med. 1996;125:360-8
- (en) Rubin MR, Lee KH, McMahon DJ, Silverberg SJ, « Raloxifene lowers serum calcium and markers of bone turnover in postmenopausal women with primary hyperparathyroidism » J Clin Endocrinol Metab. 2003;88:1174-8
- (en) Peacock M, Bilezikian JP, Klassen PS, Guo MD, Turner SA, Shoback D, « Cinacalcet hydrochloride maintains long-term normocalcemia in patients with primary hyperparathyroidism » J Clin Endocrinol Metab. 2005;90:135-41
- Elsevier Masson, « Hyperparathyroïdie », sur EM-Consulte, (consulté le )