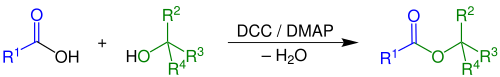Estérification de Steglich
L'estérification de Steglich est une variation d'estérification utilisant le dicyclohexylcarbodiimide comme agent de couplage et le 4-diméthylaminopyridine comme catalyseur. Cette réaction a été décrite pour la première fois par Wolfgang Steglich (de) en 1978[1]. C'est une adaptation d'une méthode plus ancienne pour la formation d'amides en utilisant le dicyclohexylcarbodiimide (DCC) et le 1-hydroxybenzotriazole (HOBT)[2],[3].
Cette réaction est généralement réalisée à température ambiante. Le dichlorométhane peut être utilisé comme solvant. Les conditions de la réaction étant vraiment douces, elle permet de former des esters qui ne peuvent être obtenus par d'autres méthodes, comme ceux de l'acide 1,4-dihydroxybenzoique. Une caractéristique de cette réaction est la consommation d'eau durant la réaction par le DCC, qui forme un des composés de l'urée, la dicyclohexylurée (DCU).
Mécanisme réactionnel modifier
Le mécanisme réactionnel est décrit de la manière suivante :
Avec les amines, cette réaction se déroule sans aucun problème pour former les amides correspondants car les amines sont plus nucléophiles. Si l'estérification est lente, une réaction parallèle peut agir et diminuer le rendement final ou rendre plus difficile la purification du produit. Cette réaction est un 1,3-réarrangement de l'intermédiaire O-acyl en une urée N-acyl qui ne peut réagir avec l'alcool. Le DMAP peut être utilisé pour supprimer cette réaction, en agissant de la manière suivante :
En fait, tout groupe carboxyle (>C=O) s'ajoute rapidement sur une des doubles liaisons C=N du DCC, formant le dérivé O-acyl urée correspondant. Cet intermédiaire est très réactif, sa réactivité étant comparable à celle d'un anhydride d'acide[4], de sorte qu'il est rapidement et facilement converti en amide par réaction sur une amine. Pour son couplage avec des alcools, un agent d'acyl-transfert comme DMAP est en outre nécessaire.
Notes et références modifier
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Steglich esterification » (voir la liste des auteurs).
- B. Neises, W. Steglich, « Simple Method for the Esterification of Carboxylic Acids », Angew. Chem. Int. Ed., vol. 17, no 7, , p. 522–524 (DOI 10.1002/anie.197805221)
- J. C. Sheehan, G. P. Hess, « A New Method of Forming Peptide Bonds », J. Am. Chem. Soc., vol. 77, no 4, , p. 1067–1068 (DOI 10.1021/ja01609a099)
- W. König, R. Geiger, « Eine neue Methode zur Synthese von Peptiden: Aktivierung der Carboxylgruppe mit Dicyclohexylcarbodiimid unter Zusatz von 1-Hydroxy-benzotriazolen », Chem. Ber., vol. 103, no 3, , p. 788–798 (DOI 10.1002/cber.19701030319)
- R. Milcent et F. Chau, Chimie organique hétérocyclique : Structures fondamentales, chimie et biochimie des principaux composés naturels, EDP Sciences, 2003. (ISBN 9782868835833), présentation en ligne