Lanthionine
| Lanthionine | |
| |
| Identification | |
|---|---|
| Nom UICPA | acide (2R,2'R)-3,3'sulfanediyl-di(2-aminopropanoïque) |
| Synonymes |
3,3'-thiobis-L-alanine |
| No CAS | |
| No ECHA | 100.011.888 |
| No CE | 213-076-7 |
| PubChem | 256406 |
| ChEBI | 21347 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C6H12N2O4S [Isomères] |
| Masse molaire[1] | 208,235 ± 0,012 g/mol C 34,61 %, H 5,81 %, N 13,45 %, O 30,73 %, S 15,4 %, |
| Propriétés physiques | |
| T° fusion | 280-283 °C |
| Solubilité | 1 500 mg·l dans l'eau |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
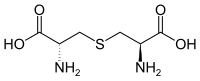
La lanthionine est un acide aminé non protéinogène de formule semi-développée HOOC–CH(NH2)–CH2–S–CH2–CH(NH2)–COOH. Comme l'analogue cystine, la lanthionine est composée de deux résidus alanine réticulés sur leur atome de carbone β par une liaison thioéther.
La lanthionine a d'abord été isolée, en 1941, par traitement de la laine avec du carbonate de sodium (Na2CO3)[2] et a été synthétisée, pour la première fois, par réaction de la cystéine et de la β-chloroalanine[3]. Les différents stéréoisomères de la lanthionine se retrouvent largement dans la nature et ont été isolés à partir de cheveux humains, de lactalbumine (en) et de plumes. Les lanthionines ont également été trouvées dans les parois cellulaires de bactéries et sont les composantes d'un groupe d'antibiotiques appelés lantibiotiques qui sont des peptides génétiquement codés et comprennent la nisine, la subtiline, l'épidermine (un composé anti-staphylocoque et streptocoque) et l'ancovénine (un inhibiteur d'enzyme)[4],[5].
Préparation modifier
Une large gamme de synthèses des lanthionines a été publiée notamment une désulfurisation à partir de la cystéine[6], une ouverture de cycle de la sérine β-lactone[5] et l'addition hétéro-conjuguée de la cystéine sur la déshydroalanine[7]. La méthode par désulfurisation est cependant la seule voie vers une lanthionine qui ait été employée pour la synthèse totale d'un lantibiotique.
Notes modifier
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Isolation of a New Sulfur-Containing Amino Acid (Lanthionine) from Sodium Carbonate-Treated Wool, Horn, M. J.; Jones, D. B.; Ringel, S. J.; Journal of Biological Chemistry, 1941, vol. 138, p. 141-149.
- The Stereoisomeric Forms of Lanthionine, Brown, G. B.; du Vigneaud, V.; Journal of Biological Chemistry, 1941, vol. 140, p. 767-771.
- Chemical and Enzymatic Synthesis of Lanthionines, Paul, M.; van der Donk, W. A.; Mini-Reviews in Organic Chemistry, 2005, vol. 2, p. 23-37.
- A Facile Synthesis of Orthogonally Protected Stereoisomeric Lanthionines by Regioselective Ring Opening of Serine β-Lactone Derivatives, Shao, H.; Wang, S. H. H.; Lee, C.-W.; Ösapay, G.; Goodman, M.; Journal of Organic Chemistry, 1995, vol. 60, p. 2956-2957.
- Preparation and Mass Spectral Properties of Cystine and Lanthionine Derivatives. Novel Synthesis of L-Lanthionine by Selective Desulfurization, Harpp, D. N.; Gleason, J. G.; Journal of Organic Chemistry, 1971, vol. 36, p. 73-80.
- Lanthionines for Solid Phase Synthesis, Probert, J. M.; Rennex, D.; Bradley, M.; Tetrahedron Letters, 1996, vol. 37, p. 1101-1104.
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Lanthionine » (voir la liste des auteurs).