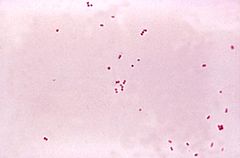
Neisseria meningitidis
Neisseria meningitidis, également connue sous le nom de meningococcus ou méningocoque, est une bactérie diplocoque gram-négative connue pour son rôle dans les méningites.
| Domaine | Bacteria |
|---|---|
| Embranchement | Proteobacteria |
| Classe | Betaproteobacteria |
| Ordre | Neisseriales |
| Famille | Neisseriaceae |
| Genre | Neisseria |
Écologie et pouvoir pathogène
modifierLes méningocoques sont des germes que l'on ne trouve que chez les humains, dans le rhinopharynx, où ils peuvent provoquer une rhinopharyngite bénigne ou un état de portage asymptomatique. On peut rester porteur pendant plusieurs mois ou même des années. Dans une population normale, on trouve 5 à 10 % de porteurs mais ce taux peut atteindre 50 à 75 % dans certaines communautés denses (casernes, pensionnats).
Pour des raisons mal connues (certains auteurs évoquent une déficience immunitaire, notamment une production médiocre ou trop tardive d'IgM ; d'autres évoquent aussi un rôle adjuvant du refroidissement évoqué par une fréquence maximale en hiver et au printemps, du surmenage et de la promiscuité), une personne seulement sur environ 400 porteurs devient victime d'une infection méningococcique grave. Celle-ci se présente le plus souvent sous forme de méningite aiguë purulente. Le méningocoque pourrait se faufiler du rhinopharynx aux méninges en suivant le trajet des nerfs olfactifs. Le plus souvent cependant, ce serait par voie sanguine que le méningocoque atteindrait le système nerveux (SNC). Il y a en effet presque constamment méningococcémie au début de la méningite. Cette septicémie peut être asymptomatique, soit ajouter au syndrome méningé une éruption purpurique (que l'on trouve, suivant les épidémies, dans 10 à 50 % des cas de méningites), soit encore dans 5 à 10 % des cas, se présenter sous forme de purpura fulminans, rapidement mortel, avant même que se développe la méningite. Ces formes suraiguës sont désignées sous le nom de syndrome de Waterhouse-Friderichsen. Dans ces cas, l'endotoxine, en contractant les veines intrahépatiques, provoque l'accumulation de sang en amont de ces veines, d'où hémorragies capillaires (dans les surrénales entre autres), thromboses intravasculaires et collapsus circulatoire.
Épidémiologie
modifierL'épidémiologie varie en fonction de 4 facteurs.
Le facteur périodique
modifierLa fréquence des méningococcies dans une population subit des oscillations lentes, amenant un sommet tous les 7 à 11 ans. C'est ainsi qu'en Belgique de 1960 à 1969 le nombre des cas déclarés par an était de 30 à 40, il a dépassé la centaine en 1970 et dépassé 500 en 1971 et 1972. La Hollande et l'Allemagne ont connu une situation similaire 2 ou 3 ans plus tôt.
L'âge
modifierLa fréquence des méningites néonatales est d'environ 0,4 %. Les microbes responsables de méningites purulentes, chez le nouveau-né, sont surtout des entérobactéries, parfois des listerias ou des streptocoques hémolytiques de type B. Chez les bébés et enfants, le méningocoque prédomine (50 à 80 % des méningites à cet âge), suivi du pneumocoque (plus ou moins 20 % surtout chez l'enfant plus âgé) et de l'haemophilus (10 à 20 % surtout chez l'enfant plus jeune). Au-delà de 15 ans, le pneumocoque passe en tête (35 %), suivi du méningocoque (20 %) et de germes divers.
En aout 2022, une épidémie causée par un nouveau variant du méningocoque B touche principalement les jeunes de 16 à 21 ans dans l'est Lyonnais[1].
Genre de communauté
modifierOn observe parfois une fréquence accrue par rapport à celle de la population générale, dans des communautés d'enfants ou de jeunes adultes vivant en contact assez étroit, dans lesquelles un noyau de personnel permanent constitue un réservoir de porteurs de germes, qui contaminent les nouvelles recrues (camps d'entraînement militaire aux États-Unis et en Grande-Bretagne, camps de travailleurs, écoles, etc.). Le taux de portage d'environ 5 % chez les entrants passe en quelques semaines à 60 - 80 %, avec éventuellement apparition de cas cliniques. Ceci explique que l'on peut observer deux sommets dans la répartition en fonction de l'âge: un premier entre 3 mois et 10 ans, le second entre 18 et 22 ans avec, pour ce second sommet, une prédominance masculine.
Facteur géographique
modifierUn aspect ėpidémiologique spécifique à l’Afrique a été décrit par Léon Lapeyssonnie en 1963[2]. Etudiant les circonstances des graves épidémies observées au XXe siècle il a montré que celles-ci surviennent dans un espace qui ceinture l'Afrique du Sénégal à l'ouest à l'Éthiopie à l'est, et qui est limité par deux niveaux de pluviométrie (on parle d'isohyète). Au nord l'isohyète 300 mm et au sud l'isohyète 1 100 mm. C'est-à-dire que toute la zone africaine où il pleut entre 300 et 1 100 mm d'eau par an, et dont la population est estimée à 450 millions de personnes est particulièrement exposée au risque d’épidémies saisonnières. On nomme depuis lors cet espace du nom de ceinture africaine de la méningite. Le méningocoque étant fort fragile dans les milieux extérieurs (surtout à cause de la dessiccation), la transmission par gouttelettes de mucus exige des contacts assez proches. Mais étant donné le grand nombre de porteurs de germes, il n'est généralement pas possible d'établir une filiation entre deux cas successifs. Il est rare d'observer plusieurs cas dans une même famille ou une même classe.
Malgré l'efficacité remarquable de l'antibiothérapie, il subsiste une mortalité de 10 à 15 %[3], due surtout aux méningococcémies fulminantes, où la mort peut survenir en quelques heures, avant même que le diagnostic et le traitement puissent intervenir.
Propriétés bactériologiques
modifierMorphologie
modifierDiplocoques gram négatifs en grains de café associés par leur côté aplati, éventuellement intracellulaires dans les produits pathologiques (LCR). Elles sont généralement encapsulées.
Culture
modifierÀ la fois fragiles et exigeants, les méningocoques doivent être ensemencés rapidement sur des milieux enrichis (sang ou liquide d'ascite), en atmosphère humide et de préférence enrichie en CO2 (5 à 10 % : jarre à la bougie). Légèrement trouble en milieux liquides (généralement peu favorables) ; colonies lisses, translucides, de 1 à 3 mm, non hémolytiques sur gélose au sang, ils sont ensemencés généralement sur gélose - chocolat (hémoglobine chauffée) ou éventuellement sur gélose - ascite.
Les méningocoques n'infectent que les humains et pas les autres animaux car la bactérie n'arrive pas à utiliser le fer d'une source autre qu'une source humaine[4].
Enzymes et toxines
modifierSeule l'endotoxine, qui est facilement libérée vu la tendance spontanée de ce germe à l'autolyse, est retrouvée dans le purpura fulminans.
Antigènes
modifierÀ côté d'antigènes protéiques communs qui ne semblent guère jouer de rôle, les méningocoques possèdent des antigènes polysaccharidiques permettant de les subdiviser en type A, B, C (et quelques types rares). Classiquement, c'est le type A qui est considéré comme responsable des « épidémies », les types B et C donnant plutôt des cas sporadiques, le type B étant le plus courant en France et dans divers pays européens. D'autres types ont été décrits, W et Y.
Le typage est assez délicat : les sérums commerciaux sont de qualités variables et inégales d'un lot à l'autre. Il s'effectue généralement en émulsionnant, sur lame, dans une goutte de sérum spécifique, une culture jeune. Il importe de faire un contrôle dans une goutte de sérum normal car certaines cultures sont auto-agglutinables et donc non typables.
Méthodes de diagnostic
modifierMéningite
modifierLe liquide cérébrospinal, généralement trouble et purulent, doit être examiné le plus rapidement possible, vu la fragilité du germe (autolyse).
L'examen microscopique du culot de centrifugation doit être soigné et prolongé car les méningocoques sont habituellement très peu nombreux.
La culture sur milieu adéquat confirme l'examen microscopique ou révélera les méningocoques trop rares pour être vus au microscope.
Dans un certain nombre de cas (les plus aigus, semble-t-il), ces deux analyses restent négatives. On pourrait dans ces cas, révéler dans le LCR, les Ag libérés par les méningocoques lysés. Actuellement les recommandations sur l'utilisation des antibiotiques avant la réalisation de tout prélèvement microbiologique dans un contexte de purpura fulminans[5] ont favorisé le développement de techniques de biologie moléculaire pour la détection du méningocoque dans le LCR et dans les biopsies de lésions purpuriques.
Méningococcémie
modifierL'hémoculture doit être pratiquée systématiquement. Elle peut être positive alors que la recherche dans le LCR est négative. En cas de purpura, on peut éventuellement révéler le méningocoque par examen microscopique ou culture du produit de ponction d'une tache purpurique.
Porteurs de germes
modifierLe problème est tout différent : la présence d'une flore commensale variée, comprenant notamment des Neisserias non pathogènes, entraîne la nécessité de milieux sélectifs. Le milieu VCN comprenant de la vancomycine inhibant les Gram positifs, de la colimycine inhibant les autres Gram négatifs et de la nystatine pour supprimer les monilias éventuels. Les colonies suspectes devront être identifiées par les caractères biochimiques des méningocoques et par agglutination à l'aide des sérums spécifiques.
Traitement
modifierIl va de soi que les malades sont isolés, mais cet isolement se justifie davantage par la gravité de leur état que comme mesure de prophylaxie, puisqu'en fait ce sont bien plus les porteurs que les malades qui disséminent l'infection.
Dans tout groupe où l'on craint une augmentation du taux de portage (entourage des malades et personnel soignant), on peut instituer une antibioprophylaxie dans le but de débarrasser les porteurs de leurs germes.
Le dépistage systématique de porteurs de germes (dans une école par ex.) n'est généralement pas justifié. Il est plus logique de considérer d'office comme porteurs l'entourage immédiat du malade. Si plusieurs cas surviennent dans un groupe, une chimioprophylaxie de tout le groupe pourra se justifier.
Vaccination
modifierEn France, la HAS recommande la vaccination des nourrissons contre le méningocoque B à l'âge de 3 mois[6]. La vaccination contre le sérogroupe C est obligatoire avec une première dose à 5 mois[7].
Dans les années 1970, des spécialistes de l'armée américaine ont préparé des vaccins à base de polysaccharides spécifiques des types A et C et les premiers essais ont favorablement influencé la fréquence des cas. La vaccination était alors essentiellement monovalente (ne concernant qu'un seul sérotype). Un vaccin tétravalent (contre les sérogroupes A, C, W et Y) a été développé au début des années 2000 mais s'est révélé être assez peu efficace chez le nourrisson[8]. Une variante de ce vaccin est désormais utilisable chez le très jeune enfant, à partir de 6 semaines[9].
La conception du vaccin contre le méningocoque B a été plus difficile car le polysaccharide de paroi (utilisé dans le vaccin contre la forme A et C) est beaucoup moins immunogène[10]. Cinq autres antigènes entraînant une réaction immunitaire ont été trouvées et forment la base d'un vaccin[11]. Il est approuvé par l'Agence européenne des médicaments en 2012[12].
Deux vaccins coexistent : Bexsero® et Trumenba®. Les antigènes utilisés sont pour les deux vaccins fHbp, protéine de liaison du facteur H du système du complément. Dans le cas de Bexsero® sont ajoutés une protéine de liaison à l'héparine (NHBA), une adhésine A de la membrane externe (NadA) et des vésicules de la membrane externe de Neisseria meningitidis OMV. Il est difficile de savoir si les trois protéines utilisées sont incluses ou non dans les vésicules, ce qui semble probable. Toutes ces protéines sont recombinantes.
Antibiotiques
modifierL'antibioprophylaxie de référence est la rifampicine pendant deux jours. En cas de contre-indication, la ceftriaxone ou la ciprofloxacine, ainsi que la spiramycine sont recommandées[13].
Quant au traitement des cas, ce sont les béta-lactamines qui sont les plus indiquées, éventuellement en association avec des sulfamides (chez un individu normal, la pénicilline ne diffuse guère dans le LCR mais l'inflammation des méninges améliore considérablement ce passage ; par ailleurs l'injection intrarachidienne est inutile et dangereuse).
Les céphalosporines de 3e génération (céfotaxime ou ceftriaxone) seront souvent employées au début du traitement, c'est-à-dire avant que le diagnostic bactériologique ne soit posé, en particulier en présence d'un purpura fulminans. La vancomycine pourra être éventuellement ajoutée avant les résultats microbiologiques en cas de suspicion de pneumocoque chez l'enfant. En cas de contexte à risque d'infection à Listeria monocytogenes, on ajoutera de l'amoxicilline. Le traitement sera ensuite réévalué en fonction des résultats microbiologiques (culture, antibiogramme, antigène soluble, PCR, etc.)[14]
Notes et références
modifier- https://www.auvergne-rhone-alpes.ars.sante.fr/le-meningocoque-b-symptomes-risques-et-prevention
- Léon Lapeyssonnie, « La méningite cérébrospinale en Afrique », Bulletin of the World Health Organization, vol. 28, no Suppl., , p. 114 (ISSN 0042-9686).
- Erickson L, De Wals P, Complications and sequelae of meningococcal disease in Quebec, Canada, 1990-1994, Clin Infect Dis, 1998;26:1159-64
- Meningococcal Disease (2004) Humana Press, Andrew J. Pollard and Martin C.J. Maiden
- Conférence de consensus « Les méningites purulentes bactériennes »
- https://www.has-sante.fr/jcms/p_3273097/fr/meningocoques-b-la-has-recommande-la-vaccination-des-nourrissons
- https://vaccination-info-service.fr/Les-maladies-et-leurs-vaccins/Meningites-et-septicemies-a-meningocoques
- Rennels M, King J Jr, Ryall R et als. Dosage escalation, safety and immunogenicity study of four dosages of a tetravalent meningococcal polysaccharide diphtheria toxoid conjugate vaccine in infants, Pediatr Infect Dis J, 2004;23:429-435
- Autorisation de mise sur le marché européenne 2017 du Nimenrix®[1]
- Finne J, Leinonen M, Mäkelä PH, Antigenic similarities between brain components and bacteria causing meningitis: implications for vaccine development and pathogenesis, Lancet, 1983;2:355-357
- Giuliani MM, Adu-Bobie J, Comanducci M et al. A universal vaccine for serogroup B meningococcus, Proc Natl Acad Sci USA, 2006;103:10834-10839
- European Medicines Agency, European Medicines Agency recommends approval of first vaccine for meningitis B, novembre 2012
- Conseil supérieur d'hygiène publique de France
- Conférence de consensus. Les méningites purulentes bactériennes.
Article connexe
modifier- Méningite, article traitant de toutes les formes de méningites.
- Épidémie de méningites à Dieppe entre 2003 et 2013, due à une souche particulièrement virulente de B:14.
Lien externe
modifier
- Ressources relatives au vivant :
- Ressources relatives à la santé :
- Notices dans des dictionnaires ou encyclopédies généralistes :
- Neisseria Meningitidis blog
- Fondation canadienne de recherche et d'information sur la méningite
Bibliographie
modifier- (fr) Haut Conseil de la santé publique (2013), avis intitulé Recommandations de vaccination contre le méningocoque C au-delà de 24 ans, notamment chez les hommes ayant des relations sexuelles avec d’autres hommes (HSH) 01/07/2013