Liaison double
En chimie, une liaison double est une liaison entre éléments chimiques impliquant quatre électrons de valence au lieu de deux pour une liaison covalente simple. Il existe un grand nombre de liaisons doubles possibles, la plus commune étant sans doute celle entre deux atomes de carbone, notée C=C, qu'on trouve dans les alcènes et de nombreuses molécules biologiques tels que des acides gras insaturés et leurs dérivés. En formule topologique, la liaison double est représentée par deux lignes parallèles (=) entre les deux atomes liés, et en typographie, on utilise simplement le signe égal[1],[2].

Ce genre de liaisons peut aussi exister entre atomes de nombreux éléments, par exemple entre un atome de carbone et un atome d'oxygène (groupe carbonyle, C=O), entre deux atomes d'azote (groupe azo, N=N), entre un atome de carbone et un atome d'azote (imine, C=N) ou encore entre un atome d'oxygène et un atome de soufre (sulfoxydes, S=O). Les liaisons doubles sont plus fortes que les liaisons simples et sont également plus courtes. Leur ordre de liaison est de deux. Les liaisons doubles sont riches en électrons, ce qui les rend réactives en présence d'accepteurs d'électrons.

|

|

|
|

|
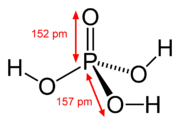
| Éthylène H2C=CH2 | Acétone (CH3)2C=O | Acide nitreux HON=O | Acide phosphorique (HO)3P=O | Diméthylsulfoxyde (CH3)2S=O |
Liaison modifier
Ce type de liaison peut être expliqué en termes d'hybridation d'orbitale. Dans l'éthylène, chaque atome de carbone possède trois orbitales sp2 et une orbitale p. Les trois orbitales sp2 sont situées dans un même plan, formant un angle de 120° entre elles, l'orbitale p étant perpendiculaire à ce plan. Lorsque deux atomes de carbone s'approchent, deux orbitales sp2 se recouvrent et forment une liaison σ. Les deux orbitales p se rapprochent également, toujours dans le même plan, et forment ensemble une liaison π. Pour un recouvrement maximum latéral, les deux orbitales p doivent rester parallèles, ce qui empêche par la suite toute rotation autour de la liaison centrale. Cette propriété donne naissance à une isomérie cis-trans. Les doubles liaisons sont aussi plus courtes pour permettre un recouvrement maximal des orbitales p.
| Deux orbitales sp2 (trois orbitales de cette nature par atome) s'approchent pour former une liaison σ sp2-sp2. |
Deux orbitales p se recouvrent pour former une liaison π parallèle à la liaison σ. |
Avec 133 pm (picomètres), la longueur de la liaison C=C dans l'éthylène est plus faible que celle de la liaison C–C de longueur 154 pm dans l'éthane. Cette double liaison est aussi plus forte (636 kJ/mol contre 368 kJ/mol) mais pas deux fois plus forte, la liaison π étant plus faible que la liaison σ car résultant d'un recouvrement latéral moins efficace.
En représentation alternative, la liaison double résulte du recouvrement de deux orbitales sp3 comme dans une liaison banane[3].
Variations modifier
Dans une molécule avec une alternance de liaisons simples et doubles, les orbitales peuvent se recouvrir entre de nombreux atomes en chaîne, menant à un système conjugué. Des phénomènes de conjugaison peuvent se produire par exemple dans des systèmes de type diènes (butadiène par exemple) ou d'énones. Dans les molécules cycliques, ces phénomènes de conjugaison peuvent mener à l'aromaticité. Dans de tels systèmes, les ordres de liaison ne sont plus strictement de 1 (liaison simple) et 2 (liaison double) mais ont une valeur entre ces deux nombres selon la nature des atomes et selon leurs positions respectives. Dans le cas du benzène, par exemple, l'indice de liaison entre n'importe quelle paire d'atomes de carbone adjacents tend vers 1,5.
Dans les cumulènes, deux liaisons doubles sont adjacentes.
Les liaisons doubles sont communes pour des éléments de la période 2 (tels que le carbone, l'azote ou l'oxygène) mais elles sont moins courantes pour des éléments de périodes plus élevées. Cependant les métaux peuvent eux aussi s'engager dans des liaisons multiples de type liaison multiple métal-ligand.
Analogues des alcènes du groupe 14 modifier
Il existe des analogues des alcènes avec des éléments du groupe 14 plus lourds que le carbone : silicium, germanium, étain, plomb. Ces composés ne sont cependant pas plans, comme les alcènes, mais ont une conformation gauche ou banane. Ces effets sont davantage prononcés pour les éléments les plus lourds. La longueur de la liaison Sn=Sn du distannène (Me3Si)2CHSn=SnCH(SiMe3)2 est à peine inférieure à celle d'une liaison simple, avec une liaison banane en coordination pyramidale au niveau de chacun des deux atomes d'étain. Ce composé se dissocie rapidement en solution pour former un stannanediyle (Me3Si)2CHSn: analogue à un carbène, dans lequel le doublet non liant est représenté par « : ». Les liaisons se forment avec deux accepteurs faibles tandis que le doublet non liant de chacun des deux atomes d'étain recouvre l'orbitale p vacante de l'autre[4],[5]. Dans les disilènes, en revanche, chaque atome de silicium présente une coordination plane mais les substituants sont en conformation gauche de sorte que l'ensemble de la molécule n'est pas plane. La liaison Pb=Pb des diplumbènes peut être plus longue que celle de la plupart des liaisons simples correspondantes[5]. Les plumbènes et les stannènes se dissocient généralement en monomères lorsqu'ils sont en solution, avec des enthalpies de liaison qui ne valent qu'une fraction de celle des liaisons simples correspondantes, certaines ayant une force de l'ordre d'une liaison hydrogène[4].
Types de double liaison entre atomes modifier
| C | O | N | S | |
|---|---|---|---|---|
| C | alcène | carbonyle | imine | thiocarbonyle |
| O | dioxygène | nitroso | sulfoxyde, sulfone, acide sulfinique, acide sulfonique | |
| N | azo | |||
| S | disulfure |
Notes et références modifier
- (en) Jerry March, Advanced Organic Chemistry: Reactions, Mechanisms, and Structure, 3e éd., Wiley, 1985. (ISBN 978-0471888413)
- (en) John McMurry, Organic Chemistry, 2e éd., Brooks/Cole, 2010. (ISBN 978-0495391470)
- (en) Francis A. Carey, 1937- (2007). Advanced organic chemistry, Richard J. Sundberg, 1938- 5e éd., Springer, 2007. (OCLC 154040953) (ISBN 978-0-387-44897-8)
- (en) Philip P. Power, « π-Bonding and the Lone Pair Effect in Multiple Bonds between Heavier Main Group Elements », Chemical Reviews, vol. 99, no 12, , p. 3463-3504 (PMID 11849028, DOI 10.1021/cr9408989, lire en ligne)
- (en) Yuzhong Wanga et Gregory H. Robinson, « Unique homonuclear multiple bonding in main group compounds », Chemical Communications, no 35, , p. 5201-5213 (PMID 19707626, DOI 10.1039/b908048a, lire en ligne)